Allgemeiner Implementierungsleitfaden (Version 3.2.1+20211001)
{{#if:
| {{{image}}}
| [[File:{{#switch:editnotice
| warning = Cmbox deletion.png
| editnotice = Information_icon.png
| system
| #default = Information_icon.png
}}|50px|link=|alt=]]
}} |
}}
Dieses Dokument gibt wieder:
Implementierungsleitfaden Allgemeiner Implementierungsleitfaden (Version 3) {{#if: 3.2.1+20211001| (3.2.1+20211001)|}}, OID: 1.2.40.0.34.7.1.9.3, Datum: 01.10.2021, Status: Normativ. Die Teilmaterialien gehören der Kategorie ILF an. |
{{#if:
| {{{imageright}}} |
| | warning | editnotice | system =
| #default =}}
Allgemeiner Implementierungsleitfaden für CDA Dokumente (Version 3)
Gesundheitswesen [1.2.40.0.34.7.1.9.3]
Inhaltsverzeichnis
- 1 Zusammenfassung
- 2 Informationen über dieses Dokument
- 3 Einleitung
- 4 Leitfadenerstellungs- und Harmonisierungsprozess
- 5 Technischer Hintergrund
- 6 Allgemeine Richtlinien für CDA-Implementierungsleitfäden
- 6.1 Konformitätskriterien
- 6.2 Der nullFlavor
- 6.3 Maximum-Set
- 6.4 Umgang mit codierten Informationen und Terminologien
- 6.5 Mehrsprachigkeit
- 6.6 Herkunft der Information
- 6.7 Zeitangaben
- 6.8 Terminologien
- 6.9 PDF Format-Vorschrift
- 6.10 Größenbeschränkung von eingebetteten Objekten
- 6.11 Verbot von CDATA
- 6.12 ELGA Interoperabilitätsstufen
- 7 Konformitätsprüfung
- 8 Datentypen
- 8.1 Identifikations-Elemente
- 8.2 Codierungs-Elemente
- 8.2.1 code-Element CS CNE
- 8.2.2 code-Element CD (Concept Descriptor)
- 8.2.2.1 Strukturbeispiele
- 8.2.2.1.1 Minimal-Variante um einen Code eindeutig darzustellen:
- 8.2.2.1.2 Gebräuchlichste Variante mit zusätzlichem Klartext für Code und Codesystem
- 8.2.2.1.3 Vollständige-Variante mit direkter Angabe des Textinhalts
- 8.2.2.1.4 Vollständige-Variante mit Referenz in den narrativen Textbereich
- 8.2.2.1.5 Vollständige-Variante mit Referenz in den narrativen Textbereich und Übersetzung in zwei andere Code-Systeme
- 8.2.2.2 Spezifikation
- 8.2.2.1 Strukturbeispiele
- 8.3 Zeit-Elemente
- 8.4 Kontaktdaten-Elemente
- 8.5 Namen-Elemente
- 8.6 Adress-Elemente
- 8.7 Messwert-Elemente
- 8.8 Verhältnisangabe RTO
- 8.9 Erfassung von Mengen (collection of quantities)
- 8.10 Komplexe (zusammengesetzte) Elemente
- 9 Dataset des Allgemeinen Implementierungsleitfadens
- 10 Administrative Daten (CDA Header)
- 10.1 Übersichtstabelle der CDA Strukturen des Headers
- 10.2 Übersicht der Zeitelemente im Header
- 10.3 Dokumentenstruktur
- 10.3.1 XML Prolog (XML Metainformationen)
- 10.3.2 Wurzelelement clinicalDocument
- 10.3.3 Hoheitsbereich des Dokuments ("realmCode")
- 10.3.4 Dokumentformat ("typeId")
- 10.3.5 ELGA Implementierungsleitfaden-Kennzeichnung ("templateId")
- 10.3.6 Dokumenten-Id ("id")
- 10.3.7 Dokumentenklasse ("code")
- 10.3.8 Titel des Dokuments ("title")
- 10.3.9 Status des Dokuments ("sdtc:statusCode")
- 10.3.10 Terminologiedatum ("hl7at:terminologyDate")
- 10.3.11 FormatCode ("hl7at:formatCode")
- 10.3.12 Fachliche Zuordnung des Dokuments ("hl7at:practiceSettingCode")
- 10.3.13 Erstellungsdatum des Dokuments ("effectiveTime")
- 10.3.14 Vertraulichkeitscode ("confidentialityCode")
- 10.3.15 Sprachcode des Dokuments ("languageCode")
- 10.3.16 Versionierung des Dokuments ("setId" und "versionNumber")
- 10.4 Teilnehmende Parteien
- 10.4.1 Patient ("recordTarget/patientRole")
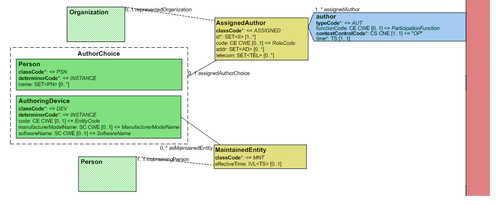
- 10.4.2 Verfasser des Dokuments ("author")
- 10.4.3 Personen der Dateneingabe ("dataEnterer")
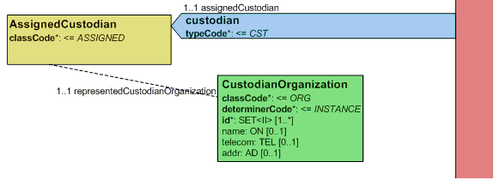
- 10.4.4 Verwahrer des Dokuments ("custodian")
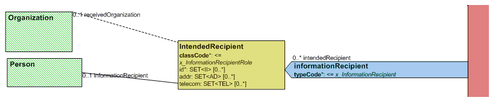
- 10.4.5 Beabsichtigte Empfänger des Dokuments ("informationRecipient")
- 10.4.6 Rechtlicher Unterzeichner ("legalAuthenticator")
- 10.4.7 Weitere Unterzeichner ("authenticator")
- 10.4.8 Weitere Beteiligte ("participant")
- 10.4.8.1 Festlegung der "Art" des Beteiligten
- 10.4.8.2 Fachlicher Ansprechpartner
- 10.4.8.3 Einweisender/Zuweisender/Überweisender Arzt
- 10.4.8.4 Hausarzt
- 10.4.8.5 Notfall-Kontakt/Auskunftsberechtigte Person
- 10.4.8.6 Angehörige
- 10.4.8.7 Versicherter/Versicherung
- 10.4.8.8 Betreuende Organisation
- 10.4.8.9 Weitere Behandler
- 10.5 Zuweisung und Ordermanagement
- 10.6 Dokumentation der Gesundheitsdienstleistung
- 10.7 Bezug zu vorgehenden Dokumenten
- 10.8 Einverständniserklärung
- 10.9 Informationen zum Patientenkontakt
- 11 Medizinische Inhalte (CDA Body)
- 11.1 Allgemeiner Aufbau des CDA Body
- 11.1.1 Unstrukturierter medizinischer Inhalt: nonXMLBody
- 11.1.2 Strukturierter medizinischer Inhalt: structuredBody
- 11.1.3 Sektionen
- 11.1.4 Textstrukturierung und Formatierung
- 11.1.4.1 Listen
- 11.1.4.2 Tabellen
- 11.1.4.3 Unterabschnitte
- 11.1.4.4 Referenzierter bzw. attribuierter Inhalt (content)
- 11.1.4.5 Erweiterte styleCodes
- 11.1.4.6 Zeilenumbrüche
- 11.1.4.7 Superscript und Subscript
- 11.1.4.8 Fußnoten
- 11.1.4.9 HTML-Verweise
- 11.1.4.10 Geschützte Leerzeichen
- 11.1.4.11 Verwendung von Revisionsmarken
- 11.1.5 Strukturen in Level 3
- 11.1.6 Untersektionen – Hierarchischer Aufbau
- 11.1.7 Einbetten von Dokumenten/Multimedia-Dateien
- 11.2 CDA Body in EIS "Basic"
- 11.3 Allgemeine Sektionen-Templates
- 11.3.1 Übersichtstabelle der allgemeinen Sektionen des CDA Bodys
- 11.3.2 Brieftext
- 11.3.3 Abschließende Bemerkung
- 11.3.4 Beilagen
- 11.3.5 Willenserklärungen und andere juridische Dokumente
- 11.3.6 Anmerkungen
- 11.3.7 Vitalparameter - kodiert
- 11.3.8 Vitalparameter - unkodiert
- 11.3.9 Übersetzung
- 11.3.10 Risiken
- 11.3.11 Hilfsmittel und Ressourcen
- 11.4 Maschinenlesbare Elemente
- 11.4.1 Eingebettetes Objekt Entry
- 11.4.2 Logo Entry
- 11.4.3 Vitalparameter Gruppe Entry
- 11.4.4 Vitalparameter Entry
- 11.4.5 Serienmessung Vitalparameter Entry
- 11.4.6 Serienmessung Entry
- 11.4.7 Serienmessungs-Gruppe Entry
- 11.4.8 Serienmessungs-Werte Entry
- 11.4.9 Serienmessungs-Periode Entry
- 11.4.10 Problem Concern Entry
- 11.4.11 Problem Entry
- 11.4.12 Severity Observation
- 11.4.13 Certainty Observation
- 11.4.14 Problem Status Observation
- 11.4.15 Comment Entry
- 11.4.16 External Document Entry
- 11.5 Sonstige Templates (Fragmente)
- 11.5.1 Address Compilation
- 11.5.2 Address Compilation Minimal
- 11.5.3 Assigned Entity
- 11.5.4 Assigned Entity with id, name, addr and telecom
- 11.5.5 Assigned Entity Body
- 11.5.6 Assigned Entity Body with name, addr and telecom
- 11.5.7 Author Body
- 11.5.8 Device Compilation
- 11.5.9 Informant Body
- 11.5.10 Laterality Qualifier
- 11.5.11 Narrative Text Reference
- 11.5.12 Organization Compilation with name
- 11.5.13 Organization Compilation with id, name
- 11.5.14 Organization Compilation with id, name, tel, addr
- 11.5.15 Organization Compilation with name, addr minimal
- 11.5.16 Organization Compilation with name, addr minimal and telecom
- 11.5.17 Organization Name Compilation
- 11.5.18 Original Text Reference
- 11.5.19 Participant Body
- 11.5.20 Performer Body
- 11.5.21 Person Name Compilation G1
- 11.5.22 Person Name Compilation G1 M
- 11.5.23 Person Name Compilation G2
- 11.5.24 Person Name Compilation G2 M
- 11.5.25 Time Interval Information minimal
- 11.1 Allgemeiner Aufbau des CDA Body
- 12 Liste der verwendeten Terminologien
- 13 Anhang
- 13.1 Anwendungsfälle für CDA-Dokumente in ELGA
- 13.1.1 Voraussetzungen für den Zugriff auf e-Befunde in ELGA
- 13.1.2 Schreiben und Einbringen von Dokumenten
- 13.1.3 Versionierung von Dokumenten
- 13.1.4 Stornierung von Dokumenten
- 13.1.5 Filtern und Suchen von Dokumenten
- 13.1.6 Lesen von ELGA Dokumenten
- 13.2 Abbildungsverzeichnis
- 13.3 Tabellenverzeichnis
- 13.4 Einzelnachweise
- 13.5 Literatur und Weblinks
- 13.6 Revisionsliste
- 13.6.1 Hauptversion 2020 (3.0.0+20200821)
- 13.6.2 Nebenversion 2020.1 (3.1.0+20201120)
- 13.6.2.1 recordTarget 1.2.40.0.34.6.0.11.1.3
- 13.6.2.2 Document code.translation 1.2.40.0.34.6.0.11.1.16
- 13.6.2.3 Problem Entry 1.2.40.0.34.6.0.11.3.6
- 13.6.2.4 Problem Concern Entry 1.2.40.0.34.6.0.11.3.7
- 13.6.2.5 Willenserklärungen und andere juridische Dokumente 1.2.40.0.34.6.0.11.2.61
- 13.6.2.6 Erweiterungen des Datentyps für effectiveTime
- 13.6.2.7 Vitalparameter - kodiert 1.2.40.0.34.6.0.11.2.46
- 13.6.2.8 Vitalparameter 1.2.40.0.34.6.0.11.2.46
- 13.6.2.9 Korrektur der Textreference
- 13.6.2.10 Schematron Assert in allen "Organization Compilation" Templates
- 13.6.3 Nebenversion 3.2.0+20210304
- 13.6.3.1 Document FormatCode 1.2.40.0.34.6.0.11.1.47 & Document PracticeSettingCode 1.2.40.0.34.6.0.11.1.44
- 13.6.3.2 DocumentLevelTemplate 1.2.40.0.34.6.0.11.0.3
- 13.6.3.3 8.4.1.2.1 telecom – Format Konventionen für Telekom-Daten
- 13.6.3.4 8.1.1 id-Element II
- 13.6.3.5 recordTarget 1.2.40.0.34.6.0.11.1.3
- 13.7 Erratum
- 13.1 Anwendungsfälle für CDA-Dokumente in ELGA
1 Zusammenfassung[Bearbeiten]
Dieser Implementierungsleitfaden beschreibt die Struktur- und Formatvorgaben für elektronische Dokumente im Österreichischen Gesundheitswesen, im Speziellen für den Einsatz in ELGA. Die Beschreibung enthält Festlegungen, Einschränkungen und Bedingungen auf Grundlage des internationalen Standards ISO/HL7 27932:2009 HL7 Clinical Document Architecture, Release 2.0 (CDA) und ist ein nationaler Standard der HL7 Austria.
Der Standard hat zum Ziel, einen umfassenden Austausch von semantisch interoperablen Informationen zwischen allen beteiligten Akteuren bei der Behandlung von Patienten zu ermöglichen. Der Datenaustausch findet hierbei nicht nur innerhalb einer Einrichtung, sondern auch zwischen kooperierenden Einrichtungen und über Sektorengrenzen hinaus statt. Die Empfänger der Dokumente sollen die Inhalte benutzen und weiterverwenden können, ohne sich vorher mit dem Ersteller absprechen zu müssen.
Der Implementierungsleitfaden enthält elementare Konzepte und erläutert das zugrunde liegende Modell, definiert die notwendigen Datentypen, Dokument-Metadaten (Header), die Möglichkeiten der Textstrukturierung, grundlegende Vorgaben für die Anwendung von Terminologien, einige allgemein genutzte Inhaltsstrukturen (Sections) sowie Codebeispiele und praktische Implementierungshilfen. Der in ELGA vorgesehene Ablauf des Datenaustausches wird im Kapitel "Anwendungsfälle" umrissen.
Für konkrete Dokumente wie etwa Entlassungsbriefe, Laborbefunde oder andere Dokumentenklassen müssen die inhaltlichen Vorgaben in so genannten "speziellen Implementierungsleitfäden" beschrieben werden. Diese speziellen Implementierungsleitfäden sind nicht Teil dieser Spezifikation. Diese Spezifikation definiert auch nicht den Transport von elektronischen Dokumenten und beschreibt weder Sicherheitsaspekte wie Digitale Signaturen, Verschlüsselung etc. noch Vorgaben zum Datenschutz.
Der primäre Leserkreis dieses Dokuments sind Software-Entwickler und Berater, die allgemein mit Implementierungen und Integrationen im Gesundheitswesen betraut sind.
Diese Version des Leitfadens stellt eine grundlegend überarbeitete Erweiterung des Allgemeinen Implementierungsleitfadens dar, die zusätzliche Möglichkeiten bietet und neben ELGA e-Befunden auch andere e-Health-Dokumente unterstützt. Die Version 3.0.0 ist eine "Hauptversion", die gegenüber der Vorversion vollständig kompatibel ist, aber neue Verpflichtungen einführt; mit Version 3.1.0 wurden Korrekturen nachgereicht.
Übersichtstabellen für Header und Body-Strukturen
- Übersichtstabelle der CDA Strukturen des Headers (administrative Daten)
- Übersichtstabelle der allgemeinen Sektionen des CDA Bodys (medizinische Inhalte)
Die Seite Allgemeiner Implementierungsleitfaden (Version 3) Änderungen enthält eine Beschreibung der Änderungen gegenüber der letzten Version 2.06.2. Auf der Diskussionsseite werden die Fehler und Änderungswünsche an dieser Version dokumentiert.
2 Informationen über dieses Dokument[Bearbeiten]
2.1 Impressum[Bearbeiten]
Medieneigentümer, Herausgeber, Hersteller, Verleger:
ELGA GmbH, Treustraße 35-43, Wien, Österreich. Telefon: +43.1.2127050
Internet: www.elga.gv.at
Email: cda@elga.gv.at
Geschäftsführer: DI Dr. Günter Rauchegger, DI(FH) Dr. Franz Leisch
Redaktion, Projektleitung, Koordination:
Mag.Dr. Stefan Sabutsch, stefan.sabutsch@elga.gv.at
Abbildungen: © ELGA GmbH
Nutzung: Das Dokument enthält geistiges Eigentum der Health Level Seven® Int. und HL7® Austria, Franckstrasse 41/5/14, 8010 Graz; www.hl7.at.
Die Nutzung ist ohne Lizenz- und Nutzungsgebühren zum Zweck der Erstellung medizinischer Dokumente ausdrücklich erlaubt. Andere Arten der Nutzung und auch auszugsweise Wiedergabe bedürfen der Genehmigung des Medieneigentümers.
Download unter www.gesundheit.gv.at und www.elga.gv.at/cda
2.2 Haftungsausschluss[Bearbeiten]
Die Arbeiten für den vorliegenden Leitfaden wurden von den Autoren gemäß dem Stand der Technik und mit größtmöglicher Sorgfalt erbracht und über ein öffentliches Kommentierungsverfahren kontrolliert. Die Nutzung des vorliegenden Leitfadens erfolgt in ausschließlicher Verantwortung der Anwender. Aus der Verwendung des vorliegenden Leitfadens können keinerlei Rechtsansprüche gegen die Autoren, Herausgeber oder Mitwirkenden erhoben und/oder abgeleitet werden. Ein allfälliger Widerspruch zum geltenden Recht ist jedenfalls nicht beabsichtigt und von den Erstellern des Dokumentes nicht gewünscht.
2.3 Sprachliche Gleichbehandlung[Bearbeiten]
Soweit im Text Bezeichnungen nur im generischen Maskulinum angeführt sind, beziehen sie sich auf Männer, Frauen und andere Geschlechtsidentitäten in gleicher Weise. Unter dem Begriff "Patient" werden sowohl Bürger, Kunden und Klienten zusammengefasst, welche an einem Behandlungs- oder Pflegeprozess teilnehmen als auch gesunde Bürger, die derzeit nicht an einem solchen teilnehmen. Es wird ebenso darauf hingewiesen, dass umgekehrt der Begriff Bürger auch Patienten, Kunden und Klienten mit einbezieht.
2.4 Lizenzinformationen[Bearbeiten]
Die von HL7 Austria erarbeiteten Standards und die Bearbeitungen der Standards von HL7 International stellen Werke im Sinne des österreichischen Urheberrechtsgesetzes dar und unterliegen daher urheberrechtlichem Schutz.
HL7 Austria genehmigt die Verwendung dieser Standards für die Zwecke der Erstellung, des Verkaufs und des Betriebs von Computerprogrammen, sofern nicht anders angegeben oder sich die Standards auf andere urheberrechtlich oder lizenzrechtlich geschützte Werke beziehen.
Die vollständige oder teilweise Veröffentlichung der Standards (zum Beispiel in Spezifikationen, Publikationen oder Schulungsunterlagen) ist nur mit einer ausdrücklichen Genehmigung der HL7 Austria gestattet. Mitglieder von HL7 Austria sind berechtigt, die Standards vollständig oder in Auszügen ausschließlich organisationsintern zu publizieren, zu vervielfältigen oder zu verteilen. Die Veröffentlichung eigener Anpassungen der HL7-Spezifikationen (im Sinne von Lokalisierungen) oder eigener Leitfäden erfordert eine formale Vereinbarung mit der HL7 Austria.
HL7® und CDA® sind die eingetragenen Marken von Health Level Seven International. Die vollständigen Lizenzinformationen finden sich unter https://hl7.at/nutzungsbedingungen-und-lizenzinformationen/. Die Lizenzbedingungen von HL7 International finden sich unter http://www.HL7.org/legal/ippolicy.cfm
2.4.1 Urheber- und Nutzungsrechte von anderen Quellen ("Third Party IP")[Bearbeiten]
Third Party Intellectual Property
Der Nutzer dieses Dokuments (bzw. der Lizenznehmer) stimmt zu und erkennt an, dass HL7 Austria nicht alle Rechte und Ansprüche in und an den Materialien besitzt und dass die Materialien geistiges Eigentum von Dritten enthalten und / oder darauf verweisen können ("Third Party Intellectual Property (IP)").
Die Anerkennung dieser Lizenzbestimmungen gewährt dem Lizenznehmer keine Rechte in Bezug auf Third Party IP. Der Lizenznehmer allein ist für die Identifizierung und den Erhalt von notwendigen Lizenzen oder Genehmigungen zur Nutzung von Third Party IP im Zusammenhang mit den Materialien oder anderweitig verantwortlich.
Jegliche Handlungen, Ansprüche oder Klagen eines Dritten, die sich aus einer Verletzung eines Third Party IP-Rechts durch den Lizenznehmer ergeben, bleiben die Haftung des Lizenznehmers.
2.4.2 SNOMED CT[Bearbeiten]
Dieser Leitfaden enthält Material, das durch SNOMED International urheberrechtlich geschützt ist. Jede Verwendung von SNOMED CT in Österreich erfordert eine aufrechte Affiliate Lizenz oder eine Sublizenz. Die entsprechende Lizenz ist kostenlos, vorausgesetzt die Verwendung findet nur in Österreich statt und erfüllt die Bedingungen des Affiliate License Agreements. Affiliate Lizenzen können über das Member Licensing and Distribution Service (MLDS) direkt beim jeweiligen NRC beantragt werden: MLDS für Österreich.
2.4.3 Weitere Terminologien[Bearbeiten]
Im Folgenden finden Sie eine nicht-exhaustive Liste von weiteren Terminologien, die eine solche separate Lizenz erfordern können:
| Terminologie | Eigentümer, Kontaktinformation |
|---|---|
| Logical Observation Identifiers Names & Codes (LOINC) <ref name="LOINC">Logical Observation Identifiers Names & Codes (LOINC) loinc.org</ref> | Regenstrief Institute, Inc. <ref name="regenstrief">Regenstrief Institute, Inc. www.regenstrief.org</ref> |
| Unified Code for Units of Measure (UCUM) <ref name="UCUM">Unified Code for Units of Measure (UCUM) www.unitsofmeasure.org</ref> | Regenstrief Institute, Inc. <ref name="regenstrief" /> |
| International Classification of Diseases (ICD) <ref name="ICD-10">WHO ICD-10 www.who.int/classifications/icd/en/</ref> | World Health Organization (WHO) <ref name="WHO">www.who.int</ref> |
| ICD-10 BM*G*<ref name="ICD-10-AT">Internationale statistische Klassifikation der Krankheiten und verwandter Gesundheitsprobleme 10. Revision – aktuelle Version bitte unter Gesundheitssystem - Krankenanstalten heraussuchen.</ref> | Für Gesundheit zuständiges Bundesministerium www.sozialministerium.at |
| Anatomical Therapeutic Chemical Classification System (ATC) <ref name"ATC">Anatomical Therapeutic Chemical Classification System (ATC) https://www.who.int/tools/atc-ddd-toolkit/atc-classification</ref> | World Health Organization (WHO)<ref name="WHO"/> |
| Pharmazentralnummer (PZN) | ARGE Pharma im Fachverband der chemischen Industrie Österreichs (FCIO) der Wirtschaftskammern Österreichs (WKO) <ref name="FCIO">ARGE Pharma im Fachverband der chemischen Industrie Österreichs (FCIO) argepharma.fcio.at</ref> |
| EDQM-Codes | Europäisches Direktorat für die Qualität von Arzneimitteln <ref name"EDQM">EDQM Council of Europe www.edqm.eu</ref> |
| Medical Device Communications (MDC) vom ISO/IEEE 11073 Standard | MDC wird als Substandard 10101 "Nomenclature" in "Health informatics - Medical / health device communication standards", kurz 11073, geführt und werden mit einem Copyright bei IEEE SA am österreichischen Termserver bereitgestellt. <ref name="11073nomenclature">Health informatics - Medical / health device communication standards ISO/IEEE 11073 Nomenclature Part 10101: Nomenclature</ref>, <ref name="11073nomenclatureamendment">Health informatics - Medical / health device communication standards ISO/IEEE 11073 Nomenclature Amendment 1 Part 10101: Nomenclature Amendment 1: Additional Definitions</ref> |
Die Terminologien werden am österreichischen Terminologieserver zur Verfügung gestellt.
2.5 Verwendete Grundlagen und Bezug zu anderen Standards[Bearbeiten]
Grundlage dieses Implementierungsleitfadens ist der internationale Standard "HL7 Clinical Document Architecture, Release 2.0" (CDA ©), für die das Copyright © von Health Level Seven International<ref name="HL7">Health Level Seven International www.hl7.org</ref> gilt. 2009 wurde die Release 2.0 als ISO-Standard ISO/HL7 27932:2009 publiziert<ref>ISO/HL7 27932:2009 Data Exchange Standards — HL7 Clinical Document Architecture, Release 2 [1]</ref>.
CDA definiert die Struktur und Semantik von "medizinischen Dokumenten" zum Austausch zwischen Gesundheitsdiensteanbietern und Patienten. Es enthält alle Metadaten zur Weiterverarbeitung und einen lesbaren textuellen Inhalt und kann diese Informationen auch maschinenlesbar tragen. Das Datenmodell von CDA und seine Abbildung in XML<ref>World Wide Web Consortium. Extensible Markup Language, 1.0, 5th Edition. [2]</ref> folgen dem Basisstandard HL7 Version 3<ref>HL7 Version 3 Product Suite [3]</ref> mit seinem Referenz-Informationsmodell (RIM). Dieser Leitfaden verwendet das HL7-Template-Austauschformat zur Definition der "Bausteine" (Templates) und ART-DECOR® <ref>ART-DECOR® www.art-decor.org</ref> als Spezifikationsplattform.
- HL7 Clinical Document Architecture (CDA) <ref name="CDA"> HL7 Clinical Document Architecture (CDA) [4]</ref>
- HL7 Referenz-Informationsmodell (RIM)<ref name="RIM">HL7 Version 3: Reference Information Model (RIM) [5]</ref>
- HL7 V3 Datentypen <ref name="HL7 Version 3 Standard: Data Types">HL7 Version 3 Standard: Data Types – Abstract Specification, Release 2[6]</ref>
- HL7 Template-Austauschformat Specification and Use of Reusable Information Constraint Templates, Release 1<ref name="Templates Specification"> HL7 Templates Standard: Specification and Use of Reusable Information Constraint Templates, Release 1 [7] </ref>
Die HL7 Standards können über die HL7 Anwendergruppe Österreich (HL7 Austria)<ref>HL7 Austria www.hl7.at</ref>, die offizielle Vertretung von Health Level Seven International in Österreich bezogen werden (www.HL7.at). Alle auf nationale Verhältnisse angepassten und veröffentlichten HL7-Spezifikationen können ohne Lizenz- und Nutzungsgebühren in jeder Art von Anwendungssoftware verwendet werden. Die erste Version dieses Implementierungsleitfadens wurde bereits 2009 erstellt und 2012 als gültiger Standard publiziert. Der Leitfaden wurde wesentlich durch den von HL7 Deutschland erstellten Leitfaden "VHitG-Arztbrief 2006"<ref>VHitG (jetzt bvitg): "Arztbrief auf Basis der HL7 Clinical Document Architecture Release 2.0 für das deutsche Gesundheitswesen" Version 1.5 (2006) PDF</ref> inspiriert, von dem einige Ausführungen direkt übernommen wurden. Seither wurde dieser Leitfaden kontinuierlich weiterentwickelt und verbessert. Die aktuelle Version führt einige Neuerungen ein, die aus dem CDA Leitfaden HL7 International Patient Summary<ref name="IPS">HL7 International Patient Summary, Standard for Trial Use 1.86 (2017) Project Wiki: [8]</ref> übernommen wurden.
2.6 Verbindlichkeit[Bearbeiten]
Die Verbindlichkeit und die Umsetzungsfrist dieses Leitfadens sind im Gesundheitstelematikgesetz 2012, BGBl.I Nr.111/2012 sowie in den darauf fußenden ELGA-Verordnungen geregelt.
Der Leitfaden in seiner jeweils aktuell gültigen Fassung sowie die aktualisierten Terminologien sind vom zuständigen Minister auf www.gesundheit.gv.at zu veröffentlichen. Der Zeitplan zur Bereitstellung der Datenaustauschformate wird durch das Gesundheitstelematikgesetz 2012 und darauf basierenden Durchführungsverordnungen durch den zuständigen Bundesminister vorgegeben. Hauptversionen, also Aktualisierungen des Implementierungsleitfadens, welche zusätzliche verpflichtende Konformitätskriterien enthalten ("Mandatory" [M], "Required" [R] und "Fixed" [F]), sind mit ihren Fristen zur Bereitstellung per Verordnung kundzumachen. Andere Aktualisierungen (Nebenversionen) dürfen auch ohne Änderung dieser Verordnung unter www.gesundheit.gv.at veröffentlicht werden.
Die Anwendung dieses Implementierungsleitfadens hat im Einklang mit österreichischem und europäischem Recht, insbesondere mit den relevanten Materiengesetzen (z.B. Ärztegesetz 1998, Apothekenbetriebsordnung 2005, Krankenanstalten- und Kuranstaltengesetz, Gesundheits- und Krankenpflegegesetz, Rezeptpflichtgesetz, Datenschutzgesetz, Gesundheitstelematikgesetz 2012, DSGVO) zu erfolgen. Technische Möglichkeiten können gesetzliche Bestimmungen selbstverständlich nicht verändern, vielmehr sind die technischen Möglichkeiten im Einklang mit den Gesetzen zu nutzen.
Die Einhaltung der gesetzlichen Bestimmungen liegt im Verantwortungsbereich der Ersteller der CDA-Dokumente.
2.7 Wichtige unterstützende Materialien[Bearbeiten]
Auf der Website Allgemeiner Implementierungsleitfaden Guide werden unter anderem folgende Materialien zur Verfügung gestellt:
- die PDF-Version dieses Leitfadens
- Beispieldokumente
- ein erweitertes CDA-Schema
- Schematron-Prüfregeln
Die im Weiteren angeführten Templatespezifikationen wurden im Art-Decor Projektrepository ATCDABBR erstellt und können dort eingesehen werden. Eine Anleitung zum Verständnis der Art-Decor-Notation finden Sie im Artikel Art-Decor-Tabellen verstehen.
Gemeinsam mit diesem Leitfaden werden auf der Website der ELGA GmbH (www.elga.gv.at/CDA) weitere Dateien und Dokumente zur Unterstützung bereitgestellt:
- Beispieldokumente
- Referenz-Stylesheet (Tool zur Darstellung im Browser - Konvertierung in HTML)
- CDA2PDF Suite (Tool zur Erzeugung einer PDF-Datei zur Ausgabe am Drucker)
- Schematron-Dateien für die Prüfung der Konformität ("Richtigkeit") von CDA Dateien
- Vorgaben zur Registrierung von CDA-Dokumenten (Leitfaden für XDS-Metadaten)
- Hinweise für die zu verwendenden Terminologien
- Leitfaden zur richtigen Verwendung von Terminologien
2.8 Bedienungshinweise[Bearbeiten]
2.8.1 Farbliche Hervorhebungen und Hinweise[Bearbeiten]
2.8.1.1 Themenbezogene Hinweise zur besonderen Beachtung:[Bearbeiten]
Hinweis:
Es dürfen keine Elemente oder Attribute verwendet werden, die nicht vom allgemeinen oder einem speziellen ELGA-Implementierungsleitfaden definiert wurden
2.8.1.2 Hinweis auf anderen Implementierungsleitfaden:[Bearbeiten]
Verweis
Verweis auf den Allgemeinen Leitfaden: …
2.8.1.3 Themenbezogenes CDA Beispiel-Fragment im XML Format:[Bearbeiten]
<BEISPIEL> <languageCode code="de-AT" />
2.8.1.4 Hinweis zum XDS-Mapping[Bearbeiten]
Elemente, die in die so genannten "XDS-Metadaten (IHE XDSDocumentEntry) von ELGA "<ref name="XDS-Metadaten">Registrierung von CDA Dokumenten für ELGA mit IHE Cross-Enterprise Document Sharing: XDS Metadaten (XDSDocumentEntry) ILF:XDS_Metadaten_2020 XDS-Metadaten</ref> übernommen werden sollen, werden mit diesem Text gekennzeichnet:
↔ Hinweis zum XDS-Mapping
Eine Übersichtstabelle findet sich in den ELGA-Spezifischen Anwendungsfällen: Schreiben und Einbringen von Dokumenten
[Bearbeiten]
Nutzen Sie die bereitgestellten Links im Dokument (z.B. im Inhaltsverzeichnis), um direkt in der PDF-Version dieses Dokuments zu navigieren. Folgende Tastenkombinationen können Ihnen die Nutzung des Leitfadens erleichtern:
- Rücksprung: Alt + Pfeil links und Retour: Alt + Pfeil rechts
- Seitenweise blättern: "Bild" Tasten
- Scrollen: Pfeil nach oben bzw. unten
- Zoomen: Strg + Mouserad drehen
- Suchen im Dokument: Strg + F
3 Einleitung[Bearbeiten]
3.1 Ausgangslage und Motivation[Bearbeiten]
In der medizinischen Welt ist es üblich, klinische Sachverhalte und Beobachtungen mit ihrem Kontext in Dokumente zusammenzufassen. Der Kontext – z.B. das Ergebnis einer Laboruntersuchung nach einer speziellen Medikamentenbehandlung – wird durch das Dokument etabliert und muss dauerhaft erhalten bleiben, da er wichtige medizinische Zusammenhänge zwischen Einzelinformationen darstellt. Gleichzeitig muss der medizinische Inhalt leicht verfügbar sein und ohne große technische Barrieren sichtbar gemacht werden können. Dies ist unabdingbar für die Akzeptanz von und das Vertrauen in Technologie bei den Endbenutzern, den GDA (Gesundheitsdiensteanbieter). Was mit der Papierwelt bis zu einem gewissen Grade erreicht wurde, muss auch für die elektronische Entsprechung des Papierdokuments gelten.
Die Elektronische Gesundheitsakte (ELGA) ermöglicht den durch das Gesundheitstelematikgesetz 2012 berechtigten Personen, entsprechend ihren Rollen, den Zugriff auf relevante Gesundheitsdaten der ELGA-Teilnehmer. Diese medizinischen Dokumente (e-Befunde) werden in vielen unterschiedlichen Informationssystemen der verschiedenen ELGA-Gesundheitsdiensteanbieter erstellt und durch ELGA in bedarfsgerecht elektronisch aufbereiteter Form online zur Verfügung gestellt. Diese Dokumente sollen allerdings nicht nur von Benutzern gelesen, sondern auch wieder in die IT-Systeme integriert und dort weiterverwendet werden können ("Semantische Interoperabilität"). Beispielsweise können für den Arzt aus ELGA-Dokumenten automatisch Warnungen, Erinnerungen und Zusammenfassungen generiert und weitere Informationen berechnet sowie kontextbezogen angezeigt werden.
3.2 Zweck des Dokuments[Bearbeiten]
Das Ziel dieses Dokuments ist die Beschreibung der Struktur von medizinischen Dokumenten der Elektronischen Gesundheitsakte ELGA (entsprechend GTelG 2012, BGBl. I Nr. 111/2012 [9]). Insbesondere behandelt das Dokument alle Dokumentenklassen-übergreifend gültigen Strukturen. Um dieses Ziel zu erreichen, wird der CDA-Standard für die Verwendung in ELGA im Detail ausspezifiziert. Vorgaben für einheitliche Dokumentation und Codierung der Information werden festgelegt und in implementierbaren Leitfäden veröffentlicht.
Der vorliegende "Allgemeine Implementierungsleitfaden für CDA-Dokumente" stellt eine grundlegende Implementierungsvorschrift für alle CDA-Dokumente im österreichischen Gesundheitswesen dar. Dies umfasst ELGA e-Befunde, also jene Dokumente, die für Patienten und deren Behandler über die ELGA Infrastruktur abrufbar sind (z.B. ELGA Portal), als auch jene e-Health Dokumente, die zwar die ELGA Infrastruktur (wie Berechtigungssystem, Zentraler Patienten-Index, Gesundheitsdiensteanbieter-Index, Protokollierung, ...) nutzen, für die aber andere gesetzliche Grundlagen gelten. Dieser Vorschrift müssen daher alle über ELGA vermittelten CDA-Dokumente folgen. Andere CDA-Dokumente im österreichischen Gesundheitswesen sollen ebenfalls dieser Vorschrift folgen, der Leitfaden wurde daher entsprechend offen ausgelegt.
Darüber hinaus MUSS auf Basis des vorliegenden Allgemeinen Implementierungsleitfadens ein spezieller Implementierungsleitfaden definiert sein, der Inhalt und Struktur der medizinisch relevanten Inhalte definiert (z.B. Entlassungsbrief, Laborbefund, etc., siehe Aufbau eines CDA-Dokuments).
3.3 Zielgruppe[Bearbeiten]
Anwender dieses Dokuments sind Softwareentwickler und Berater, die allgemein mit Implementierungen und Integrationen im Umfeld der ELGA, insbesondere der ELGA-Gesundheitsdaten, betraut sind. Eine weitere Zielgruppe sind alle an der Erstellung von CDA-Dokumenten beteiligten Personen, einschließlich der Endbenutzer der medizinischen Softwaresysteme und der Angehörigen von Gesundheitsberufen.
4 Leitfadenerstellungs- und Harmonisierungsprozess[Bearbeiten]
Für die Ausgestaltung der Inhalte von "CDA Implementierungsleitfäden" ist eine breite Beteiligung der Stakeholder wesentlich, um die praktische Nutzbarkeit und die Akzeptanz durch die ELGA-Benutzer sicherzustellen. Für diese interdisziplinären Expertengruppen stehen nicht die technischen, sondern vor allem medizinisch-inhaltliche Aspekte im Vordergrund. Die technischen Inhalte werden großteils von den Redaktionsteams beigetragen.
Ein wesentlicher Schritt auf dem Weg zur Interoperabilität der IT-Systeme im Gesundheitswesen ist die Einigung auf Vorgaben für einheitliche Dokumentation und Codierung der Information. Diese durch die Arbeitsgruppen erreichte "Harmonisierung" etabliert neue nationale Qualitätsstandards der medizinischen Dokumentation. Die Leitfäden werden über ein reguläres Standardisierungsverfahren ("Ballot") durch die HL7 Anwendergruppe Österreich (HL7 Austria) zu einem nationalen HL7 Standard.
4.1 Vorgehensmodell[Bearbeiten]
4.1.1 Harmonisierung von CDA Implementierungsleitfäden für ELGA[Bearbeiten]
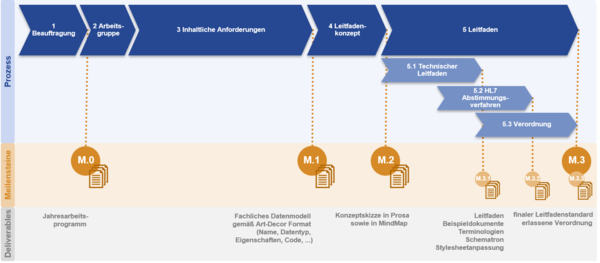
Der Initialisierungsschritt für neue CDA Implementierungsleitfäden wird im ELGA-Koordinierungsausschuss auf Basis eines Vorschlages der ELGA GmbH gesetzt. Die Planung umfasst die Einladung der Experten und die Beauftragung eines Redaktionsteams zur Erstellung des Leitfadens durch die ELGA GmbH.
<ref group="Abbildung">Standardprozess zur Erstellung eines neuen ELGA CDA Implementierungsleitfadens</ref>Für die Erarbeitung der Vorgaben einer Dokumentenklasse ist jeweils eine Arbeitsgruppe verantwortlich. Jede Arbeitsgruppe wird von einem Redaktionsteam moderiert, das aus einem AG-Leiter und weiteren Redaktionsteammitgliedern besteht. Die zentrale Koordination der Arbeitsgruppen erfolgt durch die ELGA GmbH. Die Mitglieder der Arbeitsgruppen werden von den maßgeblichen Stakeholdern des österreichischen Gesundheitswesens gestellt, die an der Erstellung und Verwendung der jeweiligen Dokumentenklassen partizipieren. Folgende Stakeholder-Gruppen werden speziell zur Teilnahme motiviert:
- Vertreter der Ärzteschaft (Ärztekammer, Fachgesellschaften)
- Krankenhaus-Trägergesellschaften
- Pflegeorganisationen
- Befundprovider
- Hersteller von medizinischen Dokumentationssystemen (z.B. Krankenhausinformationssystemen, Arztpraxissoftware)
- Bürgerinitiativen
- Standardisierungsorganisationen
Die Arbeitsgruppen werden von der CDA-Koordinationsstelle der ELGA GmbH einberufen (Semantic Competence Center). Sie koordiniert die Sitzungen und übernimmt die Kommunikationsaufgaben. Jede Arbeitsgruppe wird durch ein Redaktionsteam unterstützt, welches folgende Tätigkeiten durchzuführen hat:
- Erheben, Auswerten, Analysieren, Zusammenfassen und Aufarbeiten der eingegangenen Anforderungen
- Fachliche Vorbereitung der Arbeitsgruppensitzungen
- Erstellung der Leitfadendokumente und ergänzender Materialien (z.B. Beispiel-CDA-Dateien, Schematron-Prüfregeln)
Von der Arbeitsgruppe und dem Redaktionsteam wird eine erste Version eines CDA Implementierungsleitfadens vorgelegt. Für eine verpflichtende Anwendung eines Leitfadens ist ein normatives Abstimmungsverfahren ("Ballot") der Leitfäden durch HL7 Austria durchzuführen. Optional kann für eine Überprüfung der Implementierbarkeit vor dem normativen Ballot ein "STU-Ballot" (Standard for Trial Use Ballot) durchgeführt werden, mit dem dann eine Testphase durchgeführt werden kann.
Über die hier geschilderten "internen" Abstimmungsarbeiten hinaus wird eine Kooperation mit den betroffenen Standardisierungsorganisationen angestrebt, etwa mit dem Österreichischen Normungsinstitut, IHE Austria, DICOM Austria und auch mit weiteren nationalen und internationalen Normengremien.
4.1.2 HL7 Abstimmungsverfahren[Bearbeiten]
Für die Annahme von neuen nationalen HL7 Standards und Richtlinien existiert eine formelle Prozedur, das so genannte Abstimmungsverfahren oder "Ballot". Der Leitfaden wird dafür einem breiten Teilnehmerkreis zur Kommentierung vorgelegt. Die Kommentare werden gesammelt und bearbeitet, wobei negative Kommentare im Einvernehmen zwischen dem Autor des Leitfadens und dem Kommentierenden aufgelöst werden. Eine ausreichende Anzahl an stimmberechtigten Teilnehmern muss der Freigabe des Dokuments zustimmen. Eine genaue Beschreibung des Abstimmungsverfahrens ist auf der Website von HL7 Austria publiziert<ref>HL7 Austria Abstimmungsverfahren ("Ballots"): https://hl7.at/technische-komitees/ballots/</ref>.
4.2 Revision der Leitfäden[Bearbeiten]
Neue und geänderte Anforderungen sowie Verbesserungen können neue Versionen der bestehenden Spezifikationen notwendig machen.
Der CDA-Koordinator evaluiert in regelmäßigen Abständen, ob und welche Änderungen (etwa durch neue medizinische oder gesetzliche Anforderungen) notwendig sind. Aufgrund des Berichtes des CDA-Koordinators empfiehlt die ELGA GmbH die Erstellung von Revisionsversionen der bestehenden Leitfäden. Die geplanten Änderungen sollen mit den maßgeblichen Stakeholdern abgestimmt werden.
Neue Versionen, die "verpflichtende Elemente" (Sections oder Entries) neu einführen oder entfernen, sind "Hauptversionen", die jedenfalls über eine Durchführungsverordnung verbindlich gemacht und veröffentlicht werden. Andere Versionen sind "Nebenversionen". Alle verbindlichen Versionen sind auf http://www.gesundheit.gv.at zu veröffentlichen.
4.3 Autoren und Mitwirkende[Bearbeiten]
Dieser Implementierungsleitfaden entstand durch die Harmonisierungsarbeit der "Arbeitsgruppe" bestehend aus nachfolgend genannten Personen:
4.3.1 Autoren[Bearbeiten]
Das Redaktionsteam bestand aus folgenden Personen:
| Name | Organisation | Rolle |
|---|---|---|
| Mag. Dr. Stefan Sabutsch | ELGA GmbH, HL7 Austria | Autor, Herausgeber |
| DI Andrea Klostermann | ELGA GmbH | Autor |
| DI Oliver Kuttin | ELGA GmbH | Autor |
| DI Nikola Tanjga | ELGA GmbH | Autor |
| DI Jürgen Brandstätter | CodeWerk Software Services and Development GmbH | Autor und Moderator der Arbeitsgruppe 2008-2012 |
Unter Mitwirkung von: Stephan Rainer-Sablatnig (ELGA GmbH), Carina Seerainer, MSc. (ELGA GmbH), Nina Sjencic, B.A. (ELGA GmbH)
4.3.2 Mitwirkende[Bearbeiten]
Teilnehmer der Arbeitsgruppe Allgemeiner Implementierungsleitfaden (Version 3)1: Annette Altenpohl (Austrian Standards), Loinger Johanna (AUVA), Florian Schlechtleitner (AUVA), Herbert Matzenberger (CGM), Reinhard Egelkraut (CGM), Victor Emanuel Grogger (KAGES), Hannes Steinberger (KAGES), Jacqueline Teufl (medilab), Roman Horvath (MedIT), Manuel Ratzinger (NÖLKH), Michael Nöhammer (ÖÄK), Elke Pessl (OÖ Gesundheitsholding), Alexander Kollmann (SALK), Alexander Hörtnagl (Siemens AG), Sarah Kardinar (SVC), Matthias Frohner (Technikum Wien), Christian Stark (Tiroler Kliniken), Stefan Rausch-Schott (Vinzenz Gruppe), Hans Jürgen Schiller (Vorarlberger LKH), Franz Weissinger (Wien Digital), Maria Abzieher (Wien Digital)
Teilnehmer der Arbeitsgruppe der Vorgänger-Version 2.06.21: Milan Kornfeind (Österreichische Ärztekammer), Robert Hawliczek (Österreichische Ärztekammer), Jürgen Schwaiger (Österreichische Ärztekammer), Gerhard Holler (Österreichische Ärztekammer), Ludwig Gruber (Ärztekammer Tirol) Christian Husek (Initiative-ELGA), Susanna Michalek (Initiative-ELGA), Michael Hubich (Barmherzige Schwestern Linz), Tilman Königswieser (Oberösterreichische Gesundheits- u. Spitals AG), Josef Hamedinger (Oberösterreichische Gesundheits- u. Spitals AG), Ingrid Wimmer (Oberösterreichische Gesundheits- u. Spitals AG), Hubert Leitner (Steiermärkische Krankenanstalten-ges. m.b.H.), Walter Schwab-Ganster (Steiermärkische Krankenanstalten-ges. m.b.H.), Birgit Fürst (Steiermärkische Krankenanstalten-ges. m.b.H.), Monika Hoffberger (Steiermärkische Krankenanstalten-ges. m.b.H.), Daniela Sturm (Steiermärkische Krankenanstalten-ges. m.b.H.), Brigitte Walzl (Steiermärkische Krankenanstalten-ges. m.b.H.),Konrad Hölzl (Wiener Krankenanstaltenverbund), Reinhard Eberl (Salzburger Landeskliniken), Stefan Rausch-Schott (Vinzenz Gruppe Krankenhausbeteiligungs- und Management GmbH), Benedikt Aichinger (e-Care Projekt), Eva Friedler (Projekt "PatientInnenorientierte integrierte Krankenbetreuung"), Vera Em (FSW), Robert Em (WISO), Wolfgang Pfleger (FSW), Allg. Unfallversicherungsanstalt (Sozialversicherung), Gudrun Seiwald, Hubert Fankhauser (Sozialversicherung), Michael Szivak (Sozialversicherung), Barbara Kaller (Hauptverband der österreichischen Sozialversicherungsträger), Martin Asenbaum (Sozialversicherungs-Chipkarten Betriebs- und Errichtungsgesellschaft), Eduard Schebesta, Christoph Unfried (Health Communication Service GmbH), Jochen Peter Gallob (shm sana health management GmbH), Reinhard Egelkraut (Systema Human Information Systems GmbH), Peter Uher (Telekom Austria), Arnold Lengauer (Telekom Austria), Karl Holzer (T-Systems Austria GesmbH), Christian Ametz (x-tention), Matthias Frohner (Fachhochschule Technikum Wien), Ferenc Gerbovics (Fachhochschule Technikum Wien), Babette Dörr (Austrian Standards Institute - Österreichisches Normungsinstitut, Experte der Arbeitsgruppe 250.03 "Qualitätsmanagement in der Pflege"), Natalie Lottersberger (Austrian Standards Institute - Österreichisches Normungsinstitut, Experte der Arbeitsgruppe 250.03 "Qualitätsmanagement in der Pflege"), Andrea Klostermann (ELGA GmbH), Carina Seerainer (ELGA GmbH), Oliver Kuttin (ELGA GmbH), Stefan Sauermann (Fachhochschule Technikum Wien), Alexander Mense (Fachhochschule Technikum Wien), Martin Weigl (AIMC), Andreas Lindner (Lindner TAC)
Patronanz, Akkordierung, Ergänzungen, Zustimmung (Version 2.06.2)1: Clemens Auer (Bundesministerium für Gesundheit), Susanne Herbek (ELGA GmbH), Hubert Eisl (ELGA GmbH), Martin Hurch (ELGA GmbH), Oliver Kuttin (ELGA GmbH), Carina Seerainer (ELGA GmbH), Günther Wawrowsky (Österreichische Ärztekammer), Reinhold Renner (Österreichische Ärztekammer), Johannes Bretbacher (OÖ Gesundheits- und Spitals AG), Christian Gierlinger (Vinzenz Gruppe Krankenhausbeteiligungs- und Management GmbH), Jürgen Engelbrecht (Steiermärkische Krankenanstalten GmbH), Alexander Schanner (NÖ Landesklinikenholding), Wolfgang Amenitsch (NÖ Landesklinikenholding), Thomas Pökl (NÖ Landesklinikenholding), Eva Friessenbichler (NÖ Landesheime), Roland Nefischer (NÖ Landesheime), Thomas Schubert (Projekt NÖ Heim-Informationstechnologie), Wolfgang Hiessl (Oberösterreichischer Gesundheitsfonds), Evelyn Müller (Salzburger Landeskliniken), Wolfgang Dorda (Medizinische Universität Wien), Wolfgang Dufek (Wiener Gebietskrankenkasse), Karl Blauensteiner (Wiener Gebietskrankenkasse), Gerhard Stimac (Innomed GmbH), Herbert Thomas (Health Communication Service Gmbh), Johannes Rössler (Tieto IT Services), Thomas Hrdinka (Bundesfachgruppe Informationstechnologie der Bundeskammer der Architekten und Ingenieurkonsulenten)
1 Personen sind ohne Titel angegeben
5 Technischer Hintergrund[Bearbeiten]
5.1 Grundlagen zu HL7[Bearbeiten]
HL7 bezeichnet eine Gruppe von Standards für den Austausch von Daten zwischen Computersystemen im Gesundheitswesen. HL7 wird als Kommunikationsprotokoll vornehmlich zum Datenaustausch zwischen Abteilungssystemen in Krankenhäusern eingesetzt.
Die ursprünglich in den USA von der Organisation "Health Level Seven International" (HL7) (http://www.hl7.org) entwickelten Spezifikationen sind durch die Weiterentwicklung internationaler Benutzergruppen zu einem internationalen Standard geworden, der in über 55 Ländern eingesetzt wird.
Die HL7 Standards in Version 3 sind auf die Kommunikationsbedürfnisse des gesamten Gesundheitswesens abgestimmt. HL7 V3 bietet eine konzeptuelle Grundlage in einem gemeinsamen, umfassenden "Reference Information Model" (RIM) für alle Teile von HL7 V3.
Dieses RIM ist ANSI- und ISO-Standard (ISO/HL7 21731:2006) und bietet:
- ein festes semantisches Fundament
- ausgewählte standardisierte Terminologien, die semantische Interoperabilität ermöglichen
- die Trennung von Inhalten und Syntax
HL7 Version 3 basiert auf XML und wird für die Übermittlung von Nachrichten genutzt. HL7 stellt außerdem einen Standard zur Strukturierung des Inhalts und zum Austausch medizinischer Dokumente, die so genannte "Clinical Document Architecture" (CDA), zur Verfügung, welcher in folgendem Unterkapitel erläutert wird.
5.2 CDA Standard[Bearbeiten]
Die "Clinical Document Architecture" (CDA) ist ein Standard für den Austausch und die Speicherung von klinischer Dokumentation, wie zum Beispiel Entlassungsbriefe, Überweisungen, Behandlungsdokumentation oder OP-Berichte. Dabei steht der Informationsaustausch im gesamten Gesundheitswesen im Vordergrund (also nicht beschränkt auf Krankenhäuser).
CDA stellt einen XML-basierten Dokumenten-Markup Standard zur strukturierten klinischen Dokumentation zur Verfügung. Der CDA Standard definiert ein Informationsobjekt, das außerhalb einer Nachricht existieren kann und neben (strukturiertem) Text auch Bilder, Töne, Biosignale usw. enthalten bzw. referenzieren kann.
Als Grundlage für ELGA-Dokumente wurde der Standard HL7 Clinical Document Architecture, Release 2.0 ausgewählt. Der Standard kann über die HL7 Anwendergruppe Österreich (http://www.hl7.at) bezogen werden.
5.2.1 Eigenschaften von CDA-Dokumenten[Bearbeiten]
Der Standard CDA wird zum Austausch von medizinischen Dokumenten verwendet, die typischerweise folgende Eigenschaften aufweisen:
- Persistenz: Medizinische Dokumente sind durch Persistenz, also dauerhafte Existenz in den sendenden oder empfangenden Systemen gekennzeichnet, wo sie für einen bestimmten Zeitraum in einem unveränderten Zustand bleiben. Dieser Zeitraum wird durch lokale Regelungen definiert.
- Verwaltung (engl. "stewardship"): Für die Verwaltung des Dokuments ist eine bestimmte Organisation verantwortlich (der "Custodian").
- Kontext: Medizinische Dokumente etablieren den Standard-Kontext für die in ihnen gespeicherten Inhalte (z.B. den "Entlassungsbrief").
- Authentisierung (engl. "potential für authentication"): Medizinische Dokumente werden authentisiert. Im medizinischen Alltag entspricht das der Signierung, Vidierung oder Validierung.
- Ganzheit (engl. "wholeness"): Die Authentisierung eines medizinischen Dokumentes bezieht sich auf das Dokument als Ganzes und nicht nur auf einzelne aus dem Kontext gelöste Teile.
- Lesbarkeit (engl. "human readability"): Medizinische Dokumente sind für Menschen lesbar.
5.2.2 Bedingungen[Bearbeiten]
Eine grundsätzliche Bedingung für CDA ist die Sicherstellung der Lesbarkeit für Menschen in einem "normalen" Webbrowser (mit der üblichen Basisfunktionalität zum Browsen im Internet).
Dafür gilt zudem:
- Es muss einen eindeutig festgelegten Weg für einen Empfänger geben, den authentisierten Inhalt sichtbar zu machen (Für ELGA wird ein "Referenz-Stylesheet" bereitgestellt, siehe Kapitel Darstellung von CDA Dokumenten mittels ELGA Referenzstylesheet und CDA2PDF).
- Es ist nicht zulässig, dass die Darstellung im Browser nur mithilfe eines bestimmten Stylesheets bewerkstelligt werden kann, das dann zusammen mit dem CDA-Dokument gesendet werden muss. Es muss auch möglich sein, den Inhalt mit einem beliebigen Stylesheet und marktüblichen Browsern darzustellen.
- Lesbarkeit bezieht sich auf den authentisierten Inhalt. Zusätzlich kann weitere Information im Dokument vorhanden sein ("CDA Level 3"), die auf Auswertbarkeit durch Anwendungssysteme abzielt, die aber nicht authentisiert oder lesbar dargestellt werden muss.
- Wenn strukturierter Inhalt vom narrativen Text abgeleitet ist, muss der Mechanismus beschrieben sein, wie dies bewerkstelligt wurde, z.B. durch den Autor, durch eine Person, die eine Codierung vorgenommen hat, durch automatisierte Verarbeitung der natürlichen Sprache, durch eine spezifische Software.
- Wenn narrativer Text von strukturierter Information abgeleitet ist, muss der Mechanismus beschrieben sein, wie dies bewerkstelligt wurde.
5.2.3 Aufbau eines CDA-Dokuments[Bearbeiten]
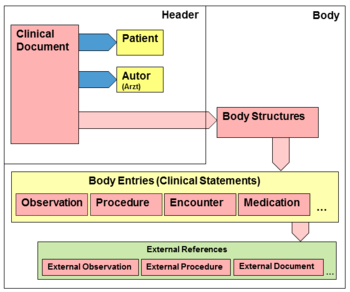
CDA-Dokumente sind XML-Dateien, welche aus einem Header mit Metadaten und einem Body mit dem eigentlichen Inhalt bestehen. Der CDA-Header (siehe Kapitel Header) trägt Informationen über das Dokument sowie deren Beteiligte, einschließlich dem Patienten. Der CDA-Body (siehe Kapitel Body) besteht wiederum aus Body Structures (Abschnitte und narrativer Text) und Body Entries (maschinenauswertbare Detailinformationen). An die Entries können externe Referenzen (External References) geknüpft sein.
Der folgende Überblick zeigt die Hauptkomponenten des CDA R2 Modells auf, in einer späteren Abbildung wird die Struktur in XML-artiger Darstellung gezeigt.
<ref group="Abbildung">CDA R2 Modell</ref>Je nach Leitfaden variieren Header und Body aus verschiedenen Templates. Templates sind definierte Vorlagen, die Strukturen von Dokumenten, Dokumentteilen oder Datenelementen vorgeben. In CDA bezeichnen solche Templates bestimmte Teilstrukturen.
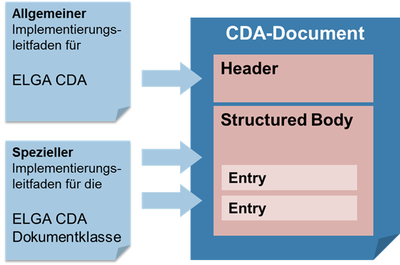
Die administrativen Daten im Dokument-Header und grundsätzliche Vorgaben für den medizinischen Inhalt werden vom vorliegenden Allgemeinen Implementierungsleitfaden definiert.
Der jeweilige Spezielle Implementierungsleitfaden enthält die Vorgaben für die medizinischen Inhalte und ergänzt gegebenenfalls die Header-Vorgaben.
<ref group="Abbildung">Zusammenspiel Implementierungsleitfäden</ref>Jeder spezielle Implementierungsleitfaden basiert somit auf diesem vorliegenden Allgemeinen Implementierungsleitfaden. Für folgende Dokumentenklassen wurden bereits spezielle ELGA CDA Implementierungsleitfäden definiert (Liste kann erweitert werden):
- Entlassungsbrief (Ärztlich), [OID Root 1.2.40.0.34.7.2]
- Entlassungsbrief (Pflege), [OID Root 1.2.40.0.34.7.3]
- Pflegesituationsbericht, [OID Root 1.2.40.0.34.7.12]
- Laborbefund, [OID Root 1.2.40.0.34.7.4]
- Befund bildgebende Diagnostik, [OID Root 1.2.40.0.34.7.5]
- e-Medikation, [OID Root 1.2.40.0.34.7.8]
Die Beschreibung des Zusammenhangs von ELGA CDA-Dokumenten und den zur Registrierung von CDA in ELGA notwendigen "XDS-Metadaten" finden Sie im Dokument
- ELGA XDS Metadaten (XDSDocumentEntry), [OID Root 1.2.40.0.34.7.6]
5.2.3.1 CDA Header[Bearbeiten]
Die Informationen im CDA Header unterstützen einen Austausch klinischer Dokumente über Institutionsgrenzen hinweg, hochstrukturiert und semantisch festgelegt.
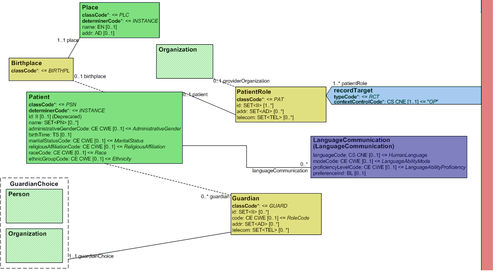
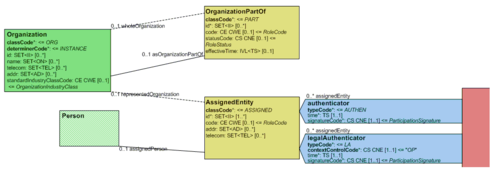
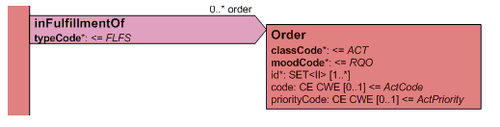
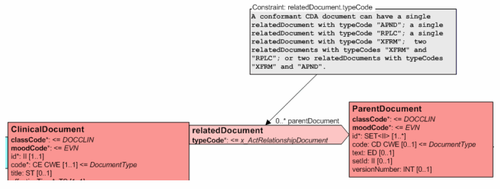
Der Header beinhaltet Informationen zum Patienten, zum Dokument selbst (eindeutige Identifikation, Art des Dokuments), zu den weiteren beteiligten Personen und Organisationen (wie Behandler und Autoren), zu den dokumentierten Episode (Zeitereignisse), sowie zu den Beziehungen zu anderen Dokumenten (zu Anforderungen und anderen Dokumenten).
Mit den Informationen des Headers werden Dokumentenmanagement-Systeme unterstützt - der Header stellt dafür entsprechende Mechanismen zur Verfügung. Damit werden die Zusammenführung und das Wiederfinden der Dokumente in ELGA oder in lokalen Patientenakten wesentlich erleichtert.
5.2.3.2 CDA Body[Bearbeiten]
Die eigentliche klinische Dokumentation wird im so genannten CDA Body festgehalten. Im Vordergrund steht hier "lesbarer" (narrativer) Text, der verpflichtender Bestandteil von CDA R2 Dokumenten ist und die Interoperabilität zwischen den menschlichen Kommunikationspartnern garantiert. Hier sind Möglichkeiten gegeben, diesen Text grob zu strukturieren und formatieren, wie man dies von den Möglichkeiten der Textverarbeitung her kennt. Zur Strukturierung stellt die Standardspezifikation eine Reihe von XML-Elementen zur Verfügung, die als Body Structures zusammengefasst werden können.
Der Body enthält ein oder mehrere Abschnitte (sections). Diese können auch ineinander geschachtelt sein, so wie Kapitel und Unterkapitel eines Buches, siehe Kapitel Sektionen. Zudem sind Strukturierungen im Sinne von Tabellen oder Listen möglich:
- Abschnitte < section>
- Paragrafen < paragraph>
- Kennzeichnung von bestimmten Inhalten < content>
- Überschriften < caption>
- Tabellen < table>
- Listen < list>
Sections enthalten immer einen narrativen Block und erfüllen damit eine der oben genannten Maximen von CDA: die Mensch-zu-Mensch-Interoperabilität, die Lesbarkeit der Informationen für den Menschen. Im narrativen Block wird der im Abschnitt eingebettete Text im Element text angegeben (section.text). Dabei kann mit oben genanntem content-Element bestimmter Inhalt gesondert gekennzeichnet werden. Zusammengefasst sind im Fließtextblock u.a. folgende Möglichkeiten der Struktur- und Formgebung des Textes gegeben:
- Zeilenumbrüche < br>
- Stilistische Angaben (unterstrichen, fett, kursiv etc.)
- Hoch- und Tiefstellung von Text
- Fußnoten, Symbole
- Revisionsmarken im Text mit <content revised=delete> und <content revised=insert> (siehe Verwendung von Revisionsmarken)
Eine ausführliche Beschreibung der Möglichkeiten der Strukturierung und Formatierung von Text ist im Kapitel Textstrukturierung und Formatierung angegeben.
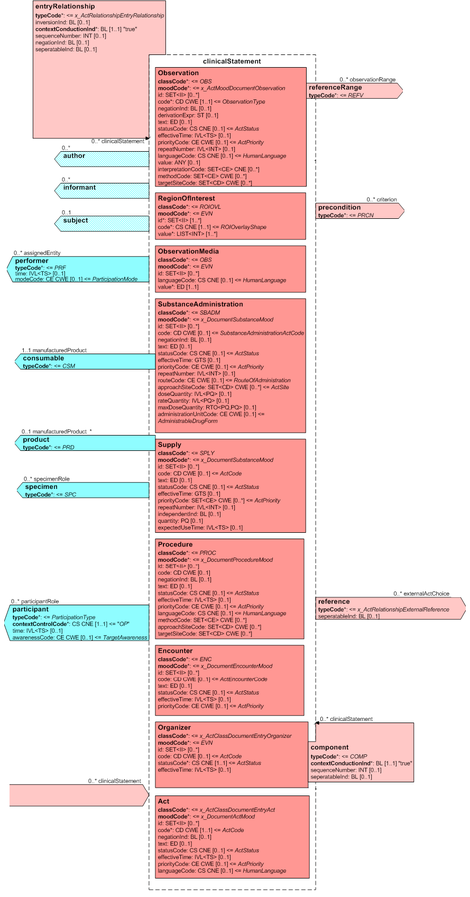
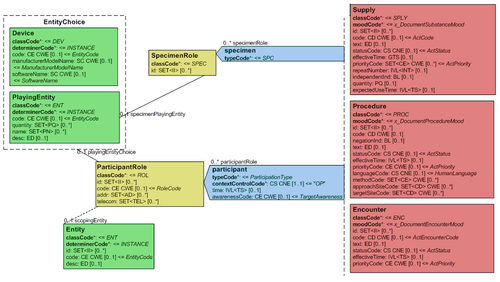
Mit den beschriebenen Body Strukturen können CDA Entries verbunden sein (Kapitel Strukturen in Level 3). Diese repräsentieren den "computerlesbaren Teil" innerhalb eines Dokumentenabschnitts. Body Entries sind im Prinzip eine Auswahl aus Klassen mitsamt Attributen aus dem HL7 Referenz-Informationsmodell (RIM). In der folgenden Abbildung ist ein Ausschnitt daraus gezeigt.
<ref group="Abbildung">R-MIM - CDA Body Entries</ref>Diese Auswahlliste von Entries wird auch als Clinical Statements bezeichnet und findet sich in gleicher oder ähnlicher Form auch in HL7-Version 3 Nachrichten zu Anforderungen und Befunden etc. wieder. Insgesamt sind in der Auswahl folgende Klassen verfügbar.
- observation, eine (codierte) Beobachtung, z.B. ein Befund oder eine Diagnose
- procedure, eine Prozedur, z.B. eine Operation, eine andere Behandlung, rein diagnostischer Eingriff
- encounter, Angaben zu früheren, jetzigen oder geplanten Patientenkontakten
- substanceAdministration, medikamenten-bezogene Angaben im Sinne von stattgefundenen (Medikamentenanamnese) oder geplanten Medikamentengaben
- supply, zur Verfügungstellung von Material oder Medikamentenverabreichungen
- organizer, zur Gruppierung von anderen CDA Entries (Batterien, Cluster)
- observationMedia, multimedialer Inhalt als Teil des Dokuments
- regionOfInterest, Kennzeichnung einer Hervorhebung eines Teilaspekts eines Bildes
Alle diese Entries können untereinander linear oder rekursiv hierarchisch verbunden sein. Es sind gleichstufige Beziehungen möglich (z.B. eine Liste von Beobachtungen), aber auch die Wiedergabe einer Hierarchie (z.B. "kleines Blutbild", bestehend aus "Erythrozyten", "Leukozyten", usw.).
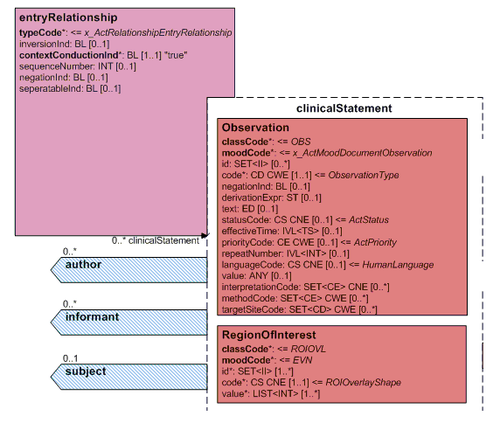
<ref group="Abbildung">Aufbau eines CDA-Dokuments aus XML Sicht</ref>Für das komplette dem CDA Release 2.0 zugrundeliegende Referenzmodell (R-MIM POCD_RM000040) wird auf den publizierten Standard verwiesen.<ref name="CDA" />
5.2.4 "CDA-Levels"[Bearbeiten]
Im CDA Body können Inhalte auf mehreren Strukturierungsebenen transportiert werden; diese Ebenen (umgangssprachlich "CDA-Levels") erlauben eine flexible Erweiterung der Interoperabilität von CDA Dokumenten.
- "Unstrukturierter Body" ("CDA-Level 1") ist ausschließlich auf die Lesbarkeit durch Menschen ausgelegt. Medizinische Inhalte werden als Text, Bilder oder auch nur als "eingebettetes PDF" (als unstrukturierter "NonXMLBody") transportiert.
- "Section-strukturierter Body" ("CDA-Level 2") ermöglicht eine Strukturierung der Inhalte nach Abschnitten ("Sections") mit festgelegter Bedeutung (z.B. "Anamnese", "Diagnosen") durch Anwendung von Section-Templates. Die Abschnitte sind mit einem vereinbarten Code versehen, der es ermöglicht, dass EDV-Programme diese eindeutig erkennen und als Block verarbeiten können.
- "Entry-strukturierter Body" ("CDA-Level 3") ist eine Technik zur Anreicherung eines lesbaren Dokuments mit medizinischen Einzelinformationen (z.B. "diastolischer Blutdruck", "ICD-10 Entlassungsdiagnose", "Körpergewicht in kg") durch Anwendung von Entry-Templates, die gemäß einer Vereinbarung maschinenlesbar codiert sind und daher automatisch in medizinische Informationssysteme integriert werden können.
Die Vereinbarungen für die Codierung in den CDA-Levels 2 und 3 werden durch Templates definiert und in Implementierungsleitfäden veröffentlicht. Die CDA-Levels können aufeinander aufbauend verwendet werden, ein Dokument kann gleichzeitig Informationen in allen drei CDA-Levels enthalten.
Diese grobe Einteilung kann erweitert bzw. verfeinert werden, da es einen Unterschied macht, ob ein CDA-Level 1 Dokument aus einem eingebetteten PDF besteht oder aus XML-Content ohne Templates oder ob ein CDA-Dokument zwar ein maschinenlesbares Entry enthält, aber nicht alle vorgesehenen. Daher wurden für ELGA die so genannten "ELGA Interoperabilitätsstufen" eingeführt.
6 Allgemeine Richtlinien für CDA-Implementierungsleitfäden[Bearbeiten]
Dieses Dokument spezifiziert eine Implementierung des Standards HL7 CDA Rel. 2; es wurde darauf geachtet, in den Grundzügen kompatibel mit dem FHIR-Standard zu sein. Daher werden Templates bereits in Richtung der FHIR Stilistik entwickelt, um Konzepte zu repräsentieren. Mechanismen für Negation (negationIndicator) und Attribute für unbekannte und fehlende Informationen (nullFlavors) werden nach Möglichkeit vermieden. Spezielle Leitfäden sollen diesem Prinzip folgen.
Um zukünftig automatische Auswertbarkeit und grenzüberschreitende Interoperabilität zu unterstützen, sollen Leitfäden so weit wie möglich strukturierte Daten (Entries) und mehrsprachige internationale Referenzterminologien wie SNOMED CT verwenden, die für die kostenfreie Nutzung in Österreich lizenziert wurden. Andere bevorzugte Terminologien, die in den Leitfäden verwendet werden, sind LOINC für Beobachtungen (z.B. Labortests) und Dokumentklassifizierung und Dokumentabschnitte (Sections) sowie UCUM für Maßeinheiten.
Nutzer dieses Leitfadens können die Projektseite in ART-DECOR® besuchen, um die Template-Spezifikationen zu durchsuchen und Beispiele zu überprüfen.
6.1 Konformitätskriterien[Bearbeiten]
6.1.1 Verwendung von Schlüsselwörtern[Bearbeiten]
Wenn im Text die Verbindlichkeit von Vorgaben angegeben wird, wird das durch Schlüsselwörter gekennzeichnet [gemäß RFC 2119], die in Majuskeln (Großbuchstaben) geschrieben werden. Die Angabe der Verbindlichkeit ersetzt nicht die Angabe von Kardinalität oder Nullwerten (die in HL7 Version 3 als nullFlavors ausgedrückt werden).
- MUSS bedeutet eine verpflichtend einzuhaltende Vorschrift (Gebot). Entspricht den Konformitätskriterien [M] und [R] 1...
- NICHT ERLAUBT formuliert ein verpflichtend einzuhaltendes Verbot. Entspricht dem Konformitätskriterium [NP].
- SOLL oder EMPFOHLEN steht für eine pragmatische Empfehlung. Es ist gewünscht und empfohlen, dass die Anforderung umgesetzt wird, es kann aber Gründe geben, warum dies unterbleibt. Entspricht dem Konformitätskriterium [R] 0...
- KANN oder OPTIONAL (engl. MAY, OPTIONAL) Die Umsetzung der Anforderung ist optional, sie kann auch ohne zwingenden Grund unterbleiben. Entspricht dem Konformitätskriterium [O].
6.1.2 Kardinalität[Bearbeiten]
Die Kardinalität beschreibt, wie oft ein Element innerhalb einer Struktur auftreten kann. Die Kardinalität wird durch ein Intervall zwischen der minimalen und maximalen Anzahl angegeben, getrennt durch "..". Eine unbegrenzte Anzahl wird durch ein "*" angegeben. Daraus ergeben sich mindestens folgende Möglichkeiten: 0..1; 0..*; 1..1; 1..*
6.1.3 Umgang mit optionalen Elementen[Bearbeiten]
Sind Elemente bzw. Attribute als "optional" gekennzeichnet ([O]) so ist ihre Verwendung OPTIONAL, aber es ist NICHT ERLAUBT, dass sie, wenn sie verwendet werden, leer sind. Möchte man ein optionales Element explizit mit einem leeren Wert angeben, so hat dies durch Kennzeichnung mit nullFlavor zu erfolgen.
6.1.4 Legende der Konformitätskriterien[Bearbeiten]
6.1.4.1 Optionalitäten von CDA-Elementen[Bearbeiten]
| Konformitäts-Kriterium | Mögliche Kardinalität | Verwendung von nullFlavor | Beschreibung |
|---|---|---|---|
| [M] | 1..1 1..* |
nicht erlaubt | Das Element MUSS mit einem korrekten "echten" Wert angegeben werden ("mandatory"). nullFlavor oder "Dummy"-Werte sind NICHT ERLAUBT. |
| [NP] | 0..0 | nicht erlaubt | Das Element ist NICHT ERLAUBT ("not permitted"). |
| [R] | 1..1 1..* |
erlaubt | Das Element MUSS in der Instanz vorhanden sein ("required"). Wenn ein Element nicht bekannt ist, ist die Verwendung eines nullFlavors vorgeschrieben, "Dummy"-Werte sind NICHT ERLAUBT. |
| 0..1 0..* |
nicht erlaubt | Das Element SOLL in der Instanz vorhanden sein, sofern bekannt ("required"). Wenn nicht bekannt, darf es nicht in der Instanz codiert sein und muss weggelassen werden. Ein nullFlavor ist daher NICHT ERLAUBT. Entspricht der in älteren Leitfäden gebräuchlichen Notation [R2] ("required if known"). | |
| [O] | 0..1 0..* |
erlaubt | Das Element ist OPTIONAL ("optional"). Sender können das Element angeben. Leere optionale Elemente sind nicht zugelassen, sofern kein nullFlavor angewandt wird. |
| [C] | Die Optionalität des Elements variiert in Abhängigkeit von anderen Elementen, Situationen oder Zuständen ("conditional"). Die konkreten Abhängigkeiten sind in Folge angegeben. |
<ref group="Tabelle">Legende der Optionalitäten von Elementen</ref>:Legende der Optionalitäten von Elementen
6.1.4.2 Optionalitäten von CDA-Attributen[Bearbeiten]
| Konformitäts-Kriterium | Mögliche Kardinalität | Beschreibung |
|---|---|---|
| [NP] | 0..0 | Das Attribut ist NICHT ERLAUBT. ("not permitted") |
| [R] | 1..1 | Das Attribut MUSS in der Instanz vorhanden sein. ("required") |
| [O] | 0..1 | Das Attribut ist OPTIONAL. ("optional") |
| [F] | 0..1
1..1 |
Wenn das Attribut angegeben wird, ist ein fixer Wert vorgeschrieben. ("fixed")
Für das Attribut ist ein fixer Wert vorgeschrieben. ("fixed") |
<ref group="Tabelle">Legende der Optionalitäten von Attributen</ref>:Legende der Optionalitäten von Attributen
6.2 Der nullFlavor[Bearbeiten]
Das Attribut @nullFlavor dient zur Kennzeichnung, dass ein Element nicht seiner Entsprechung gemäß befüllt werden kann. Die konkrete Anwendung des @nullFlavor Attributs ist im Rahmen dieser Implementierungsleitfäden nur erlaubt, wenn er explizit in der Spezifikation eines Elementes angegeben ist. Für codierte Elemente ist ein nullFlavor für unbekannte und fehlende Information nach Möglichkeit zu vermeiden, bevorzugt ist die Verwendung eines Codes mit demselben Informationsgehalt (etwa für "keine Allergie bekannt" das SNOMED Konzept 716186003 "No known allergy").
Beispiel für ein Element, welches mit dem @nullFlavor versehen wurde:
<id nullFlavor="UNK" />
Wenn in einem Element ein nullFlavor angegeben wurde, kann nicht gleichzeitig ein anderes Attribut eingetragen werden.
nullFlavor Beispiele:
| nullFlavor | displayName | Deutsche Übersetzung | Anwendung |
|---|---|---|---|
| NI | NoInformation | keine Information vorhanden | wenn es keine Informationen gibt |
| UNK | Unknown | unbekannt | wenn es Informationen gibt, diese aber unbekannt sind |
| MSK | Masked | maskiert | wenn es Informationen gibt, diese aber nicht bekannt gegeben werden (vertraulich, nicht freigegeben) |
| NA | Not applicable | nicht anwendbar | wenn keine Codierung verfügbar ist |
| OTH | Other | Andere | wenn eine Codierung nur in einem alternativen Codesystem verfügbar ist |
<ref group="Tabelle">nullFlavor-Beispiele aus Value-Set ELGA_nullFlavor</ref>: nullFlavor-Beispiele aus Value-Set ELGA_nullFlavor
6.3 Maximum-Set[Bearbeiten]
Das CDA Modell beschreibt ein höchst umfangreiches Schema von Informationselementen und bietet in manchen Bereichen über rekursive, beliebig tief verschachtelbare Elemente eine theoretisch unendlich hohe Anzahl von Möglichkeiten, Informationen abzulegen. Die vollständige Beschreibung und Definition aller Elemente in einem Implementierungsleitfaden wäre daher äußerst aufwändig und ist in den ELGA Implementierungsleitfäden nicht erfolgt.
Vielmehr beschreiben die ELGA Implementierungsleitfäden lediglich jene Elemente, die erlaubt sind. Die Verwendung aller nicht angegebenen Elemente und Attribute ist NICHT ERLAUBT. Für alle Templates gelten die im Kapitel Datentypen angegebenen Einschränkungen. Die ELGA Implementierungsleitfäden beschreiben daher ein sogenanntes "Maximum-Set", Die ELGA Templates sind demnach als "closed templates" entsprechend dem HL7 Templates Standard zu betrachten.
Elemente oder Attribute, die nicht vom Allgemeinen oder einem speziellen ELGA-Implementierungsleitfaden definiert wurden, sind NICHT ERLAUBT.
6.3.1 Ausnahmen[Bearbeiten]
Für diese Regel existieren nur die im Folgenden genannten Ausnahmen:
6.3.1.1 Ausnahme: "templateId"[Bearbeiten]
templateId-Elemente KÖNNEN bei Bedarf an allen laut CDA-Schema möglichen Stellen verwendet werden. Wenn bereits templateId-Elemente laut Spezifikation vorgeschrieben sind, KÖNNEN beliebig viele weitere templateId-Elemente angegeben werden.
6.3.1.2 Ausnahme: Fixierte Attribute[Bearbeiten]
Attribute, die gem. CDA-Schema mit "fixed" angegeben sind, haben einen festen Wert, daher können diese Attribute auch weggelassen werden. Diese Attribute werden daher üblicherweise nicht beschrieben und angegeben. Die Angabe von fixierten Attributen oder Attributen mit ihrem gem. CDA-Schema definierten Default-Wert ist erlaubt, auch wenn diese nicht explizit im Leitfaden beschrieben sind.
6.3.1.3 Explizit angegebene Ausnahmen[Bearbeiten]
Im speziellen Implementierungsleitfaden KÖNNEN bestimmte Sektionen als "offene Templates" definiert werden und Ausnahmen für Subsektionen und Entries zulassen.
↔ Hinweis zum XDS-Mapping: Beim XDS-Attribut XDSDocumentEntry.formatCode muss ein zusätzliches Plus-Zeichen ("+") am Ende des Strings hinzugefügt werden, wenn in einem Dokument selbst-definierte maschinenlesbare Elemente vorhanden sind.
Beispiel: urn:elga:lab:2011:EIS_FullSupport+
Siehe dazu die entsprechende Regelung im Leitfaden "ELGA XDS Metadaten (XDSDocumentEntry)", [OID Root 1.2.40.0.34.7.6], Kapitel Zusatz bei selbst-definierten maschinenlesbaren Elementen (Dokumente in EIS "Enhanced" oder "Full Support").
6.3.1.4 Hinweis zur Implementierung weiterverarbeitender Software[Bearbeiten]
CDA-Dokumente können unter Umständen "fremde" Elemente oder Attribute enthalten, die der "Maximum-Set" Vorschrift dieses Leitfadens widersprechen (z.B. aufgrund von Software-Fehlern). Sollten derartige Elemente oder Attribute im CDA-Dokument vorhanden sein, soll weiterverarbeitende Software so implementiert sein, dass dies nicht zu Fehlern in der Weiterverarbeitung der Dokumente führt.
6.4 Umgang mit codierten Informationen und Terminologien[Bearbeiten]
6.4.1 Codierte Information[Bearbeiten]
Eine Prämisse des Allgemeinen Leitfadens ist eine durchgängige Maschinenlesbarkeit der einzelnen medizinischen Informationen. Dazu ist es notwendig, die Informationen mit codierten Konzepten auszudrücken ("Codierung"). Codierte Informationen erlauben eine Übersetzung in andere Sprachen ("Translation") und eine Überführung in andere Terminologien oder Codesysteme ("Transcodierung"). Die Datentypen für codierte Informationen werden in Allgemeiner Leitfaden: Codierte Elemente beschrieben. Wenn die erwünschten Informationen nicht vorliegen oder nicht mit codierten Konzepten ausgedrückt werden können, kommen die im Folgenden vorgestellten Methoden zum Einsatz.
6.4.2 Unbekannte und keine Information[Bearbeiten]
Nicht immer können für bestimmte erwünschte Inhalte (Erkrankungen, Zustände, Eigenschaften, etc.) auch tatsächlich Angaben gemacht werden. Der Leitfaden unterscheidet dabei zwischen zwei Situationen:
- Der erwünschte Inhalt ist unbekannt (z.B. wenn die Medikation eines Patienten unbekannt ist)
- Der erwünschte Inhalt liegt bekanntlich nicht vor (z.B. wenn der Patient tatsächlich keine Medikamente einnimmt)
Spezifischere Formen abwesender Information oder Negation wurden nicht als relevant erachtet, wie zum Beispiel die Abwesenheit einer Allergie auf ein bestimmtes Antigen, der Ausschluss einer bestimmten Krankheit oder die Tatsache, dass eine bestimmte Impfung nicht durchgeführt wurde.
Für die semantische Repräsentation dieser Situationen werden SNOMED-CT-Codes verwendet; die sonst in CDA üblichen Mechanismen (nullFlavor, negationInd) werden hier weitgehend vermieden. So sollen die Inhalte unabhängig von einem bestimmten technischen Standard ausgedrückt werden, die Implementierungen robuster und einfacher gemacht sowie die Transformation in andere Standards wie z.B. FHIR erleichtert werden.
In einigen Fällen fehlen zum Zeitpunkt der Erstellung des Leitfadens die benötigten SNOMED-CT-Konzepte, z. B. "Allergische Disposition nicht bekannt (Situation)". Diese Konzepte wurden bereits beantragt und harren der Aufnahme in eine zukünftige Version von SNOMED CT International Edition. Zwischenzeitlich werden diese Konzepte durch temporäre Platzhalter-Codes dargestellt, die alle mit 'X-' beginnen (z.B. X-AllergicDispositionNotKnown).
6.4.2.1 Darstellung von unbekannter und bekannt fehlender Information im Text[Bearbeiten]
Unbekannte und fehlende Information soll auch im menschenlesbaren Text (section.text) einheitlich dargestellt werden. Folgende Textbausteine sind VERPFLICHTEND zu verwenden:
- Es liegt keine Information über [X] vor (Bedeutung: die Informationen über [X] wurden nicht erhoben, können nicht erhoben werden oder sind nicht verfügbar)
- Keine [X] (Bedeutung: Es gibt tatsächlich keine Informationen über [X] oder [X] liegt nachweislich nicht vor.)
6.4.2.1.1 Anwendungsbeispiele[Bearbeiten]
- Es liegt keine Information über Allergien oder Intoleranzen vor:
- Es wurden keine Impfungen durchgeführt:
6.4.2.1.2 Codebeispiel für den lesbaren Text[Bearbeiten]
Tabellarische Darstellung gilt auch für unbekannte und fehlende Informationen, zusätzlich KANN die Nicht-Information optisch hervorgehoben werden.
<title>Allergien und Intoleranzen</title>
<text>
<table>
<tbody>
<tr ID="al-1">
<td>
<content styleCode="xELGA_blue">Es liegt keine Information über Allergien oder Intoleranzen vor</content>
</td>
</tr>
</tbody>
</table>
</text>
6.4.3 Uncodierte Information[Bearbeiten]
Bei der Erstellung des Dokumentes können möglicherweise bestimmte Informationen vorliegen, die nicht codiert werden können, weil
- die Information nicht mit den im Leitfaden zugelassenen Terminologien (Value Sets) dargestellt werden kann oder
- die Information in keiner bekannten Terminologie enthalten ist, beziehungsweise der Inhalt nicht codiert wurde.
Diese erste Situation wird mit dem folgenden Beispiel verdeutlicht.
<code codeSystem="1.2.40.0.34.5.174" nullFlavor="OTH">
<originalText>
<reference value="#ref1"/>
</originalText>
</code>
Für die Information ist kein geeigneter Code im vorgegebenen Codesystem vorhanden (im Beispiel ICD-10 BMGF 2018). Der konkrete Inhalt wird im Section-Text angegeben und vom Code-Element nur referenziert (value im reference-Element). Diese Variante kann für coding strength CNE (coded no extensions) eingesetzt werden. Der Elementname kann auch anders sein, z.B. Value.
Hinweis: Mit den zugrunde liegenden Datentypen (HL7 V3 Data Types R1) kann über diese Methode nur ausgesagt werden, dass ein Konzept nicht in einem bestimmten Codesystem verfügbar ist. Die Aussage, dass ein Code zwar im Codesystem, aber nicht im referenzierten Value Set verfügbar ist, kann so nicht getroffen werden; spätere Versionen dieses Leitfadens können gegebenenfalls auf Data Types R2 aufbauen, um diese Angabe zu unterstützen. Ebenfalls stößt diese Methode an ihre Grenzen, wenn im Value Set zwei Codesysteme referenziert werden. Als Problemumgehung kann ein Code mit der gewünschten Aussage ("nicht codierbar") ins Value Set aufgenommen werden.
Das folgende Beispiel bezieht sich auf die zweite Situation:
<value xsi:type="CD" nullFlavor="NA">
<originalText>
<reference value="#ref1"/>
</originalText>
</value>
Im zweiten Beispiel wird der allgemeinste nullFlavor "NA" (not applicable) verwendet; es gilt sowohl für coding strength CNE (coded no extensions) and CWE (coded with extensions). Wie im ersten Beispiel wird der konkrete Inhalt im Section-Text angegeben und vom Code-Element nur referenziert (value im reference-Element).
Die zweite Variante ist die häufiger eingesetzte Variante.
Anmerkung: Der geeignetste nullFlavor wäre eigentlich "UNC" (Uncoded), aber dieser nullFlavor ist in der RIM-Version, auf der HL7 CDA Rel.2 aufbaut, nicht verfügbar. Daher wird der nullFlavor "NA" (not applicable) verwendet.
6.4.4 Nicht zugeordnete codierte Information[Bearbeiten]
Bei der Erstellung des Dokumentes können möglicherweise bestimmte Informationen codiert in der Quelldokumentation vorliegen, aber die Codes sind nicht in den im Leitfaden zugelassenen Terminologien (Value Sets) verfügbar.
Wenn das codierte Element mit der coding strength CNE (coded no extensions) angegeben ist, wird der nullFlavor "OTH" verwendet; bei coding strength CWE (coded with extensions) der nullFlavor "NA".
<value xsi:type="CD" codeSystem="2.16.840.1.113883.6.96" nullFlavor="OTH">
[
<originalText>
<reference value="#ref1"/>
</originalText>
]
<translation code="A02.9" codeSystem="1.2.40.0.34.5.174"
displayName="Salmonelleninfektion, nicht näher bezeichnet"/>
</value>
Die eckigen Klammern deuten an, dass Elemente optional sind. Hinweis: Mit den zugrunde liegenden Datentypen (HL7 V3 Data Types R1) kann über diese Methode nur ausgesagt werden, dass ein Konzept nicht in einem bestimmten Codesystem verfügbar ist. Die Aussage, dass ein Code zwar im Codesystem, aber nicht im referenzierten Value Set verfügbar ist, kann so nicht getroffen werden; spätere Versionen dieses Leitfadens können gegebenenfalls auf Data Types R2 aufbauen, um diese Angabe zu unterstützen. Ebenfalls stößt diese Methode an ihre Grenzen, wenn im Value Set zwei Codesysteme referenziert werden. Als Problemumgehung kann ein Code mit der gewünschten Aussage ("nicht codierbar") ins Value Set aufgenommen werden.
Im Falle der coding strength CWE (coded with extensions) wird der nullFlavor "NA" vorgeschlagen und ebenso die Angabe des korrekten Codes im <translation>-Teilelement. Dies ermöglicht die Angabe, dass eine Zuordnung zu dem Referenz-Value Set versucht wurde, aber keine geeigneten Zielcodes identifiziert wurden.
<value xsi:type="CD" codeSystem="2.16.840.1.113883.6.96" nullFlavor="NA">
[
<originalText>
<reference value="#ref1"/>
</originalText>
]
<translation code="A02.9" codeSystem="1.2.40.0.34.5.174"
displayName="Salmonelleninfektion, nicht näher bezeichnet"/>
</value>
Die eckigen Klammern deuten an, dass Elemente optional sind.
6.4.5 Zugeordnete codierte Information (Übersetzung)[Bearbeiten]
Es kann vorkommen, dass bestimmte Informationen codiert in der Quelldokumentation vorliegen, aber in einer anderen Terminologie als vom Leitfaden zugelassen. Wenn die codierten Konzepte korrekt von der einen in die andere Terminologie zugeordnet werden können (also "übersetzt" oder "gemappt"), ist es erlaubt, auch die originalen Codes zusätzlich anzugeben.
1. Fall: Ein einzelner lokaler Code wird auf einen Code im Referenz-Value Set gemappt
<value xsi:type="CD" code="42338000" codeSystem="2.16.840.1.113883.6.96"
displayName="Salmonella gastroenteritis">
[
<originalText>
<reference value="#ref1"/>
</originalText>
]
<translation code="003.0" codeSystem="2.16.840.1.113883.6.103"
displayName="Gastroenterite da Salmonella"/>
</value>
Die eckigen Klammern deuten an, dass Elemente optional sind.
2. Fall: Mehrere lokale Codes werden auf das Referenz-Value Set gemappt
<value xsi:type="CD" code="C50.9" codeSystem="1.2.40.0.34.5.171"
codeSystemName="ICD-10 BMGF"
displayName="Bösartige Neubildung: Brustdrüse, nicht näher bezeichnet">
[
<originalText>
<reference value="#problem4name"/>
</originalText>
]
<translation code="code-example" codeSystem="1.999.999"
codeSystemName="this is only an example"
displayName="FEMALE BREAST INFILTRATING DUCTAL CARCINOMA, STAGE 2">
<translation code="174.9" codeSystem="2.16.840.1.113883.6.103"
codeSystemName="ICD-9CM"
displayName="Malignant neoplasm of breast (female), unspecified"/>
<translation code="C50.919" codeSystem="2.16.840.1.113883.6.90"
codeSystemName="ICD-10-CM"
displayName="Malignant neoplasm of unspecified site of unspecified female breast"/>
</translation>
<translation code="422479008" codeSystem="2.16.840.1.113883.6.96"
codeSystemName="SNOMED CT"
displayName="FEMALE BREAST INFILTRATING DUCTAL CARCINOMA, STAGE 2"/>
</translation>
</value>
Die eckigen Klammern deuten an, dass Elemente optional sind.
3. Fall: Ein lokaler Code entstammt derselben Terminologie wie das Referenz-Value Set, besitzt aber eine unterschiedliche Granularität.
<code code="60591-5" codeSystem="2.16.840.1.113883.6.1"
codeSystemName="LOINC" displayName="Patient Summary">
<translation code="60592-3" codeSystem="2.16.840.1.113883.6.1"
displayName="Patient summary unexpected contact"/>
</code>
Hinweis: Die R1 Datentyp-Definition versteht die <translation> nur als Mapping zwischen unterschiedlichen Codesystemen ("a set of other concept descriptors that translate this concept descriptor into other code systems"). Es hat sich aber die Interpretation durchgesetzt, dass auch dasselbe Konzept in mehreren Repräsentationen ausgedrückt werden kann, wie es einige Codesysteme (z.B. SNOMED CT) erlauben.
6.5 Mehrsprachigkeit[Bearbeiten]
Codierte Informationen können einfach in unterschiedlichen Sprachen ausgedrückt werden. Für einen zuverlässigen und sicheren grenzüberschreitenden Datenaustausch (EU eHealth Network) ist dies eine funktionelle Notwendigkeit.
Der zugrunde liegende Standard HL7 CDA Rel. 2 hat mit Bordmitteln keine Möglichkeit, um einen Anzeigetext zu einem codierten Konzept in mehreren Sprachen anzugeben. Dieser Leitfaden übernimmt daher als optionales Element die Erweiterung (extension) 'ips:designation', die im HL7 IPS Leitfaden dafür vorgeschlagen wird.
Beispiel 1: Ohne Code-Mapping
<code code="60591-5" codeSystem="2.16.840.1.113883.6.1" codeSystemName="LOINC" displayName="Patient Summary"> <ips:designation language="it-IT">Profilo Sanitario Sintetico</ips:designation> <ips:designation language="fr-FR">Patient Summary</ips:designation> <ips:designation language="en">Patient Summary</ips:designation> </code>
Beispiel 2: Mit Code-Mapping und Referenz zum narrativen Text
<value xsi:type="CD" code="42338000" codeSystem="2.16.840.1.113883.6.96"
displayName="Salmonella-gastroenteritis">
<ips:designation language="da-DK">Salmonella-gastroenteritis</ips:designation>
<ips:designation language="en">Salmonella gastroenteritis (disorder)</ips:designation>
<originalText>
<reference value="#ref1"/>
</originalText>
<translation code="003.0" codeSystem="2.16.840.1.113883.6.103"
displayName="Gastroenterite da Salmonella"/>
</value>
6.5.1 Übersetzung des narrativen Textes[Bearbeiten]
Bei einer Übersetzung eines Dokuments muss vor allem der lesbare Text in anderen Sprachen dargestellt werden können. Die Übersetzung muss dazu bereits im Dokument vorhanden sein, wobei die Übersetzung von einer Person durchgeführt werden kann oder aber automatisch aus den maschinenlesbaren Elementen abgeleitet werden kann. Bei der Darstellung muss (a) die Sprache der Ausgabe identifiziert werden und (b) angegeben werden, ob es sich um das Original handelt oder die Übersetzung. Außerdem sollte die Quelle (Freitext, maschinenlesbare Elemente) und Art der Übersetzung (Übersetzer, automatisch, etc.) angegeben werden.
Die hier verwendete Methode enthält das Original im <text>-Element der Section und die optionalen Übersetzungen in einem <text>-Element einer Subsection, wobei pro Übersetzung eine Subsection angegeben wird. (specified in template 2.16.840.1.113883.10.22.3.15)
Beispiel:
<section>
<templateId root="2.16.840.1.113883.3.1937.777.13.10.5"/>
<id root="..." extension="..."/>
<code code="48765-2" codeSystem="2.16.840.1.113883.6.1"
displayName="Allergies and adverse reactions"/>
<title>Allergies and Intolerances</title>
<text>No known Allergies</text>
<!-- omissions -->
<component>
<section>
<!-- subordinate section carrying a translation of the parent section -->
<title>Allergie ed Intolleranze</title>
<text>Nessuna Allergia Nota</text>
<languageCode code="it-IT"/>
</section>
</component>
</section>
6.6 Herkunft der Information[Bearbeiten]
Die Angabe der Quelle einer Information kann für die klinische Bewertung dieser Information maßgeblich sein, besonders wenn ein Dokument aus mehreren Quellen (automatisch) zusammengestellt wurde. Daher erlaubt dieser Leitfaden eine systematische und durchgängige Angabe der Herkunft der elektronischen Daten.
6.6.1 Herkunftsangabe auf Dokument-Ebene[Bearbeiten]
Der Autor des CDA Dokuments MUSS verpflichtend im Header angegeben werden. Dabei kann es sich um eine Person ("human curated") oder um eine Software ("software assembled") handeln (siehe Verfasser des Dokuments ("author")).
6.6.2 Herkunftsangabe auf Section-Ebene[Bearbeiten]
Für jeden Dokumentationsabschnitt (Section) können jeweils mehrere Autoren und Informanten angegeben werden. Da die Zuordnung der Einzelinformation bei Angabe mehrerer Autoren und Informanten uneindeutig ist, wird empfohlen, die Herkunft auf Entry-Ebene anzugeben.
- Autor (Gesundheits-Fachperson, die die Information erstellt hat mit Name und Organisation).
- Informant (Person, auf deren Angabe die Information beruht: der Patient selbst oder eine dem Patienten verwandte oder bekannte Person)
6.6.3 Herkunftsangabe auf Entry-Ebene[Bearbeiten]
- Autor (Gesundheits-Fachperson, die die Information erstellt hat mit Name und Organisation)
- Informant (Person, auf deren Angabe die Information beruht: der Patient selbst oder eine dem Patienten verwandte oder bekannte Person)
- Dokumentverweis (externalDocument): für jedes Entry kann eine ID angegeben werden, die auf ein externes Dokument verweist, aus dem die Information stammt.
6.7 Zeitangaben[Bearbeiten]
Für den Geltungsbereich dieses Leitfaden dürfen Zeit-Elemente nur auf diese Arten angegeben werden:
- Datum und Uhrzeit mit Zeitzone im Format YYYYMMDDhhmmss[+/-]HHMM
- Datum im Format YYYYMMDD
- ungenaues Datum im Format YYYYMM oder YYYY
Ist nur eine weniger genaue Zeitangabe verfügbar, sind die fehlenden Stellen mit der Ziffer Null aufzufüllen. Also zum Beispiel ist für "September 2017" die Zeichenfolge 20170900 anzugeben. Die HL7 V3 Datentypen interpretieren Datumswerte so, als ob alle möglichen, aber nicht angegebenen Stellen mit 0 befüllt wären.
Achtung bei Zeitintervallen: Ein Datum, das mit YYYYMMDD angegeben wurde, wird standardgemäß interpretiert als YYYYMMDD000000 – also der Tag um 0:00:00 Uhr. Wenn also als Zeitraum z.B.: der ganze 1. Dezember 2017 angegeben werden soll, MUSS das so erfolgen:
<low value="20171201"/> <high value="20171202"/>
Für mehr Klarheit empfiehlt sich daher die zusätzliche Angabe der Zeit mit Zeitzone:
<low value="20171201000000+0100"/> <high value="20171201235959+0100"/>
6.8 Terminologien[Bearbeiten]
6.8.1 ELGA Value Sets[Bearbeiten]
Ein Value Set ist eine eindeutig identifizierbare und versionierte Sicht auf ein oder mehrere Codesysteme. Es kann als Zusammenstellung von einem oder mehreren Codes aus einem oder mehreren Codesystemen gesehen werden. Ein Value Set enthält die Codes selbst und die Information über die Herkunft des Codes (das Source-Codesystem), z.B. ELGA Value-Sets "ELGA_MaritalStatus", "ELGA_Laborparameter".
Wenn in den CDA Implementierungsleitfäden eine Werteauswahl getroffen werden kann, wird ein passendes Value Set mit einem eindeutigen Namen angegeben.
6.8.2 Value Set Binding[Bearbeiten]
Für ELGA gilt grundsätzlich eine DYNAMISCHE Bindung an Value Sets. Das bedeutet, dass immer die aktuell am Terminologieserver<ref name="Terminologieserver"/> publizierte Version eines Value Sets anzuwenden ist. (Das Setzen des entsprechenden Schlüsselworts DYNAMIC ist daher in den Leitfäden optional).
Für jedes Value Set ist auch ein Zeitpunkt angegeben, an dem es Gültigkeit erlangt ("Gültig ab"), das ist für Value Sets wichtig, die schon vor ihrem Inkrafttreten veröffentlicht werden. Value Sets sind so lange gültig, bis das Gültigkeitsdatum einer neueren Version dieses Value Sets erreicht wird – dann gilt die neuere Version.
Value Sets können auch STATISCH an ein Code-Element gebunden werden. Das wird gekennzeichnet durch die Angabe des Value Sets mit Name, OID, Version und "Gültig ab"-Datum (effectiveDate) sowie dem Schlüsselwort STATIC.
Im CDA-Dokument KANN über die Attribute @ValueSet und @ValueSetVersion angegeben werden, welches Value Set in welcher Version als Basis für die Befüllung des jeweiligen Datenelements verwendet wurde (code-Element CD (Concept Descriptor)).
6.8.3 Inhalte von Value Sets[Bearbeiten]
Value Sets enthalten mindestens den Code, das Codesystem (in dem der Code definiert wurde) und einen DisplayName (die Klartext-Darstellung des Codes wie vom originalen Codesystem vorgesehen). Zusätzlich wird um eine hierarchische Baumstruktur zu ermöglichen Level und Typ angegeben: Level ist die Hierarchieebene (numerisch, beginnend mit 0 bei der Wurzel, ein höherer Wert bedeutet eine tiefere Ebene) und Typ gibt die Art des Knotens im Baum an:
- L (leaf) Blattknoten ohne weitere Spezialisierungen. DARF verwendet werden.
- S (specializable) Knoten mit weiteren Codes auf einer tieferen Ebene. DARF verwendet werden.
- A (abstract) Knoten mit weiteren Codes auf einer tieferen Ebene. DARF NICHT verwendet werden, nur die Spezialisierung davon (d.h. die Unterelemente).
- D (deprecated) Blattknoten, DARF NICHT mehr verwendet werden. (CDA Dokumente, die mit einer Vorversion des Values Sets erstellt wurden, in der das Konzept noch nicht Deprecated war, können diesen Code jedoch enthalten).
Value Set Inhalte mit Typ A (abstract) und D (deprecated) DÜRFEN NICHT im CDA Dokument verwendet werden.
6.8.4 Änderbarkeit von Value Sets[Bearbeiten]
Inhalte von Value Sets können sich ändern, der Name und die OID eines Value Sets bleiben aber gleich. Bei neuen Versionen werden Versionsnummer, Änderungsdatum und "Gültig ab"-Datum (effectiveDate) angegeben. Damit kann die Gültigkeit zu einer bestimmten Zeit rekonstruiert werden.
In Ausnahmen kann bei der Definition eines Value Sets angegeben werden, dass es nicht geändert oder versioniert werden darf (Property "Immutability").
6.8.5 Publikation der Value Sets am Terminologieserver[Bearbeiten]
Sämtliche in den Implementierungsleitfäden verwendeten Value Sets werden am österreichischen Terminologieserver publiziert. <ref name="Terminologieserver"/> Value Sets sind nicht nur durch einen eindeutigen Namen, sondern auch durch eine OID, und eine Versionsnummer gekennzeichnet, weiters werden Gültigkeitsstatus und ein "Gültig ab"-Datum angegeben. Damit die jeweils aktuelle Version der Value Sets angewendet werden kann, soll der Terminologieserver regelmäßig auf Update abgeprüft werden. Es wird EMPFOHLEN, diese Überprüfung täglich durchzuführen. Weitere Hinweise zum korrekten Umgang mit Terminologien finden sich im "Leitfaden für den Umgang mit Terminologien in ELGA"<ref>Sabutsch, S. & C. Seerainer: Leitfaden zur Nutzung von ELGA-Terminologien http://elga.gv.at/CDA</ref>.
6.8.6 Terminologiedatum[Bearbeiten]
Das Datum, an dem sämtliche lokal zur Implementierung verwendeten Value Sets mit dem österreichischen Terminologieserver abgeglichen wurden, wird über das "Terminologiedatum" angegeben: Dieses Datum wird in der Notation "YYYYMMDD" im eigenen Element "terminologyDate" angegeben (siehe Kapitel Terminologiedatum ("hl7at:terminologyDate")). Beim Abgleich der Terminologien müssen immer alle Value Sets, die für ein CDA-Dokument notwendig sind, auf die am Terminologieserver aktuelle Version aktualisiert werden. Dokumente, die nur teilweise auf dem aktuellen Stand beruhen, könnten inkonsistent sein und MÜSSEN vermieden werden.
6.9 PDF Format-Vorschrift[Bearbeiten]
In CDA Dokumenten können Dokumente im PDF Format an verschiedensten Stellen eingebettet werden, entweder als gesamter CDA-Body oder als eingebetteter Inhalt in gewissen CDA-Sektionen. Im Hinblick auf eine dauerhafte Verfügbarkeit der Daten muss mindestens gewährleistet werden, dass diese PDF-Dokumente zuverlässig und eindeutig visuell reproduzierbar sind. Dies kann über die Einhaltung der Mindestkriterien der Norm ISO 19005-1:2005 sichergestellt werden (PDF/A-1b Basic bzw. PDF/A-3b Basic). Die Norm beschreibt zusätzlich die Barrierefreiheit der Dokumente, sodass sie von einem Screenreader vorgelesen werden können (PDF/A-1a Accessible bzw. PDF/A-3a Accessible). Dieser Implementierungsleitfaden schreibt daher als Minimalanforderung vor, dass jedes eingebettete PDF-Dokument dem Standard PDF/A-1b bzw. PDF/A-3b entsprechen MUSS. Im Sinne der Barrierefreiheit ist die Umsetzung von PDF/A-1a bzw. PDF/A-3a EMPFOHLEN.
Alle in ELGA-CDA-Dokumente eingebetteten PDF-Dateien MÜSSEN dem Standard PDF/A-1b bzw. PDF/A3-b (gemäß "ISO 19005-1:2005 Level A conformance") entsprechen. Die Umsetzung von PDF/A-1a bzw. PDF/A-3a ist EMPFOHLEN.
6.10 Größenbeschränkung von eingebetteten Objekten[Bearbeiten]
In CDA Dokumenten können verschiedene Objekte (z.B. PDF-Dokumente, Bilder) eingebettet werden (siehe "Eingebettetes Objekt-Entry").
Die Größe von CDA-Dokumenten und den Anhängen wird durch die Infrastruktur beschränkt, mit der die Dateien übertragen und gespeichert werden. Der CDA-Standard und dieser Leitfaden schränken die Größen für diese Objekte nicht ein, es wird allerdings EMPFOHLEN, diese in Bezug auf Anzahl und Speicherbedarf so klein wie möglich zu halten. Es liegt in der Verantwortung des Erstellers, die Größe der über ELGA bereitgestellten CDA-Dateien etwa durch Verringerung der Auflösung oder der Anzahl der Einzelbilder auf eine sinnvolle und angemessene Größe zu beschränken. EMPFEHLUNG: Damit der Download von e-Befunden keine unnötigen Verzögerungen verursacht, SOLL die Gesamtgröße von CDA-Dateien 20 MB nicht überschreiten (Die ELGA-Infrastruktur beschränkt die Größe von Dokumenten auf 20 MB<ref name="ELGA-Gesamtarchitektur">ELGA Gesamtarchitektur 2.30a</ref>).
6.11 Verbot von CDATA[Bearbeiten]
Die Verwendung von CDATA-Abschnitten (<![CDATA[…]]>), also von Zeichenketten, die vom Parser nicht als XML-Quellcode interpretiert werden können, ist für ELGA CDA Dokumente generell NICHT ERLAUBT.
6.12 ELGA Interoperabilitätsstufen[Bearbeiten]
Der zukünftige Nutzen von e-Befunden in ELGA hängt von ihrem Strukturierungsgrad ab: Je einheitlicher und strukturierter die Informationen vorliegen, desto besser können die Daten durch IT-Systeme verarbeitet und ausgewertet werden. Die "ELGA Interoperabilitätsstufen" (EIS) definieren eine bestimmte Menge von Vorgaben für Section und Entry-Level Templates ("CDA Levels" 2 und 3). Die Mindeststandards für die Datenstruktur der CDA-Dokumente und die Zeitpunkte für die verbindliche Verwendung werden per Verordnung des für Gesundheit zuständigen Ministers festgelegt.
- EIS "Basic" und EIS "Structured": EIS "Basic" beschreibt die für alle Dokumente in ELGA verpflichtende Mindeststrukturierung. Dokumente auf dieser Stufe müssen nur die Daten codiert enthalten, die unter anderem für das Dokumentenregister und das Berechtigungssystem unbedingt benötigt werden (CDA Header). Dieser Mindeststrukturierungsgrad und die Zuordnung zu einer definierten Dokumentenklasse sind die Voraussetzung für die Verwendung der Dokumente in ELGA. CDA-Dokumente auf dieser Stufe folgen den Anforderungen des "Allgemeinen Implementierungsleitfaden für CDA-Dokumente" und allfälliger Header-Spezifikationen eines speziellen Leitfadens. In EIS "Basic" ist zusätzlich die Möglichkeit gegeben, ein Organisations-Logo in Level 3 Codierung einzubetten. Die Herausforderung für die Dokumentenersteller beziehungsweise die dokumentenerstellenden EDV-Systeme ist auf dieser Stufe minimal, medizinische Inhalte sollen als XML-Textelemente vorhanden sein, können aber auch als PDF in die CDA-Dokumente eingebettet werden (eingebettetes PDF oder XML ohne Templates).
EIS "Structured" ist eine Erweiterung der verpflichtenden Mindeststrukturierung EIS "Basic". Die medizinischen Inhalte folgen auf dieser Stufe der Gliederung und dem Aufbau, den der Leitfaden für die höheren EIS "Enhanced" und "Full Support" vorgibt, sie folgen aber nicht der entsprechenden technischen Struktur und Codierung. EIS "Structured" Dokumente decken sich technisch mit EIS "Basic", erscheinen dem Leser inhaltlich wie EIS "Enhanced" und "Full Support" Dokumente, ohne deren semantische Interoperabilität zu unterstützen.
- EIS "Enhanced" und EIS "Full Support" ermöglichen eine einheitliche Darstellung und barrierefreie Anzeige der Daten im ELGA Portal, die mit PDF nicht erreichbar ist. CDA-Dokumente dieser Stufen folgen zusätzlich den Anforderungen eines speziellen Implementierungsleitfadens, der für die jeweilige Stufe angeführt wird. Die Anforderungen betreffen vorwiegend Vorgaben für die Gliederung und Strukturierung des lesbaren Textes, Verwendung und Codierung der CDA Sektionen (CDA-Level 2), können aber auch CDA Level-3 Vorgaben enthalten.
- EIS "Enhanced" stellt eine Zwischenstufe auf dem Weg zu "Full Support" dar. Die Vorgaben betreffen eine kleinere Anzahl an maschinenlesbaren Elementen und sind weniger streng als bei "Full Support".
- EIS "Full Support" kann gegenüber EIS "Enhanced" zusätzliche maschinenlesbar codierte medizinische Inhalte enthalten, die in ELGA CDA-Dokumenten anzugeben sind.
| Stufe | Beschreibung der ELGA Interoperabilitätsstufe (EIS) |
|---|---|
| "EIS BASIC" und "EIS STRUCTURED" | Einheitlicher CDA-Header. Verwendung der Dokumente in ELGA (Aufnahme in Dokumentregister, Anzeige für Berechtigte). Minimale Anforderungen an erstellende Systeme ("eingebettetes PDF" oder XML ohne Templates)
EIS "Structured" erfüllt die fachlich-inhaltlichen, aber nicht die technischen Vorgaben für den Aufbau und die Gliederung des Dokuments aus den speziellen Leitfäden. |
| "EIS ENHANCED" | Einheitliche Dokumentation (Strukturierung, Gliederung), barrierefreie Darstellung. Minimale Anforderungen an Level-3 Codierung, gemäß den speziellen Leitfäden. |
| "EIS FULL SUPPORT" | Maschinenlesbare Inhalte, automatische Übernahme der Daten in ein medizinisches Informationssystem möglich. Volle Unterstützung der Level 3-Codierung, gemäß den speziellen Leitfäden. |
<ref group="Tabelle">ELGA Interoperabilitätsstufen</ref>ELGA Interoperabilitätsstufen
Welche Informationen für das Erreichen der Interoperabilitätsstufen EIS Enhanced oder Full Support codiert vorliegen müssen, wird durch den speziellen Implementierungsleitfaden definiert. Wenn die Mindestanforderungen für EIS Enhanced nicht erreicht werden, ist das Dokument als EIS Basic/Structured zu deklarieren.
Die ELGA Interoperabilitätsstufen beschreiben einen ansteigenden Grad der Strukturierung und Codierung der medizinischen Inhalte unabhängig von "CDA-Levels". Die Harmonisierungsgruppen legen aufgrund ihrer fachlichen Expertise fest, welche Inhalte der Dokumente in welcher Form sinnvollerweise strukturiert und codiert werden müssen. Es werden nur Daten codiert, die auch medizinisch relevant sind und die mit einem vertretbaren Umsetzungsaufwand von den IT-Systemen der Gesundheitsdiensteanbieter zur Verfügung gestellt werden können.
Um codierte und damit weiter maschinell verarbeitbare strukturierte Dokumente erzeugen zu können, müssen die IT-Systeme der meisten Gesundheitsdiensteanbieter erst umgestellt werden. Die Anpassungen können in der heterogenen IT-Landschaft der Gesundheitsdiensteanbieter unterschiedlich schnell umgesetzt werden. Zur koordinierten stufenweisen Einführung von CDA bei den verschiedenen ELGA-Gesundheitsdiensteanbietern werden bestimmte "ELGA Interoperabilitätsstufen" als Zwischenziele definiert. Seit 2018 gilt EIS Full Support als Mindeststandard für die verordneten ELGA Implementierungsleitfäden.
Neben den im Gesundheitstelematikgesetz 2012 definierten Dokumentenklassen können zukünftige Dokumentenklassen mit ihrer Struktur und ihrem Format für ELGA per Verordnung festgelegt werden. Auch für diese Dokumentenklassen gilt zumindest die unterste Interoperabilitätsstufe "EIS Basic". Wenn ein CDA Implementierungsleitfaden für die jeweilige Dokumentenklasse harmonisiert wurde, ist es möglich, Dokumente in den höheren Interoperabilitätsstufen "EIS Structured", "EIS Enhanced" und "EIS Full Support" auszutauschen.
7 Konformitätsprüfung[Bearbeiten]
Ein zu diesem Implementierungsleitfaden konformes CDA-Dokument ist zunächst ein valides CDA Release 2.0 XML-Dokument mit Header und Body. Darüber hinaus erfüllt es alle in diesem Leitfaden festgelegten "Geschäftsregeln".
Dies spiegelt ein generelles Konzept im Umgang mit Dokumenten wider: die Validierung in zwei Schritten. Im ersten Schritt stellt dies die Validierung gegen zugehörige W3C Schemas dar. Das verwendete Schema ist das geringfügig erweiterte offizielle CDA Release 2.0 Schema (siehe Schema-Prüfung). Darüber hinaus existieren eine Reihe von Schematron Regeln, die für einen zweiten Validierungsschritt genutzt werden und letztlich die Detailregelungen in diesem Leitfaden wiedergeben, sowie die Einhaltung der Geschäftsregeln (Optionalität, Kardinalität/Multiplizität, Datentypen, Wertebereiche, Abhängigkeiten) sicherstellen (siehe Schematron-Prüfung). Geschäftsregeln für Abschnitte oder Elemente werden auch technisch zu "Templates" zusammengefasst. Eine XML-Instanz, die kein valides CDA-Dokument ist oder sich nicht gegen das XSD-Schema validieren lässt, oder im Widerspruch zu den angegebenen Geschäftsregeln steht, ist kein gültiges CDA-Dokument im Sinne dieses Implementierungsleitfadens.
Dieses Kapitel behandelt die technische Konformitätsprüfung von CDA-Dokumenten gemäß diesem Dokumentleitfaden mittels Schema und Schematron.
Hinweis: Nicht alle Geschäftsregeln können mit Schema oder Schematron geprüft werden (etwa Inhalte von Multimedia-Attachments, Dokumentengröße). Zusätzliche Validierungsschritte sind gegebenenfalls notwendig, um alle Regeln überprüfen zu können.
7.1 Schema-Prüfung[Bearbeiten]
Das Absolvieren der Schema-Prüfung ist der erste Teil der technischen Konformitätsprüfung.
Eine Prüfung gegen das CDA Schema prüft die gültige "Struktur" eines CDA-Dokuments, wie beispielsweise
- ob die XML Struktur generell gültig ist
- ob alle Elemente die richtigen Namen haben
- ob alle Elemente an der richtigen Stelle platziert sind
- ob alle gemäß Schema erforderlichen Elemente vorhanden sind
Die Schema-Prüfung stellt sicher, dass es sich beim geprüften CDA-Dokument tatsächlich um eine gültige CDA-Struktur handelt.
Die Gültigkeit der "Inhalte" wird nur in Bezug auf den erforderlichen Datentyp der Elemente geprüft. Hiermit kann beispielsweise sichergestellt werden, dass ein "id"-Element (technisch) immer eine gültige ID enthält.
Das hier verwendete Schema basiert im Wesentlichen auf dem original publizierten CDA Rel. 2.0 Schema, weist aber einige Spezifika auf.
Die Mindestvoraussetzung, damit ein CDA-Dokument als "gültig" erachtet wird, ist die fehlerfreie Validierung mit dem CDA-Schema. Das maßgebliche CDA-Schema wird auf Allgemeiner Leitfaden Guide publiziert.
7.2 Schematron-Prüfung[Bearbeiten]
Im Unterschied zu einer CDA Schema Prüfung kann mittels einer Schematron-Prüfung jede beliebige Inhaltsvorschrift geprüft werden.
Das Schematron-Prüfmittel wird gemäß den Spezifikationen dieses Implementierungsleitfadens angefertigt und stellt sicher, dass das geprüfte CDA-Dokument auch jene Anforderungen erfüllt, die über die Anforderungen des CDA Schemas hinausgehen. Solche Anforderungen sind beispielsweise:
- Optionalitäten von Elementen
- Zusätzliche Pflicht-Elemente
- Eventuell konditional von anderen Inhalten abhängig
- Anforderungen an den Inhalt von Elementen
- Bestimmte Code/Wertelisten
- Anzugebende Identifikatoren (ID)
- etc.
Das Absolvieren der Schematron-Prüfung ist der zweite Teil der technischen Konformitätsprüfung und stellt sicher, dass das geprüfte Dokument die in den Implementierungsleitfäden beschriebenen "Geschäftsregeln" befolgt.
ELGA Konformität: Damit ein CDA-Dokument als vollständig "gültig" hinsichtlich der ELGA Implementierungsleitfäden erachtet wird, ist die fehlerfreie Konformitätsprüfung mit den entsprechenden Schematron-Prüfregeln vorausgesetzt. Eine vollständige Prüfung der Geschäftsregeln kann nur durch einen menschlichen Prüfer erfolgen (siehe Kapitel Abnahmeprüfung). Die ELGA GmbH kann auf Anfrage an cda@elga.gv.at eine solche Prüfung durchführen. Die maßgeblichen Schematron-Prüfmittel werden auf Allgemeiner Leitfaden Guide publiziert.
7.3 Online-Validation von CDA-Dokumenten[Bearbeiten]
Für die Prüfung von einzelnen CDA-XML-Instanzen mit dem entsprechenden Schema und Schematron-Regeln stellt die ELGA GmbH eine Webapplikation zur Verfügung. Diese ist erreichbar über https://cda-tools.elga.gv.at/online-validator/. Eine erfolgreiche Prüfung durch den Online-Validator beweist nicht automatisch die vollständige Einhaltung aller Geschäftsregeln, sondern nur die technische Konformität zu den Templates.
7.4 Hinweise zur Konformitätsprüfung[Bearbeiten]
Die Schematron-Konformitätsprüfmechanismen ("Schematron-Regeln") werden vom Modellierungstool Art-Decor automatisch aus den Templates generiert. Nicht alle erlaubten Attribute müssen in den Templates ausspezifiziert sein. Sind diese nicht explizit angeben, gelten die Vorgaben des angegebenen HL7 Datentyps bzw. den weiteren Einschränkungen im Kapitel Datentyp-Definitonen dieses Leitfadens. Diese Vorgaben MÜSSEN eingehalten werden.
Attribute oder Elemente eines CDA-Dokuments, die den Datentyp-Definitonen und den Template-Spezifikationen widersprechen oder darin nicht beschrieben wurden (also fremde Inhalte im Sinne der "closed templates" Elemente, die der "Maximum-Set" Vorschrift widersprechen), werden von den Schematron-Regeln grundsätzlich als falsch erkannt. Nicht als falsch erkannt werden Elemente und Attribute, die entsprechend den HL7 V3 Datentypen erlaubt sind, aber in den ELGA-Datentyp-Definitionen nicht enthalten oder verboten sind. Diese können nur durch die Schematron-Prüfmechanismen entdeckt werden, wenn sie im Template explizit als verboten modelliert wurden (was nicht immer der Fall ist).
Fehlertoleranz: Sollten nicht erlaubte Elemente oder Attribute in einem CDA-Dokument vorhanden sein (z.B. aufgrund von Software-Fehlern), SOLL die weiterverarbeitende Software so implementiert sein, dass dies nicht zu Fehlern in der Weiterverarbeitung der Dokumente führt.
7.5 Abnahmeprüfung für ELGA e-Befunde[Bearbeiten]
Zur Sicherstellung einer möglichst hohen Qualität von Inhalt, Struktur und Format der CDA-Dokumente ist ein Abnahmeprozess implementiert, der durch die ELGA GmbH durchgeführt wird. Vor der Produktivsetzung eines ELGA CDA-Befundes muss daher ein Prüf- und Freigabebericht durch Verantwortliche des CDA-generierenden Systems bzw. des ELGA-Bereiches bei der ELGA GmbH, Postfach cda@elga.gv.at bzw. am online service portal, beantragt werden.
Erst nach positiver Prüfung und Freigabe durch die ELGA GmbH sind die ELGA-CDA-Dokumente eines Dokumenterstellers in ELGA zugelassen.
Für eine endgültige Abnahme ist ein komplettes Set von ELGA-CDA-Dokumenten zu übermitteln:
- Je erstellendem SW-System (KIS/LIS/RIS etc.) müssen 3 Beispielbefunde je Dokumentenklasse (ärztlicher Entlassungsbrief, Befund bildgebende Diagnostik, Laborbefund) inkl. einer Befund-Folgeversion geliefert werden.
- Angabe der Art der Beispieldateien:
- Produktive anonymisierte Echtbefunde von Patienten oder
- Test-Befunde von Test-Patienten, die in der Qualität und Quantität der Befüllung produktiven Echtbefunden entsprechen.
- Die Befunde sollen eine möglichst vollständige und realitätsnahe Befüllung aller Felder aufweisen und inhaltlich so korrekt sein, dass auf ein korrektes Mapping der Inhalte durch das erstellende System geschlossen werden kann.
- Beispiele mit aufeinander folgenden Versionen eines Befundes sind anzugeben.
- Beispiele mit eingebettetem PDF sind vorzulegen (PDF/A-1a bzw. PDF/A-1b konform).
- Die Befunde müssen vor der Übermittlung erfolgreich geprüft werden:
- Darstellung mit Webbrowser und Referenz-Stylesheet.
- Prüfung mit dem von der ELGA GmbH bereitgestellten Schema- und Schematronregelset (z.B. Online-Validator).
- Prüfung auf PDF/A-1a bzw. PDF/A-1b Konformität (z.B. durch den Online-Validator oder andere Tools, wie VeraPDF.org).
- Integrationstest: Die Verwendung bzw. Darstellung der Befunde ist vor dem Echtbetrieb im GIT zu prüfen. Für jeden Dokumententyp muss die korrekte Anzeige im ELGA-Portal geprüft werden, sowohl in der Online-Ansicht als auch in der Druckansicht. (Alternative bei Verwendung der GDA-SWH-Umgebung: ELGAWebGUI auf GINA-Box)
7.6 Zertifizierung[Bearbeiten]
Das Thema "Zertifizierung" (etwa die Zertifizierung von Softwaresystemen) wird von diesem Implementierungsleitfaden nicht behandelt.
8 Datentypen[Bearbeiten]
Im folgenden Abschnitt werden nur die Datentypen beschrieben, die in ELGA CDA-Dokumenten zur Anwendung kommen.
Alle Attribute und Elemente der hier definierten Datentypen dürfen grundsätzlich in einer CDA-Instanz vorkommen, außer sie wurden explizit im gegenständlichen Template verboten. Die Elemente und Attribute der Datentypen können auch in einer strengeren Konformität und Kardinalität im Template definiert werden.
Für das vollständige Verständnis und eine kosistente Implementierung der Templates ist die genaue Kenntnis der Datentypen essenziell.
Für weiterführende Informationen wird auf den zugrundeliegenden Standard Health Level Seven Version 3 (V3) "Data Types" verwiesen. <ref name="HL7 Version 3 Standard: Data Types" />
8.1 Identifikations-Elemente[Bearbeiten]
8.1.1 id-Element II[Bearbeiten]
Identifikationselemente (II Instance Identifier) erlauben die global eindeutige Identifikation durch Verwendung von Objektidentifikatoren (kurz "OID"), gemäß dem in ISO/IEC 9834-1 normierten Mechanismus zur weltweit eindeutigen Kennzeichnung von Informationsobjekten (siehe OID-Konzept <ref name="OID">Object Identifier (OID) Konzept für das österreichische Gesundheitswesen https://www.gesundheit.gv.at/OID_Frontend/OID_Konzept_1-1-0.pdf </ref>). Die relevanten OID werden im OID-Portal für das Österreichische Gesundheitswesen<ref>OID Portal für das Österreichische Gesundheitswesen: https://www.gesundheit.gv.at/OID_Frontend/ </ref> registriert und veröffentlicht.
Identifikationselemente können im id-Element grundsätzlich auf dreierlei Arten angegeben werden:
- Methode 1: Angabe der ID in Form einer OID.
- Methode 2: Angabe der ID als @extension sowie einer OID des Namensraums, aus dem die ID stammt.
- Methode 3: Angabe einer UUID<ref name="UUID">Ein Universally Unique Identifier (UUID) ist eine 128-Bit-Zahl gemäß Standard ISO/IEC 9834-8:2014, welche zur Identifikation von Informationen in Computersystemen verwendet wird. Der Ausdruck Globally Unique Identifier (GUID) wird ebenfalls benutzt.</ref>) als @extension zur OID "2.25". Eine UUID kann als Extension der OID 2.25 aufgefasst werden (definiert als "Universally Unique Identifiers (UUIDs) generated in accordance with Recommendation ITU-T X.667 | ISO/IEC 9834-8").
8.1.1.1 Strukturbeispiele[Bearbeiten]
Methode 1:
<!-- Angabe einer OID als direkten Identifikator -->
<id root="1.2.40.0.34.99.111.0.1"
assigningAuthorityName="KH Eisenstadt" />
Methode 2:
<!—
Angabe der OID der ID-Liste in @root
sowie der eigentlichen ID in @extension
-->
<id root="1.2.40.0.34.99.111.1.1"
extension="134F989"
assigningAuthorityName="KH Eisenstadt" />
Methode 3:
<!-- Angabe einer UUID als extension zur OID "2.25" --> <id root="2.25" extension="urn:uuid:19FEE6C3-6B35-4C5B-B1CC-2B5B4001AB2" assigningAuthorityName="KH Eisenstadt" />
8.1.1.2 Spezifikation[Bearbeiten]
Bei II Elementen werden, sofern nicht anders spezifiziert, immer die folgenden Attribute angegeben.
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
|---|---|---|---|---|---|
| Id | II | ID | |||
| @root | uid | 1..1 | R | Methode 1: OID des Objekts
Methode 2: OID der ID-Liste, der die ID angehört Methode 3: Fixe OID "2.25", wenn in @extension eine UUID geführt wird Die Hexadezimalzahlen A-F der UUID MÜSSEN bei der Verwendung in HL7 CDA in Großschreibung angegeben werden | |
| @extension | st | ||||
| Konditionale Konformität: Methode 1 |
0..0 |
NP |
| ||
| @assigningAuthorityName | st | 0..1 | O | Klartext-Darstellung der die ID ausgebenden Stelle | |
8.1.1.3 Vorschriften für bereits definierte ID-Arten[Bearbeiten]
Die folgenden Unterkapitel zeigen IDs, die in CDA-Dokumenten zur Anwendung kommen können.
8.1.1.3.1 ID aus dem GDA-Index[Bearbeiten]
Die Vorgaben für IDs aus dem GDA-Index sind in der Basiskomponente "GDA-Index" beschrieben.
Informationen zum österreichischen OID-Konzept finden Sie online auf dem "OID Portal Österreich": https://www.gesundheit.gv.at/OID_Frontend/index.jsp?section=1
8.1.1.3.2 DVR-Nummer[Bearbeiten]
Die Datenverarbeitungsregister-Nummer (DVR-Nummer) des jeweiligen Gesundheitsdienstleisters kann als zusätzliches ID-Element abgebildet werden.
8.1.1.3.2.1 Spezifikation[Bearbeiten]
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
|---|---|---|---|---|---|
| Id | II | ID | |||
| @root | uid | 1..1 | R | Fester Wert: 1.2.40.0.10.2.0.2.1 | |
| @extension | st | 1..1 | R | Datenverarbeitungsregister-Nummer (DVR-Nummer) z.B.: 0000137 | |
| @assigningAuthorityName | st | 0..1 | O | Fester Wert: Datenverarbeitungsregister des Gesundheitsdienstleisters | |
8.1.1.3.3 ATU Nummer[Bearbeiten]
Die Umsatzsteueridentifikationsnummer (ATU-Nummer) des jeweiligen Gesundheitsdienstleisters kann als zusätzliches ID-Element abgebildet werden.
8.1.1.3.3.1 Spezifikation[Bearbeiten]
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
|---|---|---|---|---|---|
| Id | II | ID | |||
| @root | uid | 1..1 | R | Fester Wert: 1.2.40.0.10.2.0.3.1 | |
| @extension | st | 1..1 | R | Umsatzsteueridentifikationsnummer (ATU-Nummer) z.B.: ATU56658245 | |
| @assigningAuthorityName | st | 0..1 | O | Fester Wert: Österreichisches Finanzamt | |
8.1.1.3.4 Bankverbindung[Bearbeiten]
Die einzelnen Elemente einer Bankverbindung (IBAN, SWIFT-Adresse oder BIC) können jeweils als eigene ID-Elemente abgebildet werden. Bankleitzahl und Kontonummer werden nicht mehr unterstützt.
8.1.1.3.4.1 Spezifikation: IBAN[Bearbeiten]
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
|---|---|---|---|---|---|
| Id | II | ID | |||
| @root | uid | 1..1 | R | Fester Wert: 1.0.13616 | |
| @extension | st | 1..1 | R | IBAN z.B.: 1200052066543301 | |
| @assigningAuthorityName | st | 0..1 | O | Fester Wert: Society for Worldwide Interbank Financial Telecommunication | |
8.1.1.3.4.2 Spezifikation: SWIFT-Adresse oder BIC[Bearbeiten]
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
|---|---|---|---|---|---|
| Id | II | ID | |||
| @root | uid | 1..1 | R | Fester Wert: 1.0.9362 | |
| @extension | st | 1..1 | R | SWIFT/BIC z.B.: BKAUATWW | |
| @assigningAuthorityName | st | 0..1 | O | Fester Wert: Society for Worldwide Interbank Financial Telecommunication | |
8.2 Codierungs-Elemente[Bearbeiten]
Mit Codierungselementen können Konzepte über einen Code und der Angabe des Terminologie- bzw des Codesystems, aus dem der Code stammt, ausgedrückt werden.
8.2.1 code-Element CS CNE[Bearbeiten]
Codierte Daten bestehen in ihrer einfachsten Form aus einem Code. Das Codesystem und die Version des Codesystems wird durch den Kontext, in dem der CS-Wert auftritt, festgelegt. CS wird für codierte Attribute verwendet, die nur ein einziges HL7-definiertes Vokabular zulassen. Hinzufügungen zum Vokabular nicht nicht zulässig (CNE: coded no exceptions)
8.2.1.1 Strukturbeispiel[Bearbeiten]
<languageCode code="de-AT" />
8.2.1.2 Spezifikation[Bearbeiten]
Bei CS CNE Elementen wird nur das folgende Attribut angegeben:
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
|---|---|---|---|---|---|
| code | CS CNE | Code Element | |||
| @code | cs | 1..1 | R | Der eigentliche Code-Wert z.B. de-AT | |
8.2.2 code-Element CD (Concept Descriptor)[Bearbeiten]
Für codierte Werte wird der Datentyp CD (Concept Descriptor) oder ein davon abgeleiteter Datentyp verwendet (etwa CE "Coded with Equivalents"). Für jedes codierte Attribut innerhalb des CDA-Modells und seiner Unterstrukturen muss festgelegt werden, welche Codewerte für dieses Attribut zulässig sind. Diese Festlegung wird als "vocabulary binding" bezeichnet.
8.2.2.1 Strukturbeispiele[Bearbeiten]
8.2.2.1.1 Minimal-Variante um einen Code eindeutig darzustellen:[Bearbeiten]
<code code="E10"
codeSystem="1.2.40.0.34.5.56"/>
8.2.2.1.2 Gebräuchlichste Variante mit zusätzlichem Klartext für Code und Codesystem[Bearbeiten]
<code code="E10"
displayName="Primär insulinabhängiger Diabetes mellitus, Typ-2-Diabetes"
codeSystem="1.2.40.0.34.5.56"
codeSystemName="ICD-10 BMG 2014"/>
8.2.2.1.3 Vollständige-Variante mit direkter Angabe des Textinhalts[Bearbeiten]
<code code="E10"
displayName="Primär insulinabhängiger Diabetes mellitus, Typ-2-Diabetes"
codeSystem="1.2.40.0.34.5.56"
codeSystemName="ICD-10 BMG 2014"
codeSystemVersion="1.00">
<originalText>Diabetes mellitus Typ 2</originalText>
</code>
8.2.2.1.4 Vollständige-Variante mit Referenz in den narrativen Textbereich[Bearbeiten]
<code code="E11"
displayName="Primär insulinabhängiger Diabetes mellitus, Typ-2-Diabetes"
codeSystem="1.2.40.0.34.5.56"
codeSystemName="ICD-10 BMG 2014"
codeSystemVersion="1.00">
<originalText>
<reference value="#entldiag-1"/>
</originalText>
</code>
Für eine detaillierte Beschreibung der Abbildung von Referenzen in den narrativen Bereich siehe Spezifikation und "Verknüpfung von Text und Entry".
8.2.2.1.5 Vollständige-Variante mit Referenz in den narrativen Textbereich und Übersetzung in zwei andere Code-Systeme[Bearbeiten]
<code code="E10"
displayName="Primär insulinabhängiger Diabetes mellitus, Typ-2-Diabetes"
codeSystem="1.2.40.0.34.5.56"
codeSystemName="ICD-10 BMG 2014">
<originalText>
<reference value="#entldiag-1"/>
</originalText>
<translation code="46635009"
displayName="Diabetes mellitus type I"
codeSystem="2.16.840.1.113883.6.96"
codeSystemName="SNOMED CT">
<originalText>
<reference value="#entldiag-1"/>
</originalText>
</translation>
<translation code="xyz"
displayName="Diabetes mellitus juvenilis"
codeSystem="9.8.7.6.5.4.3.2.1"
codeSystemName="AnderesCodesystem">
<originalText>
<reference value="#entldiag-1"/>
</originalText>
</translation>
</code>
8.2.2.2 Spezifikation[Bearbeiten]
Bei CD CWE und CE CWE Elementen werden - sofern nicht anders spezifiziert - immer die folgenden Attribute angegeben:
| Element/Attribut | DT | Kard | Konf | Beschreibung | |||
|---|---|---|---|---|---|---|---|
| code | CE CWE |
Code Element | |||||
| @code | cs | 1..1 | R | Der eigentliche Code-Wert z.B. E10 | |||
| @displayName | st | 0..1 | R |
Die Klartext-Darstellung des Code-Werts, wie vom originalen Codesystem (in der entsprechenden offiziellen Sprachvariante) vorgesehen. | |||
| @codeSystem | uid | 1..1 | R | Die Identifikation der Codeliste z.B. 1.2.40.0.34.5.56 bzw. die aktuell gültige OID der Codeliste | |||
| @codeSystemName | st | 0..1 | R | Der Klartext-Darstellung der Codeliste z.B. ICD-10 BMG 2014 bzw. die aktuell gültige Version | |||
| @codeSystemVersion | st | 0..1 | O | Die Versionsnummer der Codeliste z.B. 1.00 | |||
| @sdtc:valueSet | uid | 0..1 | O | Identifikation des Value Sets, an das der Code entsprechend der Leitfadenspezifikation gebunden ist
z.B. 1.2.40.0.34.10.34 | |||
| @sdtc:valueSetVersion | st | 0..1 | O | Die Versionsnummer des Value Sets, das zum Zeitpunkt der Codierung genutzt wurde. Formatvorgabe: YYYY-MM-DD
z.B. 2020-03-19 | |||
| originalText | ED | 0..1 | O | OriginalText ist ein Element, dass die sprachliche Repräsentation eines Codes in der originalen Sprache des Dokuments enthält. Der Inhalt dieses Elements darf für die menschenlesbare Anzeige des Codes verwendet werden. Entweder direkt angegeben als "String" oder indirekt als "Referenz" auf eine Textstelle im narrativen Bereich. Im Falle der direkten Angabe als "String", z.B. Diabetes mellitus Typ 1 | |||
| reference | TEL | 0..1 | C | Referenz Element | |||
| Konditionale Konformität: Wenn indirekte Angabe als "Referenz" Wenn direkte Angabe |
1..1 0..0 |
M NP |
|||||
| @value | url | 1..1 | R | #{generierter_ref_string}-{generierteID} z.B.: #entldiag-1, verweist auf die Textstelle im narrativen Block:<td id="entldiag-1">Diabetes mellitus Typ 1</td> | |||
| qualifier | CR CWE |
0..* | O | Gibt zusätzliche Codes an, die die Genauigkeit des Primärcodes erhöhen (Postkoordination). Pro Qualifier werden jeweils ein name und ein value-Element angegeben, wobei beide Elemente mindestens die Attribute code und codesystem enthalten.
Dieses Attribut ist nur im CD Datentyp erlaubt und bei CE VERBOTEN. | |||
| translation | CD CWE |
0..* | O | Beliebig viele optionale Übersetzungen des Codes in andere Codesysteme. | |||
| ips:designation | CD ST |
0..* | O | Falls Mehrsprachigkeit in einem Dokument unterstützt wird, muss das Attribut ips:designation für die Übersetzungen in die zusätzlichen Sprachen verwendet werden. Das Attribut @language ist dabei verpflichtend anzugeben. ips:designation kann auch die originale Sprache des Dokuments enthalten.
Beispiel: <ips:designation language="en-US">Typhoid fever (disorder)</ips:designation> | |||
8.3 Zeit-Elemente[Bearbeiten]
Angaben von Zeiten sind in HL7 CDA auf vielerlei Arten möglich. Es können Zeitpunkte, Zeitintervalle bestehend aus Beginn- und Endzeitpunkt, Zeitintervalle bestehend aus Beginnzeitpunkt und Dauer und vielerlei mehr Varianten abgebildet werden.
Damit nicht alle beliebigen Varianten implementiert werden müssen, werden die Varianten über den Leitfaden stark eingeschränkt. Weitere Spezifizierungen von Zeit-Elementen können von den speziellen Implementierungsleitfäden vorgenommen werden, z.B. spezifiziert der Implementierungsleitfaden e-Medikation den Datentyp GTS (General Timing Specification) für komplexe Zeitangaben mit Anfang, Ende und Häufigkeit bei den Einnahmeregeln für Medikamente.
Allgemein gilt, dass nicht angegebene Datums- und Zeitanteile (also z.B. fehlende Sekunden) mit 0 (Null) angenommen werden. D.h. 201908071633 entspricht 20190807163300.
Normale Angabe von Datum und Zeit
1) Zeitpunkte: Die häufigsten Datums- und Zeitangaben werden über den Datentyp TS.AT.TZ <ref>Datentyp TS.AT.TZ https://art-decor.org/mediawiki/index.php?title=DTr1_TS.AT.TZ</ref> zusammengefasst und im Folgenden unter Einfaches Zeitelement TS beschrieben.
Hier kann der Wert für einen Zeitpunkt auf drei Arten angegeben werden:
- als taggenaues Datum
- als Datum mit sekundengenauer Uhrzeit und Zeitzone
- als ungenaue Zeitangabe (etwa nur Jahr oder Monat) - erfordert die Spezifikation als TS.AT.VAR<ref>Datentyp TS.AT.VAR https://art-decor.org/mediawiki/index.php?title=DTr1_TS.AT.TZ</ref>
2) Zeitintervalle: Bestehen aus Anfangs- und Endpunkt, die wiederum als Zeitpunkt wie oben angegeben werden. Dieser Datentyp wird als Intervall-Zeitelement IVL_TS im Anschluss spezifiziert.
8.3.1 Zeitpunkt: Einfaches Zeitelement TS[Bearbeiten]
8.3.1.1 Nur Datum[Bearbeiten]
Wird ein Zeitpunkt als Datum (ohne Zeit) angegeben, MUSS dies in folgendem Format erfolgen: YYYYMMDD
Bedeutung:
- Jahr 4-stellig +
- Monat 2-stellig +
- Tag 2-stellig
8.3.1.2 Strukturbeispiel[Bearbeiten]
<effectiveTime value="20081224"/> <!-- Datum 24.12.2008 -->
8.3.1.2.1 Datum, Zeit und Zeitzone[Bearbeiten]
Wird ein Zeitpunkt als Datum mit Zeit angegeben, MUSS dies in folgendem Format erfolgen: YYYYMMDDhhmmss[+/-]HHMM
Bedeutung:
- Jahr 4-stellig +
- Monat 2-stellig +
- Tag 2-stellig
- Stunde 2-stellig (24 Stunden Format)
- Minute 2-stellig
- Sekunde 2-stellig
- + oder -
- Zeitzonenverschiebung Stunde 2-stellig
- Zeitzonenverschiebung Minute 2-stellig
Wird in einem Zeitelement zusätzlich zum Datum eine Zeit angegeben, MUSS die Zeitzone verpflichtend angegeben werden!
Die angegebene Zeitzone MUSS die aktuelle Sommerzeitregelung inkludieren.
8.3.1.3 Strukturbeispiele[Bearbeiten]
a) Winterzeit, Österreich (MEZ)
<effectiveTime value="20081224150000+0100"/> <!-- Datum 24.12.2008, um 15:00 Uhr in Europa/Wien (bei Winterzeit) -->
b) Sommerzeit, Österreich (MESZ)
<effectiveTime value="20080824150000+0200"/> <!-- Datum 24.08.2008, um 15:00 Uhr in Europa/Wien (bei Sommerzeit) -->
8.3.1.4 Spezifikation[Bearbeiten]
Bei Zeitpunkten werden, sofern nicht anders spezifiziert, immer die folgenden Unterelemente/Attribute angegeben:
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
|---|---|---|---|---|---|
| effectiveTime | TS.AT.TZ | ||||
| @value | ts | 1..1 | R | Zeitpunkt (bei Zeitangabe mit Zeitzone) z.B. 20131224180000+0100 | |
8.3.2 Minimale Datumsangabe: TS.DATE[Bearbeiten]
Eine minimale Datumsangabe umfasst die möglichen Formate: YYYY, YYYYMM, YYYYMMDD. Dies wird mit dem Datentyp TS.DATE <ref>TS.DATE https://art-decor.org/mediawiki/index.php?title=DTr1_TS.DATE </ref> angezeigt.
8.3.2.1 Strukturbeispiel[Bearbeiten]
Datum: "Juni 2008"
<effectiveTime value="200806"/>
8.3.2.2 Spezifikation[Bearbeiten]
Beim Datum TS.DATE werden, sofern nicht anders spezifiziert, immer die folgenden Unterelemente/Attribute angegeben:
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
|---|---|---|---|---|---|
| effectiveTime | TS.DATE | ||||
| @value | ts | 1..1 | R | Datum im Format YYYY, YYYYMM, YYYYMMDD z.B. 20131224, 201312, 2013 | |
8.3.3 Zeitintervall: Intervall-Zeitelement IVL_TS[Bearbeiten]
8.3.3.1 Strukturbeispiel[Bearbeiten]
<effectiveTime> <low value="..."/> <!-- Zeitpunkt von --> <high value="..."/> <!-- Zeitpunkt bis --> </effectiveTime>
8.3.3.2 Spezifikation[Bearbeiten]
Bei Zeitintervallen werden, sofern nicht anders spezifiziert, immer die folgenden Unterelemente/Attribute angegeben:
| Element/Attribut | DT | Kard | Konf | Beschreibung | ||
|---|---|---|---|---|---|---|
| effectiveTime | IVL_TS | Zeitintervall | ||||
| low | TS.AT.TZ | 1..1 | R | Beginn des Intervalls Zugelassene nullFlavor: UNK | ||
| @value | ts | 1..1 | R | Zeitpunkt des Beginns des Intervalls | ||
| high | TS.AT.TZ | 1..1 | R | Ende des Intervalls Zugelassene nullFlavor: UNK | ||
| @value | ts | 1..1 | R | Zeitpunkt des Endes des Intervalls | ||
Ein Datum, das mit yyyymmdd angegeben wurde, wird gemäß Standard HL7 CDA Rel.2 interpretiert als yyyymmdd000000 – also der Tag um 0:00:00 Uhr. Wenn also als Zeitraum z.B.: der ganze 1.Dezember 2013 angegeben werden soll, MUSS das so erfolgen:
<low value="20131201"/> <high value="20131202"/>
Für mehr Klarheit empfiehlt sich daher die zusätzliche Angabe der Zeit mit Zeitzone:
<low value="20131201000000+0100"/> <high value="20131201235959+0100"/>
8.3.4 Periodisches-Zeitintervall PIVL_TS[Bearbeiten]
Ein periodisch wiederkehrendes Zeitintervall. Periodische Intervalle tragen die Elemente phase und period. phase gibt den "Intervall-Prototypen" an, der jede period wiederholt wird.
8.3.4.1 Spezifikation[Bearbeiten]
Bei PIVL_TS Elementen können, sofern nicht durch einen speziellen Implementierungsleitfaden eingeschränkt, immer die folgenden Attribute angegeben werden:
| Element/Attribut | DT | Kard | Konf | Beschreibung |
| @operator | cs | 0..1 | R | Wenn ein Element vom Typ PIVL_TS Teil eines Sets ist (d.h. child von einem parent-Element mit einem Set-Datentyp basierend auf SXCM) spezifiziert dieser Code die Set-Operation. Gängige Set-Operationen sind "I" für inkludieren, "E" für ausschließen und "A" für die Schnittmenge. |
| @alignment | cs | 0..1 | R | Gibt an, in welcher Art und Weise die Wiederholung in phase einem bestimmten Kalenderzyklus zugeordnet ist. Gängige Zyklen sind "DW" für einen bestimmten Tag in der Woche oder "MY" für einen bestimmten Monat im Jahr. |
| @institutionSpecified | bl | 0..1 | R | Gibt an, ob der Start des periodischen Zeitintervalls vom durchführenden bestimmt wird. |
| phase | IVL_TS | 0..1 | O | Das Zeitintervall, das sich periodisch wiederholt. |
| period | PQ | 0..1 | O | Zeitliche Frequenz, zu der das Zeitintervall in phase auftritt. |
8.3.4.2 Strukturbeispiele[Bearbeiten]
<!-- pro Tag --> <effectiveTime xsi:type='PIVL_TS' institutionSpecified='true'> <period value='1' unit='d'/> </effectiveTime> <!-- 2x täglich, für 20 Minuten --> <effectiveTime xsi:type='PIVL_TS'> <phase> <width value='20' unit='min'/> </phase> <period value='12' unit='h'/> </effectiveTime> <!-- Jede Woche am Mittwoch, "20191113" ist ein Mittwoch --> <effectiveTime xsi:type='PIVL_TS' alignment='DW'> <phase value='20191113'/> <period value='1' unit='wk'/> </effectiveTime>
8.3.5 Periodisches-Zeitintervall EIVL_TS[Bearbeiten]
Ein periodisch wiederkehrendes Zeitintervall, bei dem das Wiederauftreten auf einer bestimmten Aktivität des täglichen Lebens oder einem Ereignis basiert, das zwar zeitbezogen, aber nicht vollständig durch eine Zeitangabe bestimmbar ist (z.B. mittags).
8.3.5.1 Spezifikation[Bearbeiten]
Bei EIVL_TS Elementen können, sofern nicht durch einen speziellen Implementierungsleitfaden eingeschränkt, immer die folgenden Attribute angegeben werden:
| Element/Attribut | DT | Kard | Konf | Beschreibung |
| @operator | cs | 0..1 | R | Wenn ein Element vom Typ EIVL_TS Teil eines Sets ist (d.h. child von einem parent-Element mit einem Set-Datentyp basierend auf SXCM) spezifiziert dieser Code die Set-Operation. Gängige Set-Operationen sind "I" für inkludieren, "E" für ausschließen und "A" für die Schnittmenge. |
| event | CS | 0..1 | O | Code für eine gebräuchliche periodische Aktivität des täglichen Lebens, das den Start des Intervalls darstellt. Gängige Codes sind "ACM" für morgens, "ACD" für mittags und "ACV" für abends aus dem HL7 v3 Codesystem "TimingEvent" (2.16.840.1.113883.5.139).
Das jeweils gültige Value Set ist in einem speziellen Implementierungsleitfaden festgelegt (wie z.B. für die e-Medikation das Value Set "ELGA_Einnahmezeitpunkte"). |
| offset | IVL_TS | 0..1 | O | Zur Angabe einer Zeitspanne als Zeitversatz vor oder nach dem Eintreten des Ereignisses in event, z.B. 1 Stunde vor dem Frühstück |
8.3.5.2 Strukturbeispiele[Bearbeiten]
<!-- morgens -->
<effectiveTime xsi:type='EIVL_TS'>
<event code='ACM'/>
<offset value="0" unit="s"/>
</effectiveTime>
<!-- abends -->
<effectiveTime xsi:type='EIVL_TS'>
<event code='ACV'/>
<offset value="0" unit="s"/>
</effectiveTime>
<!-- 1 Stunde vor dem Mittagessen -->
<effectiveTime xsi:type='EIVL_TS'>
<event code='ACD'/>
<offset>
<low value="1" unit="h"/>
</offset>
</effectiveTime>
8.3.6 Strukturierung von Zeitelementen SXPR_TS[Bearbeiten]
Ein Element von diesem Datentyp repräsentiert ein Set von Komponenten zu Zeitangaben, das als eine Einheit zu betrachten ist.
8.3.6.1 Spezifikation[Bearbeiten]
Bei SXPR_TS Elementen können, sofern nicht durch einen speziellen Implementierungsleitfaden eingeschränkt, immer die folgenden Attribute angegeben werden:
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
| @operator | cs | 0..1 | R | Wenn ein Element vom Typ SXPR_TS teil eines Sets ist (d.h. child von einem parent-Element mit einem Set-Datentyp basierend auf SXCM) spezifiziert dieser Code die Set-Operation. Gängige Set-Operationen sind "I" für inkludieren, "E" für ausschließen und "A" für die Schnittmenge. | |
| comp | IVL_TS,
PIVL_TS, EIVL_TS, SXPR_TS |
2..* | R | Komponente zur Strukturierung von Zeitangaben entsprechend dem jeweils festgelegten Datentyp. | |
8.3.6.2 Strukturbeispiele[Bearbeiten]
<!-- 1 Zeitangabe bestehend aus 2 Zeit-Komponenten, jeden Dienstag und Donnerstag pro Woche --> <effectiveTime xsi:type='SXPR_TS'> <!-- Jeden Dienstag --> <comp xsi:type='PIVL_TS' alignment='DW'> <phase value="20131001"/> <!-- Der 1.Okt 2013 ist ein Dienstag --> <period value="1" unit="wk"/> </comp> <!-- Jeden Donnerstag --> <comp xsi:type='PIVL_TS' alignment='DW'> <phase value="20131003"/> <!-- Der 3.Okt 2013 ist ein Donnerstag --> <period value="1" unit="wk"/> </comp> </effectiveTime> <!-- 1 Zeitangabe bestehend aus 2 Zeit-Komponenten, morgens jeden Montag, der 21.Dezember ist ein Montag --><effectiveTime xsi:type='SXPR_TS'> <comp xsi:type='EIVL_TS'> <event code='ACM'/> <offset value="0" unit="s"/> </comp> <comp xsi:type='PIVL_TS'> <phase value="20151221"/> <period value='1' unit='wk'/> </comp> </effectiveTime>
8.4 Kontaktdaten-Elemente[Bearbeiten]
8.4.1 telecom-Element TEL[Bearbeiten]
Ein telecom Kommunikations-Element dient zur Angabe von Kontaktdaten zu einem Personen- oder Organisationselement.
8.4.1.1 Strukturbeispiele[Bearbeiten]
8.4.1.1.1 Beispiele für Präfixe in TEL Elementen[Bearbeiten]
<telecom value="tel:+43.1.40400"/> <telecom value="fax:(02236)83.12323-12"/> <telecom value="mailto:office@organisation.at"/> <telecom value="http://www.organisation.at"/>
8.4.1.1.2 Beispiel für die Angabe einer Mobilnummer[Bearbeiten]
<telecom use="MC" value="tel:+43.660.1234567"/>
8.4.1.2 Spezifikation[Bearbeiten]
Bei TEL Elementen werden, sofern nicht anders spezifiziert, immer die folgenden Unterelemente/Attribute angegeben:
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
|---|---|---|---|---|---|
| telecom | TEL | Kontakt-Element | |||
| @value | url | 1..1 | R | Die Kontaktadresse (Telefonnummer, Email, etc.) Formatkonvention siehe "telecom – Format Konventionen für Telekom-Daten" Bsp: tel:+43.1.1234567 Zulässige Werteliste für telecom Präfixe gemäß Value-Set "ELGA_URLScheme" | |
| @use | cs | 0..1 | O | Bedeutung des angegebenen Kontakts (Heim, Arbeitsplatz, …) Bsp: WP Zulässige Werte gemäß Value-Set "ELGA_TelecomAddressUse" | |
8.4.1.2.1 telecom – Format Konventionen für Telekom-Daten[Bearbeiten]
Festlegungen für das @value Attribut des telecom-Elements:
- MUSS das URI Schema "tel:", "mailto:", etc. aufweisen
- Zulässige Werteliste für telecom Präfixe gemäß Value-Set "ELGA_URLScheme"
- Für Telefonnummern:
- … MUSS im Falle von internationalen Telefonnummern mit einem "+" beginnen
- … DARF nur Ziffernzeichen 0 bis 9 nutzen sowie als visuelle Separatorzeichen nur Bindestrich –, Punkte . oder Klammern () verwenden
- … Leerzeichen sind in Telefonnummern NICHT ERLAUBT
8.5 Namen-Elemente[Bearbeiten]
8.5.1 Namen-Elemente von Personen PN[Bearbeiten]
Personen-Namen werden über das Element name abgebildet.
Die Bedeutung des Namen-Elements KANN mit dem Attribut @use angegeben werden. Fehlt das Attribut, wird der Name als "rechtlicher Name" (Realname bzw. bürgerlicher Name) angenommen (entsprechend @use="L", legal name).
Werden mehrere Namen angegeben, MUSS die Bedeutung für jedes Namen-Element über das Attribut @use angegeben werden, wobei nur EIN rechtlicher Name angegeben werden DARF.
8.5.1.1 Granularitätsstufe 1: Unstrukturierte Angabe[Bearbeiten]
In Granularitätsstufe 1 wird der Personen-Name unstrukturiert angegeben. Die einzelnen Elemente des Namens (Vorname, Nachname) werden nicht getrennt.
8.5.1.1.1 Strukturbeispiele[Bearbeiten]
Beispiele für name-Elemente in Granularitätsstufe 1:
<name>Dr. Herbert Mustermann</name>
<name use="A">Dr. Kurt Ostbahn </name>
8.5.1.1.2 Spezifikation[Bearbeiten]
Bei name-Elementen in dieser Granularitätsstufe werden, sofern nicht anders spezifiziert, immer die folgenden Elemente angegeben:
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
|---|---|---|---|---|---|
| name | PN | Namen-Element (Person) | |||
| @use | cs | 0..1 | O | Die genaue Bedeutung des angegebenen Namens, beispielsweise, dass der angegebene Personen-Name ein "Künstlername" ist. Weitere Bsp: L (rechtlicher Name), A (Künstlername), R (Ordensname) Zulässige Werte gemäß Value-Set "ELGA_EntityNameUse" Wird kein @use Attribut angegeben, gilt der Name als rechtlicher Name ("L"). | |
Spezifiziert durch folgende Templates:
8.5.1.2 Granularitätsstufe 2: Strukturierte Angabe[Bearbeiten]
In Granularitätsstufe 2 wird der Personen-Name strukturiert angegeben. Die einzelnen Elemente des Namens (mindesten der Vorname und Nachname) werden getrennt angegeben.
8.5.1.2.1 Strukturbeispiel[Bearbeiten]
Beispiel für ein name-Element in Granularitätsstufe 2:
<name> <prefix qualifier="PR">OMedR</prefix> <prefix qualifier="AC">Dr.</prefix> <given>Sissi</given> <family>Österreich</family> <family qualifier="BR">Habsburg</family> <suffix qualifier="AC">MSc</suffix> </name>
8.5.1.2.2 Spezifikation[Bearbeiten]
Bei name-Elementen in dieser Granularitätsstufe werden, sofern nicht anders spezifiziert, immer die folgenden Elemente angegeben:
| Element/Attribut | DT | Kard | Konf | Beschreibung | ||
|---|---|---|---|---|---|---|
| name | PN | Namen-Element (Person) | ||||
| @use | cs | 0..1 | O | Die genaue Bedeutung des angegebenen Namens, beispielsweise, dass der angegebene Personen-Name ein "Künstlername" ist. Bsp: L (rechtlicher Name), A (Künstlername), R (Ordensname) Zulässige Werte gemäß Value-Set "ELGA_EntityNameUse" | ||
| prefix | en.prefix | 0..* | O | Beliebig viele Präfixe zum Namen z.B. Akademische Titel, Adelstitel Achtung: Die Angabe der Anrede ("Frau", "Herr"), ist im CDA nicht vorgesehen!
| ||
| @qualifier | cs | 0..1 | O | Die genaue Bedeutung eines prefix-Elements, beispielsweise, dass das angegebene Präfix einen akademischen Titel darstellt. z.B.: AC ("Akademischer Titel") Zulässige Werte gemäß Value-Set "ELGA_EntityNamePartQualifier" | ||
| given | en.given | 1..* | M | Mindestens ein Vorname | ||
| @qualifier | cs | 0..1 | O | Die genaue Bedeutung eines given-Elements, beispielsweise, dass das angegebene Element eine Initial (z.B. middle initial) bezeichnet. z.B.: IN ("Initial") Zulässige Werte gemäß Value-Set "ELGA_EntityNamePartQualifier" | ||
| family | en.family | 1..* | M | Mindestens ein Hauptname (Nachname) | ||
| @qualifier | cs | 0..1 | O | Die genaue Bedeutung eines family-Elements, beispielsweise, dass das angegebene Element einen Geburtsnamen bezeichnet. z.B.: BR ("Geburtsname") Zulässige Werte gemäß Value-Set "ELGA_EntityNamePartQualifier" | ||
| suffix | en.suffix | 0..* | O | Beliebig viele Suffixe zum Namen z.B. Akademische Titel, Adelstitel | ||
| @qualifier | cs | 0..1 | O | Die genaue Bedeutung eines suffix-Elements, beispielsweise, dass das angegebene Suffix einen akademischen Titel darstellt. z.B.: AC ("Akademischer Titel") Zulässige Werte gemäß Value-Set "ELGA_EntityNamePartQualifier" | ||
Die korrekte Reihenfolge der einzelnen Namenselemente ist wichtig. Als Richtlinie gilt, dass diese in der "natürlichen" Reihenfolge der Benutzung des Namens angegeben werden. Das ist besonders in den folgenden Fällen relevant:
- Präfixe (prefix) MÜSSEN immer vor dem Namen stehen, zu dem sie gehören.
- Vornamen (given) MÜSSEN immer in der offiziellen (gesetzlichen) Sequenz stehen.
- Nachnamen (family) und ein eventuelles Trennzeichen (meistens "-") MÜSSEN in der offiziellen Sequenz stehen, abhängig von der Wahl bei der Eheschließung.
- Suffixe (suffix) MÜSSEN immer hinter dem Namen stehen, zu dem sie gehören.
Für die Namenselemente kann zur näheren Bestimmung ein Qualifier angegeben werden (aus dem Value Set "ELGA_EntityNamePartQualifier"), v.a. für Prefix/Suffix.
Es gibt auch nicht näher bestimmte Prefixe/Suffixe, z.B. trifft das für die Angabe von "Junior" oder "Senior" bzw "Jun."/"Sen" oder "Jr."/"Sr" zu.
<name> <given>Herbert</given> <family>Mustermann</family> <suffix>Sen.</suffix> </name>
Spezifiziert durch folgende Templates:
8.5.2 Namen-Elemente von Organisationen ON[Bearbeiten]
Organisations-Namen werden über das Element name abgebildet.
Dieser Implementierungsleitfaden lässt nur die unstrukturierte Angabe des Organisationsnamens zu. Die Verwendung des @qualifier Attributs beim name-Element ist nicht gestattet.
8.5.2.1 Strukturbeispiel[Bearbeiten]
Beispiel für die Angabe eines Organisationsnamens:
<name>Krankenhaus Wels</name>
8.5.2.2 Spezifikation[Bearbeiten]
| Element/Attribut | DT | Kard | Konf | Beschreibung |
|---|---|---|---|---|
| name | ON | Name der Organisation |
Spezifiziert durch folgendes Template:
8.6 Adress-Elemente[Bearbeiten]
Adressen von Personen und Organisationen werden über das Element addr abgebildet. Das Adress-Element kann in verschiedenen Kontexten mit unterschiedlicher Detailgenauigkeit vorkommen. Daher werden drei Granularitätsstufen definiert, auf die je nach Anwendung entsprechend verwiesen wird.
Sind keine Adressdaten vorhanden, kann das Element entweder wegelassen werden oder mit nullFlavor angegeben werden – je nachdem wie das Adress-Element im Kontext spezifiziert wurde.
8.6.1 Granularitätsstufe 1: Unstrukturierte Angabe[Bearbeiten]
In Granularitätsstufe 1 wird die Adresse unstrukturiert angegeben. Die einzelnen Elemente der Adresse (Straße, PLZ, Ort, …) werden nicht getrennt.
Hinweis: Diese Granularitätsstufe ist ausdrücklich "nicht empfohlen" und SOLL nur in EIS Basic angewandt werden, wenn eine feinere Granularität nicht möglich ist.
Bei EIS Enhanced und EIS Full Support MUSS die Granularitätsstufe 2 oder 3 angegeben werden.
8.6.1.1 Strukturbeispiel[Bearbeiten]
Beispiel für ein addr-Element in Granularitätsstufe 1:
<addr use="HP">Musterstraße 13a, 1220 Wien, Österreich</addr>
8.6.1.2 Spezifikation[Bearbeiten]
Bei addr-Elementen in dieser Granularitätsstufe werden, sofern nicht anders spezifiziert, immer die folgenden Elemente angegeben:
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
|---|---|---|---|---|---|
| addr | AD | Namen-Element | |||
| @use | cs | 0..1 | O | Die genaue Bedeutung der angegebenen Adresse, beispielsweise, dass die angegebene Adresse die Wohn-Adresse ist, z.B. HP ("Home primary") Zulässige Werte gemäß Value-Set "ELGA_AddressUse" Wird kein @use Attribut angegeben, gilt bei Personen die Adresse als "Wohnadresse" ("H") und bei Organisationen als Büroadresse ("WP"). | |
8.6.2 Granularitätsstufe 2: Strukturierte Angabe, Stufe 1[Bearbeiten]
In Granularitätsstufe 2 wird die Adresse strukturiert angegeben, wobei aber Straße und Hausnummer noch zusammen angegeben werden.
8.6.2.1 Strukturbeispiel[Bearbeiten]
Beispiel für ein addr-Element in Granularitätsstufe 2:
<addr> <streetAddressLine>Musterstraße 11a/2/1</streetAddressLine> <postalCode>7000</postalCode> <city>Eisenstadt</city> <state>Burgenland</state> <country>AUT</country> <additionalLocator>Station A, Zimmer 9</additionalLocator> </addr>
8.6.2.2 Spezifikation[Bearbeiten]
Bei addr-Elementen in dieser Granularitätsstufe werden, sofern nicht anders spezifiziert, immer die folgenden Elemente angegeben:
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
|---|---|---|---|---|---|
| addr | AD | Namen-Element | |||
| @use | cs | 0..1 | O | Die genaue Bedeutung der angegebenen Adresse, beispielsweise, dass die angegebene Adresse die Wohn-Adresse ist, z.B. HP ("Home primary") Zulässige Werte gemäß Value-Set "ELGA_AddressUse" Wird kein @use Attribut angegeben, gilt bei Personen die Adresse als "Wohnadresse" ("H") und bei Organisationen als Büroadresse ("WP"). | |
| streetAddressLine | ADXP | 1..1 | M | Straße mit Hausnummer Bsp: Musterstraße 11a/2/1 | |
| postalCode | ADXP | 1..1 | M | Postleitzahl | |
| city | ADXP | 1..1 | M | Stadt | |
| state | ADXP | 0..1 | O | Bundesland | |
| country | ADXP | 1..1 | M | Staat Es wird EMPFOHLEN, den Staat im ISO 3 Ländercode (ISO-3166-1 Alpha 3) anzugeben, z.B. "AUT" für Österreich, "DEU" für Deutschland… | |
| additionalLocator | ADXP | 0..1 | O | Zusätzliche Addressinformationen z.B.: Station, Zimmernummer im Altersheim | |
8.6.3 Granularitätsstufe 3: Strukturierte Angabe, Stufe 2[Bearbeiten]
In Granularitätsstufe 3 wird die Adresse maximal strukturiert angegeben (Straße und Hausnummer getrennt).
8.6.3.1 Strukturbeispiel[Bearbeiten]
Beispiel für ein addr-Element in Granularitätsstufe 3:
<addr> <streetName>Musterstraße</streetName> <houseNumber>11a/2/1</houseNumber> <postalCode>7000</postalCode> <city>Eisenstadt</city> <state>Burgenland</state> <country>AUT</country> <additionalLocator>Station A, Zimmer 9</additionalLocator> </addr>
8.6.3.2 Spezifikation[Bearbeiten]
Bei addr-Elementen in dieser Granularitätsstufe werden, sofern nicht anders spezifiziert, immer die folgenden Elemente angegeben:
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
|---|---|---|---|---|---|
| addr | AD | Namen-Element | |||
| @use | cs | 0..1 | O | Die genaue Bedeutung der angegebenen Adresse, beispielsweise, dass die angegebene Adresse die Wohn-Adresse ist, z.B. HP ("Home primary") Zulässige Werte gemäß Value-Set "ELGA_AddressUse" Wird kein @use Attribut angegeben, gilt bei Personen die Adresse als "Wohnadresse" ("H") und bei Organisationen als Büroadresse ("WP"). | |
| streetName | ADXP | 1..1 | M | Straße mit Hausnummer Bsp: Musterstraße | |
| houseNumber | ADXP | 1..1 | M | Hausnummer Bsp: 11a/2/1 | |
| postalCode | ADXP | 1..1 | M | Postleitzahl | |
| city | ADXP | 1..1 | M | Stadt | |
| state | ADXP | 0..1 | R | Bundesland | |
| country | ADXP | 1..1 | M | Staat Es wird EMPFOHLEN, den Staat im ISO 3 Ländercode (ISO-3166-1 Alpha 3) anzugeben, z.B. "AUT" für Österreich, "DEU" für Deutschland… | |
| additionalLocator | ADXP | 0..1 | O | Zusätzliche Addressinformationen z.B.: Station, Zimmernummer im Altersheim | |
Adressangaben werden durch folgendes Templates spezifiziert:
8.7 Messwert-Elemente[Bearbeiten]
Die maschinenlesbare Angabe von Messwerten wie des Ergebnisses einer Laboruntersuchung oder einer Vitalparameter-Messung erfolgt über ein value-Element. Die Codierung erfolgt gemäß dem Datentyp, welcher durch das xsi:type-Attribut ausgedrückt wird, für möglichen Datentypen gibt es eine fixe Liste.
Numerische Ergebnisse werden in der Regel als "physical quantity" PQ dargestellt, was die Angabe einer Einheit in UCUM-Schreibweise erforderlich macht. Es MUSS die "case sensitive" Variante (c/s) der maschinenlesbaren Form des UCUM verwendet werden. Als Dezimaltrennzeichen MUSS im maschinenlesbaren und menschenlesbaren Teil (section.text) ein Punkt (".") verwendet werden. Die bevorzugte Einheit für jede Analyse wird in den einzelnen dazugehörigen ELGA Value Sets vorgeschlagen, jeweils in der in der maschinenlesbaren Form und in der "print" Variante für die Darstellung in section.text.
Exponent-Schreibweise
Dabei MUSS bei einer Potenz der Exponent der maschinenlesbaren Einheiten mit "*" (z.B.: 10*9 für eine Milliarde) angegeben werden (Dies resultiert aus der Reservierung des Symbols "^" als Trennzeichen in HL7 Nachrichten). Hingegen MUSS weiterhin für den Exponenten der menschenlesbaren Einheiten die "print" Variante mit "^" angegeben werden (z.B.: 10^9 für eine Milliarde).
Einheitenpräfixe
Es wird EMPFOHLEN, anstelle von Einheitenpräfixen ("Giga", "Mega", "Milli", "Mikro" etc.) eine Potenzschreibweise zu wählen, vor allem, wenn die Groß/Klein-Schreibung eine Rolle spielt und Verwechslungen möglich sind (z.B. "G/L"=Giga pro Liter vs. "g/L"=Gramm/Liter). Also '10^6 ' statt 'M' (Mega), '10^9 ' statt 'G ' (Giga) usw.
8.7.1 Strukturbeispiele[Bearbeiten]
Die Dokumentation eines numerischen Ergebniswertes erfolgt in diesem Fall als Attribut.
<value xsi:type="PQ" value="49.7" unit="%"/>
Die Codierung von textuellen Ergebnissen erfolgt in der Regel durch den "ST" Datentyp. Die Angabe des Ergebnisses erfolgt hier als Wert des Elementes.
<value xsi:type="ST">strohgelb</value>
Im narrativen Block MUSS derselbe Text wie im Entry dargestellt werden.
Auch für dimensionslose Einheiten wird in UCUM häufig eine Einheit angegeben, wie z.B. "[ph]" für den pH-Wert. Wenn keine UCUM-Einheit vorgeschlagen ist, können dimensionslose Einheiten auch mit @unit="1" dargestellt werden, hier für INR:
<value xsi:type="PQ" value="1.1" unit="1"/>
Für Verhältnisangaben, wie sie etwa für Titer verwendet werden (z.B. "1:128") steht der Datentyp RTO (Ratio) zur Verfügung. Ein Anwendungsbeispiel:
<value xsi:type="RTO"> <numerator value="1" xsi:type="INT"/> <denominator value="128" xsi:type="INT"/> </value>
Intervalle können mit dem Datentyp IVL angegeben werden, z.B. "20-30 mg/L":
<value xsi:type="IVL_PQ" > <low value="20" unit="mg/dl" inclusive="true"/> <high value="30" unit="mg/dl" inclusive="true"/> </value>
Das Attribut inclusive gibt mit true/false an, ob die Intervallgrenze im Intervall enthalten ist oder nicht (offenes oder geschlossenes Intervall)
8.7.2 Spezifikation[Bearbeiten]
Für numerische Werte gilt:
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
|---|---|---|---|---|---|
| value | PQ, IVL_PQ, INT, IVL_INT | 0..1 | O | ||
| @unit | cs | 1..1 | C | Physikalische Einheit des Messwertes mit UCUM Codierung (siehe [7]) | |
| Konditionale Konformität: Bei INT und IVL_INT Bei allen anderen |
0..0 1..1 |
NP M |
Angabe der Einheit erforderlich Angabe der Einheit nach UCUM (c/s) erforderlich. | ||
| @value | real | 1..1 | M | Größe des Messwertes | |
| @xsi:type | cs | 1..1 | M | Datentyp: für numerische Werte PQ | |
8.8 Verhältnisangabe RTO[Bearbeiten]
Repräsentiert eine Verhältnisangabe mit Zähler und Nenner. Zähler und Nenner sind abstrakt definiert und unterstützen alle vom abstrakten Datentyp QTY abgeleiteten Datentypen. Die gängigsten Datentypen sind hierbei INT und PQ.
Zähler und Nenner in der Ausprägung INT unterstützen die Strukturierung von Titer-Angaben wie z.B. 1:120.
Bei Zähler und Nenner vom Typ INT können, sofern nicht durch einen speziellen Implementierungsleitfaden eingeschränkt, immer die folgenden Attribute angegeben werden:
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
| numerator | INT | 1..1 | R | Zähler der Verhältnisangabe | |
| @value | int | 0..1 | R | Wert als positive ganze Zahl | |
| denominator | INT | 1..1 | R | Nenner der Verhältnisangabe | |
| @value | int | 0..1 | R | Wert als positive ganze Zahl | |
8.8.1 Verhältnisangabe RTO_PQ_PQ[Bearbeiten]
Repräsentiert eine Verhältnisangabe, bei der Zähler und Nenner in Einheiten messbare Größen darstellen.
8.8.1.1 Spezifikation[Bearbeiten]
Bei RTO_PQ_PQ Elementen können, sofern nicht durch einen speziellen Implementierungsleitfaden eingeschränkt, immer die folgenden Attribute angegeben werden:
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
| numerator | PQ | 1..1 | R | Zähler der Verhältnisangabe | |
| @value | real | 0..1 | R | Angabe der Größe des Messwertes | |
| @unit | cs | 0..1 | R | Physikalisch Einheit des Messwertes. Codiert nach UCUM ist EMPFOHLEN | |
| denominator | PQ | 1..1 | R | Nenner der Verhältnisangabe | |
| @value | real | 0..1 | R | Angabe der Größe des Messwertes | |
| @unit | cs | 0..1 | R | Physikalisch Einheit des Messwertes. Codiert nach UCUM ist EMPFOHLEN | |
8.8.1.2 Strukturbeispiele[Bearbeiten]
<!-- Verhältnisangabe ohne physikalische Größe, z.B. Titer 1:120 --> <value xsi:type="RTO"> <numerator xsi:type='INT' value='1'/> <denominator xsi:type='INT' value='120'/> </value> <!-- Einseitig offene Verhältnisangabe, z.B. Titer 1:≥32 --> <value xsi:type="RTO"> <numerator value="1" xsi:type="INT"/> <denominator xsi:type="IVL_INT"> <low value="32" inclusive="true"/> </denominator> </value>
8.9 Erfassung von Mengen (collection of quantities)[Bearbeiten]
Die HL7 V3 Datentypen unterstützen die geordnete Sammlung von einzelnen (aber nicht unbedingt verschiedenen) Werten innerhalb eines Datentyps (LIST).
Beispiel
<observation>
::
<value xsi:type="GLIST_TS">
<head value="20150822170922.86-0400" />
<!-- time interval between data points is 1 second -->
<increment value="1.0" unit="s" />
</value>
</observation>
::
::
<observation>
::
<value xsi:type="SLIST_PQ">
<origin value="0" unit="1" />
<scale value="1" unit="1" />
<digits>44 42 42 41 40 40 39 38 36 35 34 35 35 34 35 35 36 36 35 36</digits>
</value>
</observation>
8.9.1 Wertelisten (GLIST)[Bearbeiten]
8.9.1.1 Spezifikation[Bearbeiten]
| Name | Type | Description |
|---|---|---|
| head | T | The first item in this sequence. |
| increment | T.diffType | The difference between one value and the previous different value. |
| period | INT | If non-NULL, the duration over which the sequence repeats. |
| denominator | INT | The integer by which the index for the sequence is divided, giving the number of times the sequence generates the same sequence item value before incrementing to the next sequence item value. For example, to generate the sequence (1; 1; 1; 2; 2; 2; 3; 3; 3; ...) the denominator is 3. |
8.9.2 Wertesequenzen (SLIST)[Bearbeiten]
Für die Erfassung von Sequenzen von Werten steht der Datentyp SLIST zur Verfügung. SLIST wird verwendet, um die erfassten Biosignale zu übertragen. Eine SLIST enthält eine Liste von Ganzzahlen. Der Parameter T muss ein Typ von QTY sein. Das Item an einem bestimmten Index (i) in der Liste wird berechnet, indem das Item am gleichen Index in der Ziffernfolge (di) mit der Skala (s) multipliziert und dann dieser Wert zum Ursprung (xo) addiert wird.
8.9.2.1 Spezifikation[Bearbeiten]
| Name | Type | Description |
|---|---|---|
| origin | T | The origin of the list item value scale, i.e., the physical quantity that a zero-digit would represent in the sequence of values. |
| scale | T.diffType | A ratio-scale quantity that is factored out of the digit sequence. |
| digits | LIST<INT> | A sequence of raw digits representing the sample values. |
8.10 Komplexe (zusammengesetzte) Elemente[Bearbeiten]
8.10.1 Personen-Element[Bearbeiten]
Personen-Elemente im CDA sind komplexe, zusammengesetzte Objekte und dienen zur Abbildung von Personen. Ein Personen-Element beinhaltet im Wesentlichen das name-Element der Person.
8.10.1.1 Strukturbeispiel[Bearbeiten]
<assignedPerson>
<name>
<prefix qualifier="AC">Dr.</prefix>
<given>Hubert</given>
<family>Muster</family>
</name>
</assignedPerson>
8.10.1.2 Spezifikation[Bearbeiten]
Bei Personen-Elementen MÜSSEN, sofern nicht anders spezifiziert, immer die folgenden Elemente angegeben werden:
| Element/Attribut | DT | Kard | Konf | Beschreibung |
|---|---|---|---|---|
| name | PN | 1..* | M | Name der Person Grundsätzlich sind die Vorgaben gemäß "Namen-Elemente von Personen PN" zu befolgen. |
8.10.2 Organisations-Element[Bearbeiten]
Organisations-Elemente im CDA sind komplexe, zusammengesetzte Objekte und dienen zur Abbildung von Organisationen unter Berücksichtigung ihrer essentiellen Informationen, wie ID, Name, Adresse, Kontaktdaten, etc.
8.10.2.1 Strukturbeispiel[Bearbeiten]
<serviceProviderOrganization> <id root="1.2.40.0.34.3.1.xxx" assigningAuthorityName="GDA Index"/> <name>Amadeus Spital</name> <telecom value="tel:+43.1.3453446.0"/> <telecom value="fax:+43.1.3453446.4674"/> <telecom value="mailto:info@amadeusspital.at"/> <telecom value="http://www.amadeusspital.at"/> <addr> <streetName>Mozartgasse</streetName> <houseNumber>1-7</houseNumber> <postalCode>1234</postalCode> <city>St.Wolfgang</city> <state>Salzburg</state> <country>AUT</country> </addr> </serviceProviderOrganization>
8.10.2.2 Spezifikation[Bearbeiten]
Bei Organisations-Elementen MÜSSEN, sofern nicht anders spezifiziert, immer die folgenden Elemente angegeben werden:
8.10.2.2.1 id[Bearbeiten]
| Element/Attribut | DT | Kard | Konf | Beschreibung |
|---|---|---|---|---|
| id | II | 0..* | O | Beliebig viele IDs der Organisation. z.B.: ID aus dem GDA-Index, DVR-Nummer, ATU-Nummer, etc. Grundsätzlich sind die Vorgaben gemäß "Identifikations-Elemente" zu befolgen. |
8.10.2.2.2 Name der Organisation[Bearbeiten]
| Element/Attribut | DT | Kard | Konf | Beschreibung |
|---|---|---|---|---|
| name | PN | 1..1 | M | Name der Organisation Grundsätzlich sind die Vorgaben gemäß "Namen-Elemente von Organisationen ON" zu befolgen. |
8.10.2.2.3 Kontakt-Elemente der Organisation[Bearbeiten]
| Element/Attribut | DT | Kard | Konf | Beschreibung |
|---|---|---|---|---|
| telecom | TEL | 0..* | O | Beliebig viele Kontakt-Elemente der Organisation Grundsätzlich sind die Vorgaben gemäß "Kontaktdaten-Element" zu befolgen. |
8.10.2.2.4 Adress-Element der Organisation[Bearbeiten]
| Element/Attribut | DT | Kard | Konf | Beschreibung |
|---|---|---|---|---|
| addr | AD | 0..1 | O | Ein Adress-Elemente der Organisation Grundsätzlich sind die Vorgaben gemäß "Adress-Elemente" zu befolgen. |
Organisationen werden durch folgende Templates spezifiziert:
- Organization Compilation with name
- Organization Compilation with id, name
- Organization Compilation with id, name, tel, addr
- Organization Compilation with name, addr minimal
- Organization Compilation with name, addr minimal and telecom
8.10.3 AssignedEntity-Element (Person + Organisation)[Bearbeiten]
AssignedEntity-Elemente im CDA sind komplexe, zusammengesetzte Objekte und dienen zur Abbildung von abstrakten Entitäten, welche sich aus Person- und Organisationsinformationen zusammensetzen.
Hierbei MUSS jedenfalls die "Person" der Entität angegeben werden. Die Angabe der Organisation, der die Person angehört, ist prinzipiell optional. Diese Optionalität kann sich in Abhängigkeit vom konkreten Anwendungsfall in "verpflichtend" ändern.
8.10.3.1 Strukturbeispiel[Bearbeiten]
<assignedEntity>
<id root="1.2.40.0.34.99.111.1.3"
extension="2222"
assigningAuthorityName="Amadeus Spital"/>
<addr>
<streetName>Währinger Gürtel</streetName>
<houseNumber>18-20</houseNumber>
<postalCode>1090</postalCode>
<city>Wien</city>
<state>Wien</state>
<country>AUT</country>
</addr>
<telecom value="tel:+43.1.3453446.0"/>
<telecom value="fax:+43.1.3453446.4674"/>
<telecom value="mailto:info@amadeusspital.at"/>
<telecom value="http://www.amadeusspital.at"/>
<assignedPerson>
:
</assignedPerson>
<representedOrganization>
:
</representedOrganization>
</assignedEntity>
8.10.3.2 Spezifikation[Bearbeiten]
Bei AssignedEntity-Elementen MÜSSEN, sofern nicht anders spezifiziert, immer die folgenden Elemente angegeben werden:
8.10.3.2.1 id[Bearbeiten]
| Element/Attribut | DT | Kard | Konf | Beschreibung |
|---|---|---|---|---|
| id | II | 1..* | R | Mindestens eine ID der Person der Entität Zugelassene nullFlavor:
Grundsätzlich sind die Vorgaben gemäß "Identifikations-Elemente" zu befolgen. |
8.10.3.2.2 Adress-Element der Organisation[Bearbeiten]
| Element/Attribut | DT | Kard | Konf | Beschreibung |
|---|---|---|---|---|
| addr | AD | 0..1 | O | Ein Adress-Element der Person der Entität Grundsätzlich sind die Vorgaben gemäß "Adress-Elemente" zu befolgen. |
8.10.3.2.3 Kontakt-Elemente der Organisation[Bearbeiten]
| Element/Attribut | DT | Kard | Konf | Beschreibung |
|---|---|---|---|---|
| telecom | TEL | 0..* | O | Beliebig viele Kontakt-Elemente der Person der Entität Grundsätzlich sind die Vorgaben gemäß "Kontaktdaten-Element" zu befolgen. |
8.10.3.2.4 Personen-Element der Entität[Bearbeiten]
| Element/Attribut | DT | Kard | Konf | Beschreibung |
|---|---|---|---|---|
| assignedPerson | POCD_MT000040. Person |
1..1 | M | Personendaten der Person der Entität Grundsätzlich sind die Vorgaben gemäß "Personen-Element" zu befolgen. |
8.10.3.2.5 Organisations-Element der Entität[Bearbeiten]
| Element/Attribut | DT | Kard | Konf | Beschreibung |
|---|---|---|---|---|
| representedOrganization | POCD_MT000040. Organization |
0..1 | O | Organisationsdaten der Entität Grundsätzlich sind die Vorgaben gemäß "Organisations-Element" zu befolgen. |
Assigned Entity-Elemente werden durch folgende Templates spezifiziert:
- Assigned Entity
- Assigned Entity with id, name, addr and telecom
- Assigned Entity Body
- Assigned Entity Body with name, addr and telecom
9 Dataset des Allgemeinen Implementierungsleitfadens
Das Dataset (auch "Datenarten" oder "Konzepte") listet alle mit der Arbeitsgruppe abgestimmten Inhalte des Leitfadens auf. Es enthält Beschreibungen der Elemente mit Synonymen.
Dataset-Elemente können auf das CDA Datenmodell gemappt werden. In den Metadaten eines Templates sind alle assoziierten Konzepte auf einen Blick ersichtlich. Im Template-Body wird das assoziierte Konzept beim entsprechenden Datenelement angezeigt.
Die Live-Version des Datasets in Art-Decor kann unter folgendem Link betrachtet werden.
10 Administrative Daten (CDA Header)[Bearbeiten]
10.1 Übersichtstabelle der CDA Strukturen des Headers[Bearbeiten]
Dieses Kapitel gibt einen Überblick über die Elemente des CDA Headers und den Vorgaben bezüglich Kardinalität und Konformität. Spezielle Leitfäden können diese Vorgaben weiter einschränken.
| Element | Kard/Konf ELGA | Kard/Konf eHealth | Bedeutung / Link zum Kapitel |
|---|---|---|---|
| realmCode | 1..1 M | 1..1 M | Hoheitsbereich des Dokuments |
| typeId | 1..1 M | 1..1 M | Kennzeichnung CDA R2 |
| templateId | 3..* M | 3..* M | Kennzeichnung von Strukturvorschriften |
| id | 1..1 M | 1..1 M | Dokumenten-Id |
| code
translation |
1..1 M
1..1 M |
1..1 M
0..* R |
Klassifikation des Dokuments (fein und grob) |
| title | 1..1 M | 1..1 M | Titel des Dokuments |
| sdtc:statusCode | 0..1 C | 0..1 O | Status des Dokuments |
| hl7at:terminologyDate | 1..1 M | 0..1 O | Terminologie-Datum des Dokuments |
| hl7at:formatCode | 1..1 M | 0..1 O | FormatCode des Dokuments |
| hl7at:practiceSettingCode | 1..1 M | 0..1 O | Fachliche Zuordnung des Dokuments |
| effectiveTime | 1..1 M | 1..1 M | Erstellungsdatum des Dokuments (medizinisch relevantes Datum) |
| confidentialityCode | 1..1 M | 1..1 M | Vertraulichkeitscode |
| languageCode | 1..1 M | 1..1 M | Sprachcode des Dokuments |
| setId
versionNumber |
1..1 M
1..1 M |
1..1 M
1..1 M |
Versionierung des Dokuments |
| recordTarget | 1..1 M | 0..1 C | Patient |
| recordTarget de-identified | 0..0 NP | 0..1 C | Anonymer oder pseudonymisierter Patient |
| author | 1..* M | 1..* M | Verfasser des Dokuments |
| dataEnterer | 0..1 O | 0..1 O | Personen der Dateneingabe |
| informant | 0..* O | 0..* O | Informant |
| custodian | 1..1 M | 1..1 M | Verwahrer des Dokuments |
| informationRecipient | 0..* O | 0..* O | Beabsichtigte Empfänger des Dokuments |
| legalAuthenticator | 0..* C | 0..* C | Rechtlicher Unterzeichner, wird im speziellen Leitfaden definiert. |
| authenticator | 0..* O | 0..* O | Weitere Unterzeichner |
| participant | 0..* O | 0..* O | Weitere Beteiligte (nähere Unterscheidung im entsprechenden Leitfaden) |
| inFulfillmentOf | 0..* O | 0..* O | Zuweisung und Ordermanagement |
| documentationOf
serviceEvent |
0..* O
1..1 M |
0..* O
1..1 M |
Gesundheitsdienstleistungen |
| relatedDocument | 0..1 O | 0..1 O | Bezug zu vorgehenden Dokumenten |
| authorization | 0..0 NP | 0..* O | Einverständniserklärung |
| componentOf
encompassingEncounter |
0..1 O
1..1 M |
0..1 O
1..1 M |
Patientenkontakt (Aufenthalt) |
10.2 Übersicht der Zeitelemente im Header[Bearbeiten]
Dieses Kapitel gibt einen Überblick über die Elemente des CDA Headers mit Zeitangaben und ihre Zusammenhänge.
| Element | Kard/Konf
ELGA |
Kard/Konf
eHealth |
Bedeutung | Link zum Kapitel |
|---|---|---|---|---|
| hl7at:terminologyDate | 1..1 M | 0..1 O | Das Datum, an dem die lokal zur Implementierung verwendeten Value Sets mit dem österreichischen Terminologieserver abgeglichen wurden, wird hier angegeben. | Terminologie-Datum des Dokuments |
| effectiveTime | 1..1 M | 1..1 M | Das letzte medizinisch relevante Datum, an welchem das Dokument medizinische Inhalte hinzugefügt worden sind. Kann im speziellen Leitfaden anders definiert werden. | Erstellungsdatum des Dokuments |
| recordTarget
birthTime |
1..1 M
1..1 R |
0..1 C
1..1 R |
Der Geburtstag des Patienten. | Patient |
| recordTarget
deceasedTime |
1..1 M
0..1 O |
0..1 C
1..1 R |
Das Sterbedatum des Patienten. | Patient |
| author
time |
1..* M
0..1 R |
1..* M
0..1 R |
Das jeweilige Datum, an welche der jeweilige Autor neue medizinische Informationen hinzugefügt hat. | Verfasser des Dokuments |
| dataEnterer
time |
0..1 O
0..1 R |
0..1 O
0..1 R |
Das Datum, an welchem eine Schreibkraft die Informationen aus einem Medium in das CDA Dokument überträgt, ohne weitere fachliche Informationen hinzuzufügen. | Personen der Dateneingabe |
| legalAuthenticator
time |
0..* C
1..1 R |
0..* C
1..1 R |
Die Zeitpunkte, an welchem das Dokument von den einzelnen berechtigten Personen vidiert wurde. Diese Personen sind die Hauptunterzeichner. Ist im jeweiligen speziellen Implementierungsleitfaden genauer vorgeschrieben. Dieser Zeitpunkt, wenn vorhanden, sollte nach author.time und dataenterer.time liegen. | Rechtlicher Unterzeichner |
| authenticator
time |
0..* O
1..1 R |
0..* O
1..1 R |
Die Zeitpunkte, an welchem das Dokument von den einzelnen berechtigten Personen vidiert wurde. Diese Personen sind die weiteren Unterzeichner. | Weitere Unterzeichner |
| Notfallkontakt / Auskunftsberechtigte Person
participant [templateId[@root='1.2.40.0.34.6.0.11.1.27']] time |
0..* O
0..1 O |
0..* O
0..1 O |
Zeitraum, in dem der angegebene Kontakt den Notfall-Kontakt darstellt.
Wird nur angegeben, wenn der Kontakt bereits absehbar nur in einem eingeschränkten Zeitraum zur Verfügung steht. |
Weitere Beteiligte |
| Versicherter/Versicherungparticipant
participant [templateId[@root='1.2.40.0.34.6.0.11.1.26']] time |
0..* O
0..1 O |
0..* O
0..1 O |
Gültigkeitszeitraum der Versicherungspolizze. | Weitere Beteiligte |
| documentationOf serviceEvent |
0..* O 1..1 M |
0..* O 1..1 M |
Zeitraum der durchgeführten Gesundheitsdienstleistung. Ist im jeweiligen speziellen Implementierungsleitfaden genauer vorgeschrieben. | Gesundheitsdienstleistungen |
| componentOf encompassingEncounter |
0..1 O 1..1 M |
0..1 O 1..1 M |
Zeitraum des Patientenkontakts. | Patientenkontakt (Aufenthalt) |
10.3 Dokumentenstruktur[Bearbeiten]
10.3.1 XML Prolog (XML Metainformationen)[Bearbeiten]
10.3.1.1 Zeichencodierung[Bearbeiten]
CDA-Dokumente MÜSSEN mit UTF-8 (8-Bit Universal Character Set Transformation Format, nach RFC 3629 / STD 63 (2003)) codiert werden.
<?xml version="1.0" encoding="UTF-8" standalone="yes"?> :
10.3.1.2 Hinterlegung eines Stylesheets[Bearbeiten]
Um ein CDA-Dokument in einem Webbrowser anzeigen zu können, muss es nach HTML tranformiert werden. Das kann durch eine XSLT-Transformation (ein so genanntes "Stylesheet") geschehen. Ist das Stylesheet im angegebenen Pfad erreichbar, wird dieses beim Öffnen des CDA-Dokuments mit einem Browser üblicherweise automatisch auf das CDA-Dokument angewandt und die Darstellung gerendert. ELGA stellt zur einheitlichen Darstellung von CDA-Dokumenten ein "Referenz-Stylesheet" zur Verfügung (verfügbar unter http://www.elga.gv.at/cda). Da der Zugriff auf XSLT-Programme von den meisten Browsern eingeschränkt ist, wird kein absoluter Pfad auf eine Webressource angegeben.
<?xml-stylesheet type="text/xsl" href="ELGA_Stylesheet_v1.0.xsl"?>
- Das Stylesheet MUSS angegeben werden [M].
- Die Angabe eines Pfades ist NICHT ERLAUBT.
- Defaultwert ist
href="ELGA_Stylesheet_v1.0.xsl", ein anderes Stylesheet KANN in speziellen Leitfäden vorgeschrieben werden.
10.3.2 Wurzelelement clinicalDocument[Bearbeiten]
CDA-Dokumente beginnen mit dem Wurzelelement ClinicalDocument, der grobe Aufbau ist im folgenden Übersichtsbeispiel gegeben. Der XML-Namespace für CDA Release 2.0 Dokumente ist urn:hl7-org:v3 (Default-Namespace). Dieser MUSS in jeder CDA XML Instanz genannt werden. Zusätzlich MÜSSEN für Schema-Erweiterungen folgende Namespaces angegenben werden: xmlns:xsi="http://www.w3.org/2001/XMLSchema-instance" xmlns:pharm="urn:ihe:pharm:medication" xmlns:sdtc="urn:hl7-org:sdtc" xmlns:ips="urn:hl7-org:ips" xmlns:hl7at="urn:hl7-at:v3"
Hinweis: Die im Art-Decor vorgestellten Namespaces "hl7:" oder "cda:" werden nicht in den letztendlichen eHealth-Austria Dokumenten genutzt! Das HL7-International-Namespace, welches im Art-Decor unter "hl7:" oder "cda:" geführt wird, ist in den eHealth-Austria Dokumenten als Default-Namespace für alle eHealth-Austria-Dokumente geführt: "<ClinicalDocument xmlns="urn:hl7-org:v3" ... >". Somit ist bei Elementen, bei welchem das Namespace-Präfix weggelassen wurde, dieser sofort "urn:hl7-org:v3" - das Default-Namespace.
In speziellen Leitfäden können weitere neben den hier vordefinierten namespace-Präfixe angegeben werden.
<ClinicalDocument xmlns="urn:hl7-org:v3" xmlns:xsi="http://www.w3.org/2001/XMLSchema-instance" xmlns:pharm="urn:ihe:pharm:medication" xmlns:sdtc="urn:hl7-org:sdtc" xmlns:ips="urn:hl7-org:ips" xmlns:hl7at="urn:hl7-at:v3">
<!-- CDA Header -->
… siehe Beschreibung CDA R2 Header …
<!-- CDA Body -->
<component>
<structuredBody>
… siehe Beschreibung CDA R2 Body …
</structuredBody>
</component>
</ClinicalDocument>
10.3.3 Hoheitsbereich des Dokuments ("realmCode")[Bearbeiten]
Dieses Element kennzeichnet, dass das Dokument aus dem Hoheitsbereich Österreich stammt.
10.3.3.1 Spezifikation[Bearbeiten]
10.3.4 Dokumentformat ("typeId")[Bearbeiten]
Dieses Element kennzeichnet, dass das Dokument im Format CDA R2 vorliegt.
10.3.4.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.30 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 11:05:29 | |||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||
| Name | atcdabbr_header_DocumentTypeId | Bezeichnung | Document TypeId | |||||||||||||||||||||||||||||
| Beschreibung | Dieses Element kennzeichnet, dass das Dokument im Format CDA R2 vorliegt. | |||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.30 Document TypeId (2019‑05‑13 10:27:22) ref at-cda-bbr- | |||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||
10.3.5 ELGA Implementierungsleitfaden-Kennzeichnung ("templateId")[Bearbeiten]
Mittels templateId-Elementen können Teile von CDA-Dokumenten hinsichtlich ihrer Konformität zu bestimmten Templates gekennzeichnet werden. Auch Konformität zu Spezifikationen wie Implementierungsleitfäden kann ausgedrückt werden.
Der Einsatz von so genannten "templateId"-Elementen sichert zu, dass eine CDA-Instanz nicht nur CDA konform ist, sondern auch dem referenzierten Template oder Implementierungsleitfaden entspricht. Mit Zusicherung ist dabei nur eine informelle Behauptung des Verfassers gemeint und nicht notwendigerweise auch eine erfolgreich durchgeführte Validierung.
Ein CDA Dokument, welches den Vorgaben einer bestimmten Template entspricht, ist berechtigt und verpflichtet, die entsprechende templateId-Kennung einzutragen.
10.3.5.1 Strukturbeispiel[Bearbeiten]
<!— Folgt dem vorliegenden Implementierungsleitfaden-Template --> <templateId root="1.2.40.0.34.11.1"/> <!— Beliebig viele weitere templateIds, falls das Dokumente noch weiteren Templates, Implementierungsleitfäden oder Spezifikationen folgt --> <templateId root="…"/> :
10.3.5.2 Spezifikation[Bearbeiten]
Die OID des vorliegenden Implementierungsleitfadens MUSS im @root Attribut des Elements angegeben werden.
Mit Angabe dieses Elements wird ausgesagt, dass das vorliegende CDA-Dokument zu diesem Implementierungsleitfaden konform ist.
| Element/Attribut | DT | Kard | Konf | Beschreibung | |
|---|---|---|---|---|---|
| templateId[1] | II | 1..1 | M | eHealth Austria Dokumente ("Allgemeiner Leitfaden") Fester Wert: @root = "1.2.40.0.34.6.0.11.0.1" | |
| templateId[2] | II | 1..1 | M | OID des (speziellen) Implementierungsleitfadens. Dient als informative Referenz. Beispiel: @root = "1.2.40.0.34.7.1.7.0" | |
| templateId[3] | II | 1..1 | M | TemplateId für ein im speziellen Implementierungsleitfaden definiertes Dokument Beispiel: @root = "1.2.40.0.34.6.0.11.0.4" (Leitfaden e-Impfpass "Kompletter Immunisierungsstatus") | |
| templateId[n] | II | 0..* | O | Weitere TemplateIds, um Konformität zu weiteren (internationalen) Leitfäden zu dokumentieren. Dient als informative Referenz. Beispiel: @root="1.3.6.1.4.1.19376.1.5.3.1.1.18.1.2" (Immunization Content (IC) Content Module, IHE PCC Technical Framework Revision 11.0 - November 11, 2016) | |
Verweis auf speziellen Implementierungsleitfaden:
Die templateIds[2-n] werden speziellen Implementierungsleitfaden gemäß der Dokumentenklasse angegeben.
10.3.6 Dokumenten-Id ("id")[Bearbeiten]
Weltweit eindeutiger Instanzidentifikator des Dokuments.
10.3.6.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.1 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 10:36:12 | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||
| Name | atcdabbr_header_DocumentId | Bezeichnung | Document Id |
| ||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.1 Document Id (2019‑02‑18 11:06:14) ref at-cda-bbr- | |||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||
| ||||||||||||||||||||||||
10.3.7 Dokumentenklasse ("code")[Bearbeiten]
Der "Code des Dokuments" (im CDA das Element ClinicalDocument/code) bezeichnet die "Dokumentenklasse" bzw den präziseren "Dokumententyp".
Beispiele für die Klasseneinteilung der Dokumente:
- Dokumentenklasse: Entlassungsbrief
- Dokumententyp: "Entlassungsbrief aus stationärer Behandlung (Ärztlich)"
- Dokumententyp: "Entlassungsbrief aus stationärer Behandlung (Pflege)"
- Dokumentenklasse: Laborbefund
- Dokumentenklasse: Befundbericht Befund bildgebende Diagnostik
- …
Für das Mapping in XDS siehe den entsprechenden Leitfaden "ELGA XDS Metadaten".
Verweis auf speziellen Implementierungsleitfaden:
Die gültigen Wertebereiche dieses Elements entnehmen Sie bitte den entsprechenden speziellen Implementierungsleitfaden gemäß der Dokumentenklasse bzw dem Dokumententyp.
10.3.7.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.16 | Gültigkeit | 2021‑02‑19 10:34:26 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.1.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_DocumentCode | Bezeichnung | Document Code |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.16 Document Code (2020‑11‑17 14:56:33) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.1.16 Document Code (2019‑03‑18 10:56:56) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.3.8 Titel des Dokuments ("title")[Bearbeiten]
"Titel" (im CDA das Element ClinicalDocument/title) bezeichnet die verpflichtende "Dokumentenüberschrift" (zusätzlich zur Dokumentenklasse).
Beispiele für Titel der Dokumente:
- "Arztbrief"
- "Entlassungsbrief der gynäkologischen Abteilung des SMZ Ost"
- "Vorläufiger Entlassungsbrief"
- "Befundbericht"
- …
10.3.8.1 Strukturbeispiel[Bearbeiten]
<title>Entlassungsbrief</title>
10.3.8.2 Spezifikation[Bearbeiten]
| Element/Attribut | DT | Kard | Konf | Beschreibung |
|---|---|---|---|---|
| title | ST | 1..1 | M | Dokumententitel Der Sinn der Benennung MUSS mit der Dokumentenklasse übereinstimmen. Die Verwendung von Zeichenketten für Line Feed (lf), Carriage Return (cr) sowie Tabulator ist innerhalb des title generell NICHT ERLAUBT. |
10.3.9 Status des Dokuments ("sdtc:statusCode")[Bearbeiten]
Der Status eines Dokuments wird im CDA-Element ClinicalDocument/sdtc:statusCode gespeichert.
10.3.9.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.45 ref at-cda-bbr- | Gültigkeit | 2021‑06‑24 15:59:26 | ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210624 | |||||||||||||||||||||||||||||
| Name | atcdabbr_header_DocumentStatusCode | Bezeichnung | Document StatusCode |
| |||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.45 Document StatusCode (2021‑02‑19 11:04:04) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.1.45 Document StatusCode (2020‑05‑19 09:38:43) ref at-cda-bbr- | ||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
10.3.10 Terminologiedatum ("hl7at:terminologyDate")[Bearbeiten]
Das Terminologiedatum gibt an, dass ein Dokument mit den Terminologien zum Stand eines bestimmten Datums erstellt wurde. Das Datum wird in einem eigens für die HL7-Austria Domäne geschaffenen Element "hl7at:terminologyDate" angegeben.
10.3.10.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.46 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 11:04:44 | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||
| Name | atcdabbr_header_DocumentTerminologyDate | Bezeichnung | Document TerminologyDate | |||||||||||||||||||
| Beschreibung | Das Terminologie-Datum des Dokumentes Das Datum, an dem die lokal zur Implementierung verwendeten Value Sets mit dem österreichischen Terminologieserver abgeglichen wurden, wird hier angegeben. | |||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.46 Document TerminologyDate (2020‑07‑08 11:49:46) ref at-cda-bbr- | |||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||
| ||||||||||||||||||||||
10.3.11 FormatCode ("hl7at:formatCode")[Bearbeiten]
Die XDS-Metadaten enthalten ein Element formatCode, das das Format des Dokuments bezüglich seiner semantischen Interoperabilität beschreibt. Im CDA-Schema wurde für die HL7-Austria Domäne ein genau entsprechendes Element geschaffen.
10.3.11.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.47 ref at-cda-bbr- | Gültigkeit | 2021‑02‑24 07:21:13 | ||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.1.0+20210303 | |||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_DocumentFormatCode | Bezeichnung | Document FormatCode | ||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | die genaue Version des XDS FormatCode ↔ Hinweis zum XDS-Mapping: Dieses Element wird ins XDS-Attribut formatCode gemappt. | ||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.47 Document FormatCode (2021‑02‑19 10:35:52) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.1.47 Document FormatCode (2020‑07‑08 14:56:41) ref at-cda-bbr- | ||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
10.3.12 Fachliche Zuordnung des Dokuments ("hl7at:practiceSettingCode")[Bearbeiten]
Die "fachliche Zuordnung des Dokuments" wird im CDA-Element ClinicalDocument/hl7at:practiceSettingCode gespeichert.
10.3.12.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.44 ref at-cda-bbr- | Gültigkeit | 2021‑03‑01 15:37:20 | ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.1.0+20210303 | |||||||||||||||||||||||||||||
| Name | atcdabbr_header_DocumentPracticeSettingCode | Bezeichnung | Document PracticeSettingCode |
| |||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.44 Document PracticeSettingCode (2020‑05‑18 13:03:08) ref at-cda-bbr- | ||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
10.3.13 Erstellungsdatum des Dokuments ("effectiveTime")[Bearbeiten]
10.3.13.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.11 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 10:35:26 | |||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||
| Name | atcdabbr_header_DocumentEffectiveTime | Bezeichnung | Document Effective Time |
| ||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||
| Assoziiert mit |
| |||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.11 Document Effective Time (2019‑02‑12 16:30:12) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.90008 CD effectiveTime (2016‑07‑21) ref elgabbr- | |||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||
| ||||||||||||||||||||||||||
10.3.14 Vertraulichkeitscode ("confidentialityCode")[Bearbeiten]
10.3.14.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.12 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 13:39:30 | |||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | ||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_DocumentConfidentialityCode | Bezeichnung | Document Confidentiality Code |
| ||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| |||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.12 Document Confidentiality Code (2021‑02‑19 10:35:04) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.1.12 Document Confidentiality Code (2019‑03‑04 12:35:46) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.90009 CD confidentialityCode (2013‑11‑07) ref elgabbr- | |||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||
10.3.15 Sprachcode des Dokuments ("languageCode")[Bearbeiten]
10.3.15.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.13 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 10:36:53 | ||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_DocumentLanguage | Bezeichnung | Document Language |
| |||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| ||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.13 Document Language (2019‑02‑12 14:08:58) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.90010 CD languageCode (2013‑11‑07) ref elgabbr- | ||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
10.3.16 Versionierung des Dokuments ("setId" und "versionNumber")[Bearbeiten]
Mit den Attributen setId und versionNumber kann eine Versionskennung des Dokuments erreicht werden. Die setId bezeichnet das Set von Dokumenten, die zu einer Reihe von Versionen gehören. Sie bleibt über alle Versionen der Dokumente gleich (initialer Wert bleibt erhalten). Die versionNumber ist eine natürliche Zahl für die fortlaufende Versionszählung. Die versionNumber von neuen Dokumenten wird mit 1 festgelegt, mit jeder neuen Version wird diese Zahl hochgezählt, die setId bleibt gleich (muss mit der setId der Vorversion übereinstimmen).
Achtung: Manche Validatoren erkennen es als Fehler, wenn die SetID und ID gleich sind.
Für die direkte Referenzierung zwischen Dokumenten siehe "Bezug zu vorgehenden Dokumenten".
10.3.16.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.15 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 10:57:14 | ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||
| Name | atcdabbr_header_DocumentSetIdAndVersionNumber | Bezeichnung | Document Set Id and Version Number |
| |||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.15 Document Set Id and Version Number (2019‑02‑12 14:48:59) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.90007 SetId VersionNumber (2015‑09‑18) ref elgabbr- | ||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
10.4 Teilnehmende Parteien[Bearbeiten]
10.4.1 Patient ("recordTarget/patientRole")[Bearbeiten]
Im CDA-Header wird mindestes eine Patientenrolle beschrieben, die zu genau einer Person zugehörig ist. Die recordTarget Beziehung weist auf die Patient-Klasse und gibt an, zu welchem Patienten dieses Dokument gehört.
Auszug aus dem R-MIM:
<ref group="Abbildung">R-MIM Klassen rund um den Patienten</ref>
10.4.1.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.3 ref at-cda-bbr- | Gültigkeit | 2020‑11‑24 10:03:02 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.2.0+20210303 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_RecordTarget | Bezeichnung | Record Target |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.3 Record Target (2020‑10‑21 10:42:28) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.1.3 Record Target (2019‑02‑20 12:10:02) ref at-cda-bbr- Adaptation: Template 2.16.840.1.113883.10.12.101 CDA recordTarget (2005‑09‑07) ref ad1bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.4.1.2 Alternative Spezifikation de-identifizierter Patient[Bearbeiten]
Die Angabe von anonymen oder pseudonymisierten Patienten kann in speziellen e-Health-Leitfäden erforderlich sein, ist aber im Kontext von ELGA NICHT ERLAUBT.
| Id | 1.2.40.0.34.6.0.11.1.39 | Gültigkeit | 2021‑02‑19 11:22:28 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_RecordTargetDeIdentified | Bezeichnung | Record Target de-identified |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.39 Record Target de-identified (2020‑03‑31 10:49:11) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.1.3 Record Target (2019‑02‑20 12:10:02) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.4.2 Verfasser des Dokuments ("author")[Bearbeiten]
Auszug aus dem R-MIM:
<ref group="Abbildung">R-MIM Klassen rund um den Autor</ref>
10.4.2.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.2 ref at-cda-bbr- | Gültigkeit | 2021‑08‑24 08:35:56 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_Author | Bezeichnung | Author |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.2 Author (2021‑02‑18 12:40:27) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.1.2 Author (2019‑02‑13 09:50:17) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.4.3 Personen der Dateneingabe ("dataEnterer")[Bearbeiten]
10.4.3.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.22 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 10:33:56 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_Data_Enterer | Bezeichnung | Data Enterer | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Die das Dokument „ schreibende “ Person (z.B. Medizinische/r Dokumentationsassistent/in, Schreibkraft, …). Das Element "DataEnterer" entfällt bei automatisch erstellten Dokumenten (ODD). | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.22 Data Enterer (2019‑03‑26 11:33:48) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.4.4 Verwahrer des Dokuments ("custodian")[Bearbeiten]
Auszug aus dem R-MIM:
10.4.4.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.4 ref at-cda-bbr- | Gültigkeit | 2021‑10‑13 14:05:15 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_Custodian | Bezeichnung | Custodian |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.4 Custodian (2021‑02‑19 10:33:30) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.1.4 Custodian (2019‑02‑26 11:28:24) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.4.5 Beabsichtigte Empfänger des Dokuments ("informationRecipient")[Bearbeiten]
Auszug aus dem R-MIM:
<ref group="Abbildung">Klassen rund um die beabsichtigten Empfänger des Dokuments</ref>10.4.5.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.24 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 11:10:25 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_Information_Recipient | Bezeichnung | Information Recipient |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.24 Information Recipient (2019‑03‑26 13:08:59) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.20005 HeaderInformationRecipient (2011‑12‑19) ref elgabbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.4.6 Rechtlicher Unterzeichner ("legalAuthenticator")[Bearbeiten]
Auszug aus dem R-MIM:
<ref group="Abbildung">R-MIM Klassen rund um den Rechtlichen Unterzeichner und Mitunterzeichner</ref>
10.4.6.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.5 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 11:10:59 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_LegalAuthenticator | Bezeichnung | Legal Authenticator |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.5 Legal Authenticator (2019‑03‑04 11:41:57) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.20006 HeaderLegalAuthenticator (2011‑12‑19) ref elgabbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.4.7 Weitere Unterzeichner ("authenticator")[Bearbeiten]
10.4.7.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.6 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 10:25:00 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_Authenticator | Bezeichnung | Authenticator |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Offen (auch andere als die definierten Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.6 Authenticator (2019‑03‑04 13:11:54) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.4.8 Weitere Beteiligte ("participant")[Bearbeiten]
Mit dieser Assoziation und den entsprechenden Klassen können weitere für die Dokumentation wichtige beteiligte Personen oder Organisationen wie Angehörige, Verwandte, Versicherungsträger sowie weitere in Beziehung zum Patienten stehende Parteien genannt werden.
Es können grundsätzlich beliebig viele participant-Elemente im Dokument angegeben werden, teilweise gibt es aber Einschränkungen für die einzelnen Elemente.
Auszug aus dem R-MIM:
<ref group="Abbildung">R-MIM Klassen rund um weitere Beteiligte (participants)</ref>
10.4.8.1 Festlegung der "Art" des Beteiligten[Bearbeiten]
Die "Art" des Beteiligten wird über eine Kombination aus
- Attribut participant/@typeCode
- Element participant/functionCode
- Attribut participant/associatedEntity/@classCode
festgelegt.
Eine eindeutige Identifikation ist darüber hinaus noch über das templateId-Element möglich, welches für jede Art von Beteiligten einen eindeutigen Wert enthält.
Ebenfalls erhalten die Elemente innerhalb der Unterelemente ihre Bedeutung in Abhängigkeit von der Beteiligten-Art. Beispielsweise drückt das time-Element zwar generell den Zeitraum der Beteiligung, im Falle der Darstellung einer Versicherung allerdings den Gültigkeitsbereich der Versicherungspolizze aus.
Dieses Kapitel enthält eine detaillierte Anleitung zur Angabe der folgenden Arten von "weiteren Beteiligten":
| Element | Kard/Konf ELGA & eHealth |
Art des Beteiligten |
|---|---|---|
| participant | 0..1 O | Fachlicher Ansprechpartner |
| 0..1 O | Einweisender/Zuweisender/Überweisender Arzt | |
| 0..1 O | Hausarzt | |
| 0..* O | Notfall-Kontakt / Auskunftsberechtigte Person | |
| 0..* O | Angehörige | |
| 0..* O | Versicherter/Versicherung | |
| 0..1 O | Betreuende Organisation | |
| 0..* O | Weitere Behandler |
<ref group="Tabelle">Übersichtstabelle participant - weitere Beteiligte</ref>:Übersichtstabelle participant - weitere Beteiligte
Verweis auf speziellen Implementierungsleitfaden:
Welche der folgenden "weiteren Beteiligten" im Dokument angegeben werden müssen bzw. sollen, ergibt sich aus dem jeweiligen speziellen Implementierungsleitfaden.
Die angegebenen Templates können dort weiter spezifiziert / eingeschränkt werden.
10.4.8.2 Fachlicher Ansprechpartner[Bearbeiten]
Der fachliche Ansprechpartner ist jene Kontaktperson oder –stelle, welche zur Kontaktaufnahme für fachliche Auskünfte zum betreffenden Dokument veröffentlicht wird. Diese Maßnahme dient zur Kanalisierung und Vereinheitlichung der Kommunikationsschiene zwischen dem Erzeuger und dem Empfänger der Dokumentation, beispielsweise für Rückfragen oder Erfragung weiterer fachlicher Informationen. Die Angabe dieses Elements ist grundsätzlich optional, wobei in den speziellen Leitfäden eine verpflichtende Angabe spezifiziert sein kann. Bei Verwendung sollen möglichst präzise Kontaktdaten angegeben werden. Es obliegt der dokumenterzeugenden Organisation zu entscheiden, welchen Ansprechpartner sie veröffentlicht.
<ref group="Abbildung">Darstellung des fachlichen Ansprechpartners mittels ELGA Referenz-Stylesheet</ref>
Soll als Ansprechpartner der Verfasser des Dokuments angegeben werden, so sind die entsprechenden Daten an dieser Stelle noch einmal anzugeben.
Als fachlicher Ansprechpartner kann aber auch eine Stelle beschrieben sein, die eingehende Anfragen als erste entgegennimmt und in Folge an die zuständigen Personen weiterleitet.
Diese Beteiligten-Art wird durch folgende Kombination angegeben:
| Element | Wert | Beschreibung | Bedeutung |
|---|---|---|---|
| @typeCode | CALLBCK | Callback contact | Fachlicher Ansprechpartner |
| templateId | 1.2.40.0.34.6.0.11.1.20 | - | Template ID zur Identifikation dieser Art von Beteiligten |
| functionCode | - | - | Wird nicht angegeben |
| @classCode | PROV | Healthcare provider | Gesundheitsdienstanbieter |
10.4.8.2.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.20 ref at-cda-bbr- | Gültigkeit | 2021‑08‑03 11:02:47 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.2+20210803 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_ParticipantFachlicherAnsprechpartner | Bezeichnung | Participant Fachlicher Ansprechpartner |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.20 Participant Fachlicher Ansprechpartner (2021‑06‑30 15:57:10) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.1.20 Participant Fachlicher Ansprechpartner (2021‑02‑19 11:15:35) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.1.20 Participant Fachlicher Ansprechpartner (2019‑02‑12 15:59:16) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.1.1.1 HeaderParticipant Ansprechpartner (2014‑03‑25) ref elgabbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.4.8.3 Einweisender/Zuweisender/Überweisender Arzt[Bearbeiten]
Diese Beteiligten-Art wird durch folgende Kombination angegeben:
| Element | Wert | Beschreibung | Bedeutung |
|---|---|---|---|
| @typeCode | REF | Referrer | Einweisender/Zuweisender/Überweisender Arzt |
| templateId | 1.2.40.0.34.6.0.11.1.21 |
- | Template ID für: Einweisender/Zuweisender/Überweisender Arzt |
| functionCode | - | - | Wird nicht angegeben |
| @classCode | PROV | Healthcare provider | Gesundheitsdienstanbieter |
10.4.8.3.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.21 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 11:15:01 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_ParticipantEinweisenderZuweisenderUeberweisenderArzt | Bezeichnung | Participant Ein-, Ueber-, Zuweisender Arzt | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Beteiligter (Einweisender/Zuweisender Arzt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.21 Participant Ein-, Ueber-, Zuweisender Arzt (2019‑02‑12 16:23:33) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.1.1.1 HeaderParticipant Ansprechpartner (2014‑03‑25) ref elgabbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.4.8.4 Hausarzt[Bearbeiten]
Diese Beteiligten-Art wird durch folgende Kombination angegeben:
| Element | Wert | Beschreibung | Bedeutung |
|---|---|---|---|
| @typeCode | IND | Indirect target | In indirektem Bezug |
| templateId | 1.2.40.0.34.6.0.11.1.23 | - | Template ID zur Identifikation dieser Art von Beteiligten |
| functionCode | PCP | primary care physician | Hausarzt |
| @classCode | PROV | Healthcare provider | Gesundheitsdienstanbieter |
10.4.8.4.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.23 ref at-cda-bbr- | Gültigkeit | 2021‑08‑03 11:32:38 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210803 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_ParticipantHausarzt | Bezeichnung | Participant Hausarzt | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Hausarzt | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.23 Participant Hausarzt (2021‑02‑19 11:16:07) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.1.23 Participant Hausarzt (2019‑02‑13 10:44:48) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.1.1.1 HeaderParticipant Ansprechpartner (2014‑03‑25) ref elgabbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.4.8.5 Notfall-Kontakt/Auskunftsberechtigte Person[Bearbeiten]
Der Notfall-Kontakt entspricht in Österreich der "Auskunftsberechtigten Person" (oder auch "Vertrauensperson").
Diese Beteiligten-Art wird durch folgende Kombination angegeben:
| Element | Wert | Beschreibung | Bedeutung |
|---|---|---|---|
| @typeCode | IND | Indirect target | In indirektem Bezug |
| templateId | 1.2.40.0.34.6.0.11.1.27 | - | Template ID zur Identifikation dieser Art von Beteiligten |
| functionCode | - | - | Wird nicht angegeben |
| @classCode | ECON | Emergency contact | Notfall-Kontakt |
10.4.8.5.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.27 ref at-cda-bbr- | Gültigkeit | 2021‑08‑03 11:25:19 Andere Versionen mit dieser Id: | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.2+20210803 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_ParticipantAuskunftsberechtigtePersonNotfallkontakt | Bezeichnung | Participant Auskunftsberechtigte Person (Notfallkontakt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Der Notfall-Kontakt entspricht in Österreich der „Auskunftsberechtigten Person“ (oder auch „Vertrauensperson“). | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.27 Participant Auskunftsberechtigte Person (Notfallkontakt) (2021‑08‑03 10:59:17) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.1.27 Participant Auskunftsberechtigte Person (Notfallkontakt) (2021‑02‑19 11:13:06) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.1.27 Participant Auskunftsberechtigte Person (Notfallkontakt) (2019‑02‑12 15:50:47) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.1.1.1 HeaderParticipant Ansprechpartner (2014‑03‑25) ref elgabbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.4.8.6 Angehörige[Bearbeiten]
Als Angehörige sind in Österreich jene Personen anzusehen, welche in einem Verwandtschaftsverhältnis zum Patienten stehen, aber nicht unter die Gruppe der "Auskunftsberechtigten Personen" fallen (siehe Notfall-Kontakt/Auskunftsberechtigte Person).
Diese Beteiligten-Art wird durch folgende Kombination angegeben:
| Element | Wert | Beschreibung | Bedeutung |
|---|---|---|---|
| @typeCode | IND | Indirect target | In indirektem Bezug |
| templateId | 1.2.40.0.34.6.0.11.1.25 | - | Template ID zur Identifikation dieser Art von Beteiligten |
| functionCode | - | - | Wird nicht angegeben |
| @classCode | PRS | Personal relationship | In persönlicher Beziehung |
10.4.8.6.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.25 ref at-cda-bbr- | Gültigkeit | 2021‑08‑03 11:17:27 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210803 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_ParticipantAngehoerige | Bezeichnung | Participant Angehoerige |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.25 Participant Angehoerige (2021‑02‑19 11:11:34) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.1.25 Participant Angehoerige (2019‑02‑12 14:56:37) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.1.1.1 HeaderParticipant Ansprechpartner (2014‑03‑25) ref elgabbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.4.8.7 Versicherter/Versicherung[Bearbeiten]
Diese Beteiligten-Art wird durch folgende Kombination angegeben:
| Element | Wert | Beschreibung | Bedeutung |
|---|---|---|---|
| @typeCode | HLD | Holder | Teilnehmer hält ein finanzielles Instrument |
| templateId | 1.2.40.0.34.6.0.11.1.26 | - | Template ID zur Identifikation dieser Art von Beteiligten |
| functionCode | - | - | Wird nicht angegeben |
| @classCode | POLHOLD | Policy holder | Halter einer Versicherungspolizze |
10.4.8.7.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.26 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 11:16:42 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_ParticipantVersicherung | Bezeichnung | Participant Versicherung | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Der Beteiligte (Patient) ist selbst der Versicherungsnehmer oder ist bei einem Angehörigen mitversichert. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.26 Participant Versicherung (2019‑03‑26 14:54:17) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.1.1.1 HeaderParticipant Ansprechpartner (2014‑03‑25) ref elgabbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.4.8.8 Betreuende Organisation[Bearbeiten]
Als betreuende Organisation ist jene Organisation anzusehen, welche den Patienten nach Entlassung betreut (Trägerorganisationen, Vereine).
Beispiele: Mobile Hauskrankenpflege, Wohn- und Pflegeheime, Behinderteneinrichtungen, sozial betreutes Wohnen, …
Diese Beteiligten-Art wird durch folgende Kombination angegeben:
| Element | Wert | Beschreibung | Bedeutung |
|---|---|---|---|
| @typeCode | IND | Indirect target | In indirektem Bezug |
| templateId | 1.2.40.0.34.6.0.11.1.29 | - | Template ID zur Identifikation dieser Art von Beteiligten |
| functionCode | - | - | Wird nicht angegeben |
| @classCode | CAREGIVER | Betreuer | Betreuende Entität |
10.4.8.8.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.29 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 11:14:25 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_ParticipantBetreuungsorganisation | Bezeichnung | Participant Betreuungsorganisation |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.29 Participant Betreuungsorganisation (2019‑03‑26 17:25:44) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.1.28 Participant Weitere Behandler (2019‑03‑26 14:54:10) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.1.1.1 HeaderParticipant Ansprechpartner (2014‑03‑25) ref elgabbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.4.8.9 Weitere Behandler[Bearbeiten]
Über dieses Element können weitere an der medizinischen Behandlung maßgeblich beteiligte Personen angegeben werden. Das können Ärzte aus der gleichen oder einer anderen Abteilung sein, weiters niedergelassene behandelnde Ärzte (z.B. der behandelnde Internist oder Kinderarzt) aber auch nicht-ärztliche Behandler, wie z.B. Psychologen.
Die Angabe dieses Elements ist grundsätzlich optional, wobei in den speziellen Leitfäden eine verpflichtende Angabe spezifiziert sein kann. Bei Verwendung sollen möglichst präzise Kontaktdaten angegeben werden. Es obliegt der dokumenterzeugenden Organisation zu entscheiden, welche weitere Behandler sie veröffentlicht.
Diese Beteiligten-Art wird durch folgende Kombination angegeben:
| Element | Wert | Beschreibung | Bedeutung |
|---|---|---|---|
| @typeCode | CON | Consultant | Weitere Behandler |
| templateId | 1.2.40.0.34.6.0.11.1.28 | - | Template ID zur Identifikation dieser Art von Beteiligten |
| functionCode | Wert aus Value Set ELGA_Funktionscodes | Angabe der Funktion bzw. der Fachrichtung des Behandlers | |
| @classCode | PROV | Healthcare provider | Gesundheitsdienstanbieter |
10.4.8.9.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.28 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 11:17:20 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_ParticipantWeitereBehandler | Bezeichnung | Participant Weitere Behandler |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.28 Participant Weitere Behandler (2019‑03‑26 14:54:10) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.1.1.1 HeaderParticipant Ansprechpartner (2014‑03‑25) ref elgabbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.5 Zuweisung und Ordermanagement[Bearbeiten]
10.5.1 Auftrag ("inFulfillmentOf")[Bearbeiten]
Auszug aus dem R-MIM:
<ref group="Abbildung">R-MIM Klassen rund um den Zuweisung und Ordermanagement</ref>
10.5.1.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.9 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 13:42:25 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_InFulfillmentOf | Bezeichnung | In Fulfillment Of |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.9 In Fulfillment Of (2021‑02‑19 11:09:32) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.1.9 In Fulfillment Of (2019‑03‑14 13:22:14) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.20009 HeaderInFulfillmentOf (2011‑12‑19) ref elgabbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.6 Dokumentation der Gesundheitsdienstleistung[Bearbeiten]
10.6.1 Service Events ("documentationOf/serviceEvent")[Bearbeiten]
Repräsentiert die eigentliche Gesundheitsdienstleistung, die in dem Dokument dokumentiert wird.
Auszug aus dem R-MIM:
<ref group="Abbildung">R-MIM Klassen rund um die Gesundheitsdienstleistung</ref>
10.6.1.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.17 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 11:06:35 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_DocumentationOfServiceEvent | Bezeichnung | Documentation Of Service Event |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.17 Documentation Of Service Event (2019‑03‑14 15:08:34) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.7 Bezug zu vorgehenden Dokumenten[Bearbeiten]
10.7.1 Allgemeines[Bearbeiten]
Der Bezug zu Vordokumenten KANN über die parentDocument Beziehung ausgedrückt werden, indem der dazugehörige @typeCode einen Wert aus der Liste der gültigen @typeCodes in der relatedDocument-Beziehung erhält. Das Originaldokument, auf das sich das Dokument bezieht, bleibt dabei unverändert.
Für die Anwendung in ELGA ist ausschließlich die "ersetzende Beziehung" (replaces) erlaubt, wenn auch funktional nicht notwendig. Die Beziehung zwischen den verschiedenen Versionen eines Dokuments wird über die setId im XDS-Attribut referenceIdList im ELGA Verweisregister hergestellt. Der Bezug zu Vorgängerversionen KANN zusätzlich im CDA-Dokument durch die relatedDocument-Beziehung und die ParentDocument-Klasse, zusammen mit setId und versionNumber aus der ClinicalDocument-Klasse angegeben werden (siehe Versionierung des Dokuments).
<ref group="Abbildung">Grundsätzlicher Aufbau eines CDA-Dokuments aus XML Sicht</ref>
Ein konformes CDA Dokument kann theoretisch ein einzelnes relatedDocument mit @typeCode APND, oder ein relatedDocument mit @typeCode RPLC, oder ein relatedDocument mit @typeCode XFRM, oder zwei relatedDocuments mit @typeCode XFRM und RPLC, oder zwei relatedDocuments mit @typeCode XFRM und APND enthalten.
Liste der möglichen Werte der @typeCodes in der relatedDocument Beziehung:
| code | displayName | Bedeutung |
|---|---|---|
| RPLC | replaces | Das Dokument ersetzt ein existierendes Dokument. Der Status des zu ersetzenden Dokumentes wird auf "überholt" gesetzt, das ursprüngliche Dokument bleibt aber noch im System als historische Referenz verfügbar. |
| APND | append | Verwendung in ELGA NICHT ERLAUBT Zusammenhängen von Dokumenten. Dies ist in ELGA bereits über das Einbetten von Dokumenten realisiert. |
| XFRM | transformed | Verwendung in ELGA NICHT ERLAUBT Das Dokument ist Ergebnis eines Transformationsprozesses, d.h. ist aus einem anderen Originaldokument hervorgegangen. |
<ref group="Tabelle">Vokabel-Domäne relatedDocument.typeCode</ref>:Vokabel-Domäne relatedDocument.typeCode
10.7.2 Document Replacement - Related Document[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.14 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 13:42:15 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_DocumentReplacementRelatedDocument | Bezeichnung | Document Replacement - Related Document | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Der Bezug zu vorgehenden Dokumenten wird durch die relatedDocument-Beziehung und die ParentDocument-Klasse, zusammen mit setId und versionNumber aus der ClinicalDocument-Klasse, spezifiziert. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.14 Document Replacement - Related Document (2021‑02‑19 10:45:45) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.1.14 Document Replacement - Related Document (2019‑02‑28 14:06:32) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.20011 HeaderRelatedDocument (2014‑12‑06) ref elgabbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.8 Einverständniserklärung[Bearbeiten]
10.8.1 Autorisierung ("authorization")[Bearbeiten]
In dieser optionalen Klasse können die Einverständniserklärungen reflektiert werden, die mit dem Dokument verbunden sind. Dies kann ein Einverständnis für einen Eingriff oder die Verfügbarmachung der Informationen gegenüber Dritten beinhalten. Der Typ der Einverständniserklärung wird dabei in Consent.code angegeben.
Auszug aus dem R-MIM:
<ref group="Abbildung">R-MIM Consent Klasse</ref>
10.8.1.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.18 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 10:32:14 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_Authorization | Bezeichnung | Authorization |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.18 Authorization (2019‑02‑12 16:14:17) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.9 Informationen zum Patientenkontakt[Bearbeiten]
Diese Klasse repräsentiert Informationen, in welchem Rahmen der Patientenkontakt, der dokumentiert wird, stattgefunden hat. Dokumente werden nicht notwendigerweise immer während eines Patientenkontakts erstellt, sondern ggf. auch zu einem späteren Zeitpunkt, wenn beispielsweise ein Arzt wegen eines pathologischen Laborwertes den Patienten vergeblich versucht zu erreichen und dennoch seine Verlaufsdokumentation fortführt.
Wenn die Dokumentation ein Entlass- oder Verlegungsdokument ist, muss die Information in dieser Klasse mitgegeben werden, inklusive der Dauer des Aufenthalts (hier: nicht nur stationäre Aufenthalte, sondern auch Patientenkontakt in der Praxis eines Niedergelassenen beispielsweise) und der Einrichtung, wo der Patientenaufenthalt stattfand.
Auszug aus dem R-MIM:
<ref group="Abbildung">R-MIM EncompassingEncounter Klasse und Umgebung</ref>
10.9.1 Spezifikation[Bearbeiten]
10.9.2 Encounter ("componentOf/encompassingEncounter")[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.7 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 10:32:49 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_ComponentOfEncompassingEncounter | Bezeichnung | Component Of - Encompassing Encounter |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.7 Component Of - Encompassing Encounter (2020‑09‑29 10:39:03) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.20013 HeaderEncompassingEncounter (2011‑12‑19) ref elgabbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.9.3 Encounter Location[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.8 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 11:08:16 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_EncounterLocation | Bezeichnung | Encounter Location |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.8 Encounter Location (2020‑09‑29 10:33:43) ref at-cda-bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10.9.4 Encounter Location with addr, telecom[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.1.19 | Gültigkeit | 2021‑02‑19 11:08:57 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_header_EncounterLocation1 | Bezeichnung | Encounter Location with addr, telecom |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.1.19 Encounter Location with addr, telecom (2019‑03‑25 12:18:26) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.1.8 Encounter Location (2019‑03‑07 11:13:21) ref at-cda-bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11 Medizinische Inhalte (CDA Body)[Bearbeiten]
11.1 Allgemeiner Aufbau des CDA Body[Bearbeiten]
Der CDA Body eines CDA-Dokuments kann entweder "strukturiert" oder "unstrukturiert" angegeben werden.
11.1.1 Unstrukturierter medizinischer Inhalt: nonXMLBody[Bearbeiten]
Diese Art des CDA Body dient dazu, medizinische Inhalte völlig unstrukturiert anzugeben. Dies erfolgt in einem text-Element, wobei der Inhalt dieses Elements auch ein eingebettetes Dokument, beispielsweise PDF, codiert in Base64 sein kann.
Welche Art von Inhalt in dem text-Element abgebildet ist, wird über die Attribute @mediaType und @representation festgelegt.
11.1.1.1 Strukturbeispiel[Bearbeiten]
<ClinicalDocument xmlns="urn:hl7-org:v3">
:
CDA Header
:
<component>
<!-- Unstrukturierter CDA Body (Non-XML) -->
<nonXMLBody>
<text mediaType="application/pdf" representation="B64">
:
</text>
</nonXMLBody>
</component>
</ClinicalDocument>
11.1.2 Strukturierter medizinischer Inhalt: structuredBody[Bearbeiten]
Der structuredBody eines CDA Release 2.0 Dokuments setzt sich aus ein oder mehreren Komponenten (component) zusammen, wobei jede Komponente wiederum aus einer oder mehreren Sektionen (section) und gegebenenfalls aus einem oder mehreren maschinenlesbaren entry-Elementen (siehe CDA Level 1 bis 3) besteht.
11.1.2.1 Strukturbeispiel[Bearbeiten]
<ClinicalDocument xmlns="urn:hl7-org:v3">
:
CDA Header
:
<component>
<!-- strukturierter CDA Body -->
<structuredBody>
:
<component>
<section>
… CDA Body Sektion …
</section>
</component>
:
</structuredBody>
</component>
</ClinicalDocument>
11.1.2.2 CDA Level 1 bis 3[Bearbeiten]
Die CDA Level repräsentieren die unterschiedliche Feinheit (Granularität) der "maschinenlesbaren", also automatisch auswertbaren klinischen Informationen und des entsprechenden Text-Markups (standardisierte Form der maschinenauswertbaren Auszeichnung von Text).
11.1.2.2.1 CDA Level 1[Bearbeiten]
Mit Level 1 ist ein XML Dokument gekennzeichnet, das vor allem auf das Lesen des Dokuments von Menschen abzielt ("human readable"), also leicht für den menschlichen Gebrauch zugänglich gemacht werden kann (z.B. durch Stylesheets). Es gibt keine Einschränkungen hinsichtlich des Inhalts, Zwecks oder Gebrauchs des Dokuments. Die technischen Anforderungen, Level 1 Dokumente zu erzeugen oder zu verarbeiten, sind verhältnismäßig niedrig. Dies ist aus Datenverarbeitungssicht das gröbste Niveau von Informationen, gewährleistet damit aber sofort die Mensch-Mensch-Interoperabilität, die aus der klassischen "Papierwelt" bekannt ist.
CDA Level 1 sind alle Dokumente mit einem CDA "nonXMLBody" und jene mit Sektionen ohne Codierung:
<section> <title>Aufnahmegrund</title> <text> … Medizinischer Text … </text> </section>
11.1.2.2.2 CDA Level 2[Bearbeiten]
CDA Level 2 ermöglicht eine Klassifizierung der Abschnitte (sections) eines Dokuments. Dies wird durch die Angabe eines Codes erreicht, wofür prinzipiell jedes Codesystem herangezogen werden kann (etwa LOINC, SNOMED CT). Durch diese Codes werden die Abschnitte semantisch definiert. So kann ein Entlassungsbrief beispielsweise ganz bestimmte Abschnitte beinhalten (Anamnese, Behandlung, Medikation, weiteres Vorgehen etc.), während ein Befundbericht ganz andere Erfordernisse bezüglich der Abschnitte und Strukturen haben kann.
Auf dieser Ebene kommen so genannte Section-Level-Templates zur Anwendung. Diese machen Abschnitte maschinenauswertbar, d.h. durch Applikationen identifizierbar und ermöglichen eine Überprüfung des CDA-Dokuments dahingehend, ob es spezifische Abschnitte, Paragrafen und andere Strukturbestandteile aufweist.
<section>
<code
code="42349-1"
displayName="Grund für die Überweisung/Einweisung"
codeSystem="2.16.840.1.113883.6.1"
codeSystemName="LOINC" />
<title>Aufnahmegrund</title>
<text>
… Medizinischer Text …
</text>
</section>
11.1.2.2.3 CDA Level 3[Bearbeiten]
CDA-Dokumente, die auch Level 3 konform sind, beinhalten zusätzlich zu der lesbaren Text-Sektion auf dem Niveau von Einzelinformationen maschinenauswertbare Komponenten, so genannte entry-Elemente (wie beispielsweise "systolischer Blutdruck").
Eine Anwendung kann damit Daten wie eine einzelne Beobachtung, Prozedur, Medikamentengabe etc. identifizieren und verarbeiten. Selbst die Anwesenheit von bestimmten Einzelinformationen kann durch Vorgaben (Templates-Konzept) verpflichtend gemacht werden.
Alle relevanten medizinischen Daten MÜSSEN im "menschenlesbaren Teil", dem narrativen Block (title und text-Elemente der Sections) enthalten sein. Für die maschinenlesbaren Einträge (entry) kommen Entry-Level-Templates zum Einsatz. Dies MÜSSEN inhaltlich konsistent zum lesbaren Textbereich sein und sollen zusätzlich die entsprechenden Inhaltsstellen im Textbereich referenzieren. Zusätzliche maschinenlesbare Informationen können angegeben werden, sofern sie nicht dargestellt werden müssen und auch nicht Bestandteil des signierten Originalbefundes sind. Sind die narrativen Daten direkt von den maschinenlesbaren abgeleitet und daher inhaltlich gleich, wird das im Entry durch das Attribut typeCode="DRIV" angegeben. Hier kann ausschließlich der maschinenlesbare Teil ohne Informationsverlust zur Weiterverarbeitung verwendet werden.
<section>
<code
code="42349-1"
displayName="Grund für die Überweisung/Einweisung"
codeSystem="2.16.840.1.113883.6.1"
codeSystemName="LOINC" />
<title>Aufnahmegrund</title>
<text>
… Medizinischer Text …
</text>
<entry>
… HL7 Version 3 RIM Klassen (Beobachtung, Prozedur, …) mit Codes …
</entry>
</section>
11.1.3 Sektionen[Bearbeiten]
CDA bietet die Möglichkeit Sektionen mit sogenannten "templateId"-Elementen zu versehen. Mit diesen Elementen ist es möglich, analog zur ELGA Implementierungsleitfaden-Kennzeichnung für das gesamte Dokument, auch einzelne Sektionen zu kennzeichnen.
Diese Kennzeichnung ist speziell für Prüfmittel (z.B.: Schematron) wichtig, da über diese Kennzeichnungen die zugrundeliegenden Regeln zur Befüllung der Sektion zugeordnet und abgeprüft werden können.
Verweis auf speziellen Implementierungsleitfaden:
Welche templateId angegeben werden muss, ist im entsprechenden speziellen Implementierungsleitfaden in der Definition der Sektionen beschrieben.
Grundsätzlich können von speziellen Leitfäden folgende Elemente einer Section hinzugefügt werden:
- Untersektionen,
- Übersetzungs-Subsektionen in unterschiedlicher Sprache, wenn abweichend vom Gesamtdokument
- Maschinenlesbare Entry-Elemente
- Multimedia-Elemente für Grafiken und Attachments
- Verfasser (Author), wenn abweichend vom Gesamtdokument oder von der übergeordneten Struktur
- Informant, wenn abweichend vom Gesamtdokument oder von der übergeordneten Struktur
- Dokumentenverweise Verweise auf Quelldokumente (aus denen eine Information entnommen wurde)
11.1.3.1 "Kodiert" und "unkodiert" Sektionen[Bearbeiten]
Damit das Vorhandensein von maschinenlesbaren Werten in Sektionen klarer auszudrücken, werden manche Sektionen in zwei unterschiedlichen Templates mit dem Nachsatz "kodiert" und "unkodiert" angegeben (z.B. "Vitalparameter - kodiert" und "Vitalparameter - unkodiert").
- kodiert: Alle Informationen, die für diese Sektionen als maschinenlesbare Information vorgesehen sind, MÜSSEN alle entsprechenden Entrys enthalten.
- unkodiert: Diese Sektionen enthalten KEINE maschinenlesbaren Informationen, Entrys sind VERBOTEN.
11.1.4 Textstrukturierung und Formatierung[Bearbeiten]
Die medizinischen Informationen werden im CDA Body immer in Textform wiedergegeben (section.text ist verpflichtend). Dies garantiert, dass die Dokumente immer für den Menschen lesbar sind.
Der Text selber kann wiederum Strukturelemente aufweisen, mit den Listen, Tabellen, Unterabschnitte etc definiert werden.
Der CDA-Standard erlaubt nur eine kleine Auswahl an Formatierungsoptionen für den section.text, damit die oben genannte einfache Lesbarkeit ("human readability") zuverlässig erhalten bleibt und die Anforderungen für die Wiedergabe einfach bleiben. Die Syntax entspricht einem vereinfachten und stark eingeschränkten HTML.
Dieses Kapitel behandelt die verschiedenen Möglichkeiten der Textstrukturierung im text-Element einer CDA Sektion.
Hinweis: Damit Struktur und Formatierung möglichst von allen im Umlauf befindlichen Stylesheets korrekt wiedergegeben kann, dürfen nur bekannte Formatierungsoptionen verwendet werden.
Nur die in diesem Leitfaden genannten Optionen für die Strukturierung des Textes im narrativen Block sind ERLAUBT, alle anderen daher VERBOTEN.
Innerhalb von Sections wird das text-Element verwendet, um den narrativen Text ("plain text") darzustellen. In vielen Fällen lassen sich die medizinischen Inhalte aber auch noch weitergehend strukturieren. Dazu stehen in CDA als Stil-Elemente Listen, Tabellen und Unterabschnitte (Paragrafen) zur Verfügung. Mit Hilfe eines einfachen Stylesheets können die Inhalte in diesen Strukturelementen für den Menschen lesbar dargestellt werden.
11.1.4.1 Listen[Bearbeiten]
Das Strukturelement "Liste" dient zur Abbildung einer einfachen Aufzählung medizinischer Inhalte.
Eine Liste wird mit dem list Tag eingeschlossen. Das optionale Attribut @listType ermöglicht die Auflistung unsortiert (@listType="unordered"), die üblicherweise mit Bulletpoints • dargestellt wird, und in sortierter Form (@listType="ordered"), die mit Zahlen etc. dargestellt wird. Ohne Angabe von @listType ist die Liste unsortiert.
Ein Element der Aufzählung (item) wird mit dem item Tag eingeschlossen.
Folgende styleCodes können für die Formatierung von Listen mittels Aufzählungspunkten verwendet werden:
| styleCode | Definition | Nutzungsbeispiel |
|---|---|---|
| Disc | Unsortierte Liste mit ausgefüllten Kreisen | <list listType="unordered" styleCode= "Disc"> |
| Circle | Unsortierte Liste mit nicht ausgefüllten Kreisen | <list listType="unordered" styleCode= "Circle"> |
| Square | Unsortierte Liste mit ausgefüllten Quadraten | <list listType="unordered" styleCode= "Square"> |
| Arabic | Sortierte Liste mit Zahlen (1, 2, 3) | <list listType="ordered" styleCode= "Arabic"> |
| LittleRoman | Sortierte Liste mit kleingeschriebenen römischen Zahlen (i, ii, iii) | <list listType="ordered" styleCode="LittleRoman"> |
| BigRoman | Sortierte Liste mit großgeschriebenen römischen Zahlen (I, II, III) | <list listType="ordered" styleCode="BigRoman"> |
| LittleAlpha | Sortierte Liste mit kleingeschriebenen Buchstaben (a, b, c) | <list listType="ordered" styleCode= "LittleAlpha"> |
| BigAlpha | Sortierte Liste mit großgeschriebenen Buchstaben (A, B, C) | <list listType="ordered" styleCode="BigAlpha"> |
| None | Unterdrückt die Ausgabe von Aufzählungszeichen Kann verwendet werden, um eine Tabelle in einem Tabellenfeld einzufügen. Dabei wird ein List-Item im <td> -Element eingefügt, darin kann eine Tabelle als Unterelement angegeben werden. |
<list styleCode= "none"> |
<ref group="Tabelle">Listen - styleCodes</ref>:Listen - styleCodes
11.1.4.1.1 Strukturbeispiel[Bearbeiten]
Eine Liste hat das folgende Aussehen:
<text>
:
<list listType="ordered" styleCode= "BigAlpha">
<item>Pulmo: Basal diskrete RGs</item>
<item>Cor: oB</item>
<item>Abdomen: weich, Peristaltik: +++</item>
<item>Muskulatur: atrophisch</item>
<item>Mundhöhle: Soor, Haarleukoplakie</item>
<item>Haut blass, seborrhoisches Ekzem, Schleimhäute blass, Hautturgor herabgesetzt</item>
<item>Neuro: herabgesetztes Vibrationsempfinden der Beine, distal betont, Parästesien der Beine, PSR, AST oB und seitengleich.</item>
</list>
:
</text>
11.1.4.2 Tabellen[Bearbeiten]
Zur Repräsentation medizinischer Inhalte, die sich adäquat tabellarisch darstellen lassen, bietet sich die Tabellenform an. Als Beispiele seien genannt: Laborwerte, Allergiewerte, Diagnosen mit ICD-Codierung etc.
CDA realisiert ein vereinfachtes XHTML Table Modell, das HTML sehr ähnelt. Eine Tabelle wird mit dem table-Element angegeben. Siehe auch Erweiterte styleCodes.
Die Tabellenüberschrift wird eingeschlossen in thead Tags, die Überschriftenzeile in tr Tags und die einzelnen Spalten-Items der Überschrift mit th Tags.
Die optionale Tabellenunterschrift <tfoot> wird entsprechend der HTML-Tabellenkonvention direkt vor dem <tbody>-Tag und nach dem <thead> Tag angeführt. Es wird für Fußnoten in Tabellen verwendet und enthält genau einen <tr> und einen <td>-Tag (Siehe auch Beispiel in Fußnoten)
Die eigentlichen Tabelleninhalte werden in tbody Tags, die Datenzeile in tr Tags und die einzelnen Spalteninhalte einer Datenzeile mit td Tag gekapselt.
Mit dem caption-Unterelement wird eine Beschreibung der Tabelle angegeben. Die Textalternative für Tabellen (für Alt-Text bzw das alt-Tag in HTML) SOLL auch im caption-Unterelement von < table> angegeben werden. Dieses Element kann in Screenreadern entsprechend ausgewertet werden und erhöht die Barrierefreiheit.
Die Vorgaben für Tabellen MÜSSEN korrekt eingehalten werden, damit sie zuverlässig und korrekt durch Stylesheets dargestellt werden können.
Die Anzahl der Spalten MUSS über eine komplette Tabelle in thead und tbody gleich bleiben (ausgenommen tfoot).
Folgende Elemente und Attribute mit Auswirkung auf die Darstellung sind erlaubt:
- span (Achtung: Anzahl der Spalten muss über die Tabelle konstant bleiben)
- stylecode
Folgende Attribute sind ebenfalls erlaubt und sind im erzeugten HTML enthalten. Die Attribute werden z.B. für Barrierefreiheit benötigt (Ausgabe mit Screenreadern), müssen aber keine direkt sichtbare Auswirkung auf die Darstellung haben:
- language
- ID
- summary
- abbr
- axis
- headers
- scope
Alle anderen Attribute, wie z.B. rowspan sind explizit VERBOTEN!
11.1.4.2.1 Strukturbeispiel[Bearbeiten]
Eine Tabelle hat das folgende Aussehen:
<text>
:
<table>
<caption>Dies ist ein Strukturbeispiel einer Tabelle</caption>
<!-- Kopfzeile -->
<thead>
<tr>
<th>Spaltenüberschrift 1</th>
<th>Spaltenüberschrift 2</th>
</tr>
</thead>
<!-- Optionale Fußzeile mit EINER Spalte -->
<tfoot>
<tr>
<td>Die Fußzeile hat eine durchgehende Spalte</td>
</tr>
</tfoot>
<!-- Tabelleninhalte - Anzahl der Spalten gleich wie Kopfzeile -->
<tbody>
<tr>
<td>1. Zeile - Daten der Spalte 1</td>
<td>1. Zeile - Daten der Spalte 2</td>
</tr>
<tr>
<td>n. Zeile - Daten der Spalte 1</td>
<td>n. Zeile - Daten der Spalte 2</td>
</tr>
</tbody>
</table>
:
</text>
11.1.4.3 Unterabschnitte[Bearbeiten]
Zur Strukturierung eines längeren Textes kann das paragraph Tag verwendet werden.
11.1.4.3.1 Strukturbeispiel[Bearbeiten]
<text>
:
<paragraph>Sollten nach der empfohlenen Medikation mit Atemur die klinischen Zeichen weiterhin bestehen, halte ich bei dem umfangreichen Risikoprofil einen Kuraufenthalt für zwingend notwendig.</paragraph>
<paragraph>Ich bitte dann um Wiedervorstellung des Patienten.</paragraph>
:
</text>
11.1.4.4 Referenzierter bzw. attribuierter Inhalt (content)[Bearbeiten]
Das CDA content-Element wird benutzt, um Text ausdrücklich mit Tags "einzurahmen", so dass er referenziert werden kann oder bestimmte Möglichkeiten zur visuellen Darstellung genutzt werden können. Das content-Element kann rekursiv ineinander geschachtelt werden, was die Einrahmung von ganzen Texten bis hin zu kleinsten Teilen (Worte, Buchstaben etc.) erlaubt.
Referenzierter Inhalt
Das content-Element enthält ein optionales Identifikator Attribut, das als Ziel einer XML Referenz dienen kann. Alle diese IDs sind als XML IDs definiert und MÜSSEN im gesamten Dokument eindeutig sein. Die originalText Komponente einer RIM Klasse, die sich in den CDA Entries (siehe unten) wiederfindet, kann sich somit explizit auf die vom content-Element im Textteil umschlossene Information beziehen.
Attribuierter Inhalt
Das content-Element wird auch zur Einrahmung von Text benutzt, der in einem bestimmten Stil dargestellt werden soll, was mit dem @styleCode Attribut näher beschrieben wird.
11.1.4.4.1 Zugelassene styleCode Attribut-Werte[Bearbeiten]
| styleCode | Definition | Nutzungsbeispiel |
|---|---|---|
| bold | Fettdruck | <content styleCode="bold"> text </content> |
| underline | Unterstrichen | <content styleCode="underline"> text </content> |
| italics | Kursivschrift | <content styleCode="italics"> text </content> |
| emphasis | Kapitälchen | <content styleCode="emphasis"> text </content> |
<ref group="Tabelle">Tabellen - styleCodes</ref>:Tabellen - styleCodes
11.1.4.4.2 Strukturbeispiel[Bearbeiten]
Im folgenden Beispiel wird das Textstück "Asthma" durch das content-Element eingerahmt, so dass in einem möglichen Level 3 Entry darauf Bezug genommen werden kann (siehe "Verknüpfung von Text und Entry").
Darunter findet sich ein Text, der fett gedruckt erscheinen soll.
<text> : Diagnose des Patienten: <content ID="diag1">Asthma</content> <content styleCode="bold">Dieser Text ist fettgedruckt.</content> <content styleCode="bold italics"> Text ist fett und kursiv.</content> : </text>
11.1.4.5 Erweiterte styleCodes[Bearbeiten]
Neben den vom CDA-Standard vorgesehenen Möglichkeiten der Formatierung von Textelementen, erlaubt dieser Leitfaden die Nutzung weiterer styleCodes. Das ELGA Referenz-Stylesheet unterstützt die Verwendung dieser erweiterten, ELGA-spezifischen StyleCodes.
Die Darstellung der erweiterten, ELGA-spezifischen StyleCodes erfordert ein speziell angepasstes Stylesheet (z.B. das ELGA Referenz-Stylesheet).
Textstrukturen können durch diese ELGA-spezifisch erweiterten StyleCodes formatiert werden, z.B. um bestimmte Abschnitte wie Überschriften oder Unterüberschriften zu formatieren oder um die Textfarbe zu setzen.
| styleCode | Definition | Nutzungsbeispiel |
|---|---|---|
| xELGA_h1 | Überschriften gem. HTML < h1> | <paragraph styleCode="xELGA_h1"> |
| xELGA_h2 | Überschriften gem. HTML < h2> | <paragraph styleCode="xELGA_h2"> |
| xELGA_h3 | Überschriften gem. HTML < h3> | <paragraph styleCode="xELGA_h3"> |
| xELGA_blue | CMYK: 100, 60, 0, 6 RGB: 0, 96, 240 HTML: #0060f0 |
<content styleCode="xELGA_blue"> Anmerkung: Dient zur farblichen Hervorhebung von Wörtern oder Passagen im Fließtext. |
| xELGA_red | CMYK: 0, 91, 65, 12 RGB 224, 20, 79 HTML: #e3144f Zusätzlich wird der Text Fett dargestellt, da Rot für farbfehlsichtige Personen schwer erkennbar ist. |
<content styleCode="xELGA_red"> Anmerkung: Dient zur farblichen Kennzeichnung von pathologischen Labormesswerten in Tabellen (wird für die ganze Ergebniszeile in einer Tabelle) verwendet. |
| xELGA_colw:NN | NN...numerische Angabe des Prozentwertes der Spaltenbreite in Tabellen, maximal 2 Ziffern, nur positive Ganzzahlen. Wird nichts angegeben, wird die Spaltenbreite automatisch berechnet (bei n Spalten -- 1/n der gesamten Tabellenbreite) |
< th styleCode="xELGA_colw:20"> Die Spaltenbreite entspricht 20% der gesamten Tabellenbreite |
| xELGA_tabVertical | Gilt nur für die Ausgabe als Druckvorstufe (PDF): Die Ausrichtung der Tabelle ist um 90% in eine vertikale Orientierung gedreht Defaultausrichtung ist horizontal |
< table styleCode="xELGA_tabVertical"> Die Tabelle ist auf einer neuen Seite vertikal ausgerichtet, Tabellenbreite = Seitenhöhe Default: Horizontale Ausrichtung, Tabellenbreite = Textbreite |
| xELGA_monospaced | Statt der normalen Proportionalschrift wird eine nichtproportionale Schriftart (Festbreitenschrift) verwendet. | <content styleCode="xELGA_monospaced"> Anmerkung: Verwendung in Anwendungsszenarien, wo Texte in Befunde übernommen werden, die durch Verwendung von äquidistanten Schriftarten formatiert wurden. Beispiel: Laborwerttabellen |
<ref group="Tabelle">Erweiterte styleCodes</ref>:Erweiterte styleCodes
11.1.4.6 Zeilenumbrüche[Bearbeiten]
Das br-Element
kann benutzt werden, um im laufenden Text einen "harten" Zeilumbruch zu erzwingen. Dies unterscheidet es vom paragraph-Element, da der Zeilenumbruch keinen Inhalt hat. Empfänger sind angehalten, dieses Element als Zeilenumbruch darzustellen.
11.1.4.6.1 Strukturbeispiel[Bearbeiten]
<text> : Patient hat Asthma seit seinem zehnten Lebensjahr.<br/> Patient kommt damit gut zurecht. : </text>
11.1.4.7 Superscript und Subscript[Bearbeiten]
Ein Textbereich kann mit dem Element sup umspannt werden, um ihn Superscript (hochgestellt) darzustellen. Er kann mit sub umspannt werden, um ihn Subscript (tiefgestellt) darzustellen.
11.1.4.7.1 Strukturbeispiel[Bearbeiten]
<text> : Dieses Wort ist <sup>hochgestellt</sup> Dieses Wort ist <sub>tiefgestellt</sub> : </text>
11.1.4.8 Fußnoten[Bearbeiten]
Mit den Elementen footnote und footnoteref sind diese Gestaltungsmöglichkeiten im CDA-Standard beschrieben.
11.1.4.8.1 Strukturbeispiel[Bearbeiten]
Die Fußnotenreferenzen werden fortlaufend nummeriert und durch einen Tag hochgestellt. Der Text wird unter <tfoot> mit dem <footnote> Tag gekennzeichnet. Die ID gibt eine eindeutige Referenz auf den Text einer Fußnote.
<table>
<thead>
...
</thead>
<tfoot>
<tr>
<td>
<footnote ID="fn1"><sup>1)</sup> Wert kontrolliert</footnote>
</td>
</tr>
</tfoot>
<tbody>
...
<tr ID="OBS-13-1">
<td ID="OBS-13-1-Code">aPTT</td>
<td ID="OBS-13-1-Value">57.0
<!-- Fußnoten werden durch das XSL entsprechend angezeigt -->
<sup>1)</sup>
</td>
<td ID="OBS-13-1-Unit">s</td>
<td ID="OBS-13-1-Reference">26.0-40.0</td>
<td ID="OBS-13-1-Interpretation">++</td>
<td ID="OBS-13-1-Delta"/>
<td ID="OBS-13-1-Extern">E</td>
</tr>
...
<tbody>
</table>
11.1.4.9 HTML-Verweise[Bearbeiten]
Über das Element linkHtml lassen sich Verweise dokumentintern und auf externe Webseites (ähnlich wie im HTML-Standard beschrieben) realisieren. Wird in diesem Leitfaden nicht genutzt.
11.1.4.10 Geschützte Leerzeichen[Bearbeiten]
Grundsätzlich werden zusätzliche Leerzeichen am Anfang und am Ende eines Elementinhaltes bei der Darstellung entfernt, auch mehrere Leerzeichen hintereinander (z.B. zwischen Wörtern) werden wie ein Leerzeichen behandelt.
Zusätzlicher Leerraum (whitespace bzw "no-break space") kann in CDA erzeugt werden durch & #160; oder & #xA0;
Es erzeugt einen Leerraum von einem Zeichen und entspricht dem in HTML verwendeten, in CDA aber NICHT ERLAUBTEN "& nbsp;".
11.1.4.11 Verwendung von Revisionsmarken[Bearbeiten]
Wenn eine neue Version eines CDA-Dokuments erstellt wird, können in der Update-Version jene Text-Elemente, die sich gegenüber der Vorversion geändert haben, entsprechend markiert und besser ersichtlich gemacht werden. Eingefügter Text wird unterstrichen und kursiv, gelöschter Text durchgestrichen dargestellt.
Umgesetzt wird dies mithilfe des content-Elements, welches ein optionales Attribut revised enthält und mit "insert" oder "delete" befüllt werden kann.
Die korrekte Anzeige wird durch Angabe entsprechende Parameter durch das ELGA Referenz-Stylesheets (ShowRevisionMarks) unterstützt.
Beispiel:
Verwendung von Revisionsmarken in CDA / XML: Revisionsmarken: das ist der Fließtext mit <content revised='delete'>Text den man nur mit ShowRevisionMarks=1 durchgestrichen</content> und <content revised='insert'>eingefügtem (daher kursiv und unterstrichen dargestelltem)</content> Text.
Darstellung HTML:
Revisionsmarken: das ist der Fließtext mit Text den man nur mit ShowRevisionMarks=1 durchgestrichen und eingefügtem (daher kursiv und unterstrichen dargestelltem) Text.
11.1.5 Strukturen in Level 3[Bearbeiten]
Neben der obligatorischen Repräsentation der medizinischen Inhalte in section.text ("Level 2") kann eine zusätzliche Darstellung dieser Inhalte auf Level 3 hinzugefügt werden, um sie für das empfangende System strukturiert auswertbar zu machen. Es sei an dieser Stelle nochmals darauf hingewiesen, dass der menschenlesbare Inhalt von section.text führend für den medizinischen Inhalt ist, und dass Level 3-Konstrukte dieselbe, aber maschinenauswertbare Information tragen.
Generell sind in der CDA Entry Auswahl folgende Klassen aus dem RIM modelliert:
| CDA Entry | Bedeutung |
|---|---|
| Observation | Allgemeine oder spezifische Beobachtung, wie z. B. Diagnosen, Befunde, Laborergebnisse etc. |
| ObservationMedia | Medieninformation zur Beobachtung, z. B. externe Referenzen auf Bilder etc. |
| Procedure | Prozeduren, Eingriffe, die den Patienten "verändern" |
| RegionOfInterest | Fokusinformation |
| SubstanceAdministration | Verordnung von Medikamenten, Hilfsmitteln etc. |
| Supply | Verabreichung, Verfügbarmachung von Medikamenten, Hilfsmitteln etc. |
| Encounter | Kontakt mit Patient |
| Act | Generische Aktivität |
| Organizer | Ordnungsmöglichkeit für CDA Entries Hinweis: Das Attribut sdtc:text ist zusätzlich erlaubt, um diesem Element einen lesbaren Textinhalt zu geben und um die FHIR-Kompatibilität zu erhöhen. |
<ref group="Tabelle">CDA Entry Klassen</ref>:CDA Entry Klassen
Dieses Kapitel gibt eine grundsätzliche Anleitung für den Aufbau von Level 3 Strukturen und behandelt den Zusammenhang von text und entry.
Ähnlich wie bei einzelnen Sections können auch jedem Entry einzeln Participants zugeordnet werden. So kann eine bestimmte Prozedur um teilnehmende Personen ergänzt werden, die nur an dieser Prozedur beteiligt waren (siehe nachfolgende Abbildung)
<ref group="Abbildung">Zuordnung von Participants zu einzelnen Sections</ref>
11.1.5.1 Bezug zwischen Entries[Bearbeiten]
Angabe dieser Beziehung in entryRelationship. Beispiele für solche Beziehungen zwischen Entries sind:
- Observation und ObservationMedia (entryReleationship.typeCode = COMP "component")
- Observation ("Nesselsucht") und Observation ("Allergie"), entryReleationship.typeCode = MFST ("Manifestation of")
- Eine Beobachtung besteht aus Teilbeobachtungen, z. B. eine Batterie von Labortests, systolischer und diastolischer Blutdruck.
Über die entryRelationship Klasse können die verschiedenen Entries miteinander verbunden werden. Der @typeCode gibt dabei die Art der Beziehung wieder.
<ref group="Abbildung">R-MIM entryRelationship Klasse</ref>
11.1.5.2 Verknüpfung von Text und Entry ("CDA Level 4")[Bearbeiten]
Wenn eine Verknüpfung zwischen dem codierten Eintrag und dem Text in CDA hergestellt ist, wird das inoffiziell auch "Level 4" genannt. Die Verknüpfung funktioniert über Angabe von id-Attributen bei den Elementen innerhalb der Textabschnitte, die auf die zugehörigen Level 3 Entries referenzieren. Dabei wird das Ziel verfolgt, schrittweise mehr strukturiertes Markup zur Verfügung zu stellen, das Applikationen nutzen können.
Jedes Element im narrativen Kontext kann ein id-Attribut mitführen. Dieses ist vom Typ xs:ID und MUSS im gesamten Dokument eindeutig sein. IDs dieser Art beginnen mit einem Buchstaben, gefolgt von einem oder mehreren Buchstaben, Zahlen, Bindestrichen oder Unterstrichen.
<ref group="Abbildung">Referenzierung Text - Entry</ref>
Dies erlaubt, dass der Text mit einer einfachen URI dereferenziert werden kann. Die URI ist lokal im Dokument definiert, beginnt mit einem #-Zeichen, gefolgt von der ID.
Aus den obigen Beispielen würde das folgende Textfragment durch De-Referenzierung der Referenz "#disdiag1_diagnosis" gewonnen: "M25.46, Meniskus: Empyema gen. sin.".
Der Bezug vom Quelltext zu den Entries wird im @typeCode Attribut des entry-Elements angegeben und ist im Normalfall (und Default) COMP (component). Dies ist der allgemeine Fall und bedeutet, dass die Information in den Entries im Inhalt des Quelltexts enthalten ist. Weiter sind keine inhaltlichen Implikationen dabei vorhanden. In diesem Falle ist außerdem der narrative Quelltext der authentifizierte Inhalt.
Für den Fall, dass der narrative Text gänzlich aus codierten Entries abgeleitet ist, wird dies mit dem @typeCode DRIV (derived from) ausgedrückt. Dies ist beispielsweise bei Diagnoseninformationen der Fall, die eigentlich vollständig hoch-codiert in den Entries vorliegen und woraus der klinische Text erzeugt wird.
Weiterhin gibt es Situationen, in denen Entries vorhanden sind, ohne dass dazu ein Quelltext vorhanden ist, z.B. bei Kalibierungsangaben, Reagenzien oder andere Informationen, die für die weitere Verarbeitung notwendig sind. Auch hier ist der @typeCode der entryRelationship = COMP.
Auch ein Mix aus verschiedenen Entries und verschiedenen Beziehungstypen ist möglich.
11.1.5.2.1 Templates für Level 4-Referenzen[Bearbeiten]
Für die Herstellung dieser Referenzen wurden zwei Muster-Templates bereitgestellt, die diese Beziehung erzeugen ("compilations"):
11.1.6 Untersektionen – Hierarchischer Aufbau[Bearbeiten]
Sektionen können laut CDA Schema beliebig verschachtelt werden.
Eine Sektion kann eine oder mehrere Untersektionen enthalten, welche jeweils wiederum Untersektionen enthalten können, usw.
Verweis auf speziellen Implementierungsleitfaden:
Ob eine Sektion weitere Untersektionen enthält, ist im entsprechenden speziellen Implementierungsleitfaden in der Definition der Sektionen beschrieben.
11.1.6.1 Strukturbeispiel[Bearbeiten]
<ClinicalDocument xmlns="urn:hl7-org:v3">
:
<!-- CDA Header -->
:
<component>
<!-- strukturierter CDA Body -->
<structuredBody>
<component>
<section>
<code …/>
<title>Name der Sektion</name>
<text>…</text>
<!-- Untersektion -->
<component>
<section>
<code …/>
<title>Name der Untersektion</name>
<text>…</text>
</section>
</component>
</section>
</component>
</structuredBody>
</component>
</ClinicalDocument>
11.1.7 Einbetten von Dokumenten/Multimedia-Dateien[Bearbeiten]
Es ist möglich, zusätzlich zu dem Text auch Referenzen auf externe Multimediaobjekte wie Bilder etc. zu spezifizieren. Dies geschieht über das renderMultiMedia-Element und dient dazu aufzuzeigen, wo das Multimedia-Objekt gezeigt/dargestellt werden soll.
Das renderMultiMedia-Element trägt dabei im @referencedObject Attribut die ID auf den Verweis auf das Multimedia-Objekt. Dieser Verweis wird als entry in der ObservationMedia-Klasse abgelegt. Im value-Element des observationMedia-Elements wird das eigentliche Objekt (Dokument, Bild …) eingebettet. Im caption-Unterelement wird eine Beschreibung des Multimedia-Objektes angegeben. Das Referenzstylesheet wird den Inhalt als Mouseover und als Alternativtext ausgeben.
<ref group="Abbildung">R-MIM ObservationMedia Klasse zur Ablage von Multimedia-Objekten</ref>
Hinweis zur erlaubten Größe von Multimedia-Inhalten siehe "Größenbeschränkung von eingebetteten Objekten":
Die Gesamtgröße von CDA-Dokumenten (XML-Datei) wird durch die Infrastruktur eingeschränkt. Die Größe der eingebetteten Dateien soll auf ein sinnvolles und angemessenes Minimum beschränkt werden.
Hinweis zur Verwendung von Multimedia-Inhalten und Barrierefreiheit:
Die Empfänger der Dokumente haben unterschiedliche Ausgabegeräte und unterschiedliche Bedürfnisse. Bilder, sowie Audio- und Videodateien werden möglicherweise nicht dargestellt oder gedruckt werden können.
Bitte beachten Sie also im Sinne der Barrierefreiheit folgende Punkte
- Bei Multimedia-Daten MÜSSEN die relevanten Inhalte immer im lesbaren Text beschrieben werden.
- Wo Multimedia-Dateien normalerweise angezeigt werden, MUSS eine sprechende Beschreibung ihres Inhaltes angegeben werden (z.B. Bildunterschrift).
- Die Textalternative für Bilddaten (für Alt-Text bzw das alt-Tag in HTML) SOLL auch im caption-Unterelement von <renderMultimedia> angegeben werden. Dieses Element kann in Screenreadern entsprechend ausgewertet werden und erhöht die Barrierefreiheit.
- Grafiken mit Transparenzen sind NICHT ERLAUBT.
11.1.7.1 Strukturbeispiele[Bearbeiten]
11.1.7.1.1 Eingebettetes PDF[Bearbeiten]
Das folgende Beispiel beschreibt einen eingebetteten Befund, der in der Sektion "Beigelegte Befunde" angegeben wurde.
<section>
<!-- Inhalt der Section, mit Title, Text... -->
<entry>
<observationMedia classCode="OBS" moodCode="EVN" ID="MM1">
<!-- Eingebettetes Objekt Entry -->
<templateId root="1.2.40.0.34.6.0.11.3.19"/>
<value
mediaType="application/pdf"
representation="B64">
JVBEi0xLjMKJcfsj6IKNSAwIG9iago8PC9MZW5ndGggNiAwIFIvRmlsdGVyI
C9GbGF0ZURlY29kZT4+CnN0cmVhbQp4nM1aW28dtxFGnLfzK/ap3S0ihveLU
M5z5OHt+bjgTznIVGh7/o/84Xi0+PwjN+d3i54Vh1nNjezltH6+a50sYJngj
AuOu2Z5thB9n2gcZ55r2XjoEzBjuVq0Tbf8V5wAUhjvQqhNUJyZ4E2c8KZ90
e0opgNXrv2p40zBn/YAZU0HLR+cb3lnW Tbf8V5wAUhjvQqhNUJyZ4E2c8KZ
: : :
</value>
</observationMedia>
</entry>
</section>
11.1.7.1.2 Eingebettetes Bild[Bearbeiten]
Das folgende Beispiel beschreibt einen Befund am linken Zeigefinger, der zusätzlich mit einem Bild dokumentiert ist.
<section>
<!-- Inhalt der Section, mit Title, Text... -->
<entry>
<observationMedia classCode="OBS" moodCode="EVN" ID="MM1">
<!-- Eingebettetes Objekt Entry -->
<templateId root="1.2.40.0.34.6.0.11.3.19"/>
<value
mediaType="image/jpeg"
representation="B64">
JVBEi0xLjMKJcfsj6IKNSAwIG9iago8PC9MZW5ndGggNiAwIFIvRmlsdGVyI
C9GbGF0ZURlY29kZT4+CnN0cmVhbQp4nM1aW28dtxFGnLfzK/ap3S0ihveLU
AQYydprBSJcJICNvqgu1TrSI4kN0H+bF76M/LQ4S7Jmd3DlY/kg6IO4NBDch
e0opgNXrv2p40zBn/YAZU0HLR+cb3lnW Tbf8V5wAUhjvQqhNUJyZ4E2c8KZ
: : :
</value>
</observationMedia>
</entry>
</section>
11.1.7.2 Spezifikation[Bearbeiten]
Siehe "Eingebettetes Objekt Entry".
11.1.7.3 Zugelassene mediaType Attribut-Werte[Bearbeiten]
Der Datentyp von Multimedia-Objekten ist immer ED (encapsulated data). Dabei ist auch der Medientyp (MIME) im entsprechenden @mediaType Attribut zu nennen.
Zulässige Werte gemäß Value-Set "ELGA_Medientyp"
Verweis auf speziellen Implementierungsleitfaden:
Spezielle Implementierungsleitfäden können zusätzliche Medientypen (MIME) erlauben.
Achtung: Grafiken mit Transparenz (z.B: bei GIF oder PNG möglich) können zu schweren Problemen bei der Wiedergabe oder Konvertierung zu PDF/A-1 führen und sind daher NICHT ERLAUBT.
11.2 CDA Body in EIS "Basic"[Bearbeiten]
Neben den allgemein gültigen Aussagen über den grundsätzlichen Aufbau eines CDA Body, spezifiziert dieser Allgemeine Implementierungsleitfaden auch die Vorgaben, die ein ELGA Dokument in Interoperabilitätsstufe EIS "Basic" erfüllen muss.
11.2.1 Dokumente gemäß dem Allgemeinen Implementierungsleitfaden[Bearbeiten]
Der CDA Body kann unstrukturiert ("nonXMLBody") oder strukturiert ("structuredBody") angegeben werden. Die grundsätzlichen Richtlinien von CDA sind einzuhalten. Dieser Leitfaden macht keine speziellen Vorgaben für die Strukturierung des medizinisch-inhaltlichen Teils (CDA Body), dies erfolgt durch die jeweiligen speziellen Leitfäden.
Siehe "Allgemeiner Aufbau des CDA Body".
Verweis auf speziellen Implementierungsleitfaden:
Existiert bereits ein spezieller Implementierungsleitfaden zur Dokumentenklasse (z.B. Entlassungsbrief, Laborbefund etc.), MUSS dieser angewandt werden.
Spezielle Leitfäden definieren gegebenenfalls zusätzliche Vorgaben sowohl im administrativen Bereich ("CDA Header") als auch im medizinischen Bereich ("CDA Body"), wie beispielsweise:
- Welche Art von CDA Body ist zugelassen (nonXMLBody, structuredBody)
- Welche Sektionen sind anzugeben (verpflichtend, optional)
- Sektionendetails (Code und Titel der Sektionen)
- In welcher Granularität soll die Sektion angegeben werden (mit maschinenlesbaren Einträgen)
- Welche Codelisten werden für die maschinenlesbaren Einträge verwendet
- Reihenfolge der Sektionen im Dokument
- etc.
11.3 Allgemeine Sektionen-Templates[Bearbeiten]
Dieses Kapitel beschreibt ELGA Sektionen-Templates, die von mehr als einem speziellen Implementierungsleitfaden verwendet werden.
11.3.1 Übersichtstabelle der allgemeinen Sektionen des CDA Bodys[Bearbeiten]
| Sektion | Kard/Konf | Bedeutung / Link zum Kapitel | Konformität Level 3 (Entry) |
|---|---|---|---|
| Brieftext | 0..1 O | Anrede oder Begrüßung (Freitext) | 0..1 O (falls Logo angegeben) |
| Abschließende Bemerkungen | 0..1 O | Grußformel am Ende des Briefes (Freitext) | 0..0 NP |
| Beilagen | 0..1 O | Sonstige Beilagen (außer Willenserklärungen und andere juridische Dokumente) | 1..* M |
| Willenserklärungen und andere juridische Dokumente | 0..1 O | Wichtige Willenserklärungen und juridische Dokumente (Freitext) | 0..0 NP |
| Willenserklärungen und andere juridische Dokumente - Subsektion | 0..1 O | Wichtige Willenserklärungen und juridische Dokumente | 0..0 NP |
| Anmerkungen | 0..1 O | Nicht-medizinische Anmerkungen zum Patienten (Freitext) | 0..0 NP |
| Vitalparameter - kodiert | 0..1 O | Kodierte Informationen zu den Vitalparametern | 1..* M |
| Vitalparameter - unkodiert | 0..1 O | Angabe von Vitalparametern (Freitext) | 0..0 NP |
| Übersetzung | 0..1 O | Subsection für die Übersetzung des narrativen Textes | 0..0 NP |
| Risiken - Subsektion | 0..1 O | Risiken zur übergeordneten Sektion (Freitext) | 0..0 NP |
| Hilfsmittel und Ressourcen | 0..1 O | Hilfsmittel und Ressourcen zur übergeordneten Sektion (Freitext) | 0..0 NP |
11.3.2 Brieftext[Bearbeiten]
Der Titel dieser Sektion wird vom ELGA Referenz-Stylesheet nicht angezeigt, das Logo wird speziell platziert. Andere CDA-Stylesheets könnten den Titel der Sektion anzeigen und das Logo direkt im Text der Sektion darstellen.
Um eine möglichst kompakte Darstellung der Befunde zu ermöglichen, sollte der Text dieser Sektion so knapp wie möglich gehalten werden. Vermieden werden sollten jedenfalls der Patienten- oder Arztname, die Bezeichnung der Krankenanstalt sowie Daten zum Aufenthalt. Diese Daten werden an anderer Stelle im Befund angezeigt, eine Erwähnung in dieser Sektion führt zu Redundanzen.
11.3.2.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.2.69 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 11:19:35 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_section_Brieftext | Bezeichnung | Brieftext |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.2.69 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Section level template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.2.69 Brieftext (2021‑02‑19 11:44:10) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.2.69 Brieftext (2019‑04‑02 15:48:06) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.3.3 Abschließende Bemerkung[Bearbeiten]
Der Titel dieser Sektion wird vom ELGA Referenz-Stylesheet nicht angezeigt. Andere CDA-Stylesheets könnten den Titel der Sektion anzeigen.
Um eine möglichst kompakte Darstellung der Befunde zu ermöglichen, sollte der Text dieser Sektion so knapp wie möglich gehalten werden. Vermieden werden sollten jedenfalls der Patienten- oder Arztname, die Bezeichnung der Krankenanstalt sowie Daten zum Aufenthalt. Diese Daten werden an anderer Stelle im Befund angezeigt, eine Erwähnung in dieser Sektion führt zu Redundanzen.
11.3.3.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.2.70 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 11:25:03 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_section_AbschliessendeBemerkung | Bezeichnung | Abschließende Bemerkung |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.2.70 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Section level template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.2.70 Abschließende Bemerkung (2021‑02‑19 11:27:16) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.2.70 Abschließende Bemerkung (2020‑01‑09 09:53:27) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.1.2.2 AbschliessendeBemerkung (2012‑07‑14) ref elgabbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.3.4 Beilagen[Bearbeiten]
11.3.4.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.2.71 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 11:22:40 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_section_Beilagen | Bezeichnung | Beilagen |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.2.71 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Section level template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.2.71 Beilagen (2021‑02‑19 11:43:44) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.2.71 Beilagen (2020‑01‑09 09:53:16) ref at-cda-bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.3.4.2 Textbereich der Sektion[Bearbeiten]
Vorgaben und Empfehlungen zur Gestaltung des Textbereichs der Sektion im Falle des Vorhandenseins von maschinenlesbaren Elementen (CDA Level 3): Vorgaben:
- Es SOLLEN der Titel des Dokuments, sowie das Erstellungsdatum angegeben werden
11.3.4.3 Maschinenlesbare Elemente der Sektion[Bearbeiten]
Die Beilagen MÜSSEN als maschinenlesbare Elemente angegeben werden.
11.3.5 Willenserklärungen und andere juridische Dokumente[Bearbeiten]
11.3.5.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.2.61 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 12:03:11 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.1.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabrr_section_WillenserklaerungenUndAndereJuridischeDokumente | Bezeichnung | Willenserklärungen und andere juridische Dokumente |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.2.61 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Section level template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.2.61 Willenserklärungen und andere juridische Dokumente (2020‑10‑07 13:52:27) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.2.61 Willenserklärungen und andere juridische Dokumente (2019‑11‑25 12:58:58) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.11.1.2.4 Patientenverfügung (2011‑12‑19) ref elgabbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.3.5.2 Willenserklärungen und andere juridische Dokumente - Subsektion[Bearbeiten]
11.3.5.3 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.2.62 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 11:58:06 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabrr_section_SUBWillenserklaerungenUndAndereJuridischeDokumente | Bezeichnung | Willenserklärungen und andere juridische Dokumente - Subsektion |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.2.62 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Section level template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.2.62 Willenserklärungen und andere juridische Dokumente - Subsektion (2019‑11‑26 11:15:17) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.11.13.2.11 Willenserklärungen (2017‑08‑04 11:56:28) ref elgabbr- Adaptation: Template 1.2.40.0.34.11.1.2.4 Patientenverfügung (2011‑12‑19) ref elgabbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.3.6 Anmerkungen[Bearbeiten]
11.3.6.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.2.75 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 11:40:34 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabrr_section_Anmerkungen | Bezeichnung | Anmerkungen | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Ein Freitext für beliebige weitere nicht-medizinische Anmerkungen zum Patienten. Der Text soll keine fachlich relevante Information beinhalten. z.B. „Die Patientin mag besonders Kamelien.“ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.2.75 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Section level template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.2.75 Anmerkungen (2020‑01‑27 06:52:14) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.1.2.5 Anmerkungen (2011‑12‑19) ref elgabbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.3.7 Vitalparameter - kodiert[Bearbeiten]
11.3.7.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.2.46 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 12:03:03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.1.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabrr_section_VitalparameterKodiert | Bezeichnung | Vitalparameter - kodiert | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Informationen zu den Vitalparametern (Körpertemperatur, Puls, Blutdruck …). | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.2.46 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Section level template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Assoziiert mit |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.2.46 Vitalparameter - kodiert (2020‑10‑06 09:16:17) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.2.46 Vitalparameter - kodiert (2019‑07‑19 13:48:27) ref at-cda-bbr- Spezialisierung: Template 2.16.840.1.113883.10.20.1.16 Vital signs section (DYNAMIC) ref ccd1- Spezialisierung: Template 1.3.6.1.4.1.19376.1.5.3.1.3.25 IHE Vital Signs Section (DYNAMIC) ref IHE-PCC- Spezialisierung: Template 1.3.6.1.4.1.19376.1.5.3.1.1.5.3.2 eHDSI Vital Signs (DYNAMIC) ref epsos- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.3.7.2 Vorgaben zur Text-Gestaltung[Bearbeiten]
Vorgaben:
- Darstellung der Vitalparameter in Tabellenform
- Reihenfolge der Informationen:
- Vitalparameterart (@displayName des Codes des Vitalparameter-Entry)
- Wert (@value des Werts des Vitalparameter-Entry)
- Einheit (@unit des Werts des Vitalparameter-Entry)
- Das Erhebungsdatum SOLL den Vitalparametern eindeutig zugeordnet werden (Erhebungsdatum des VitalparameterGruppe-Entry)
11.3.7.3 Maschinenlesbare Elemente der Sektion[Bearbeiten]
Es MÜSSEN maschinenlesbare Elemente angegeben werden.
11.3.8 Vitalparameter - unkodiert[Bearbeiten]
11.3.8.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.2.68 ref elgagab- | Gültigkeit | 2021‑02‑19 10:43:13 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20201105 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | elgagab_section_VitalparameterUnkodiert | Bezeichnung | Vitalparameter - unkodiert |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.2.68 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Section level template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.2.68 Vitalparameter - unkodiert (2019‑12‑17 10:12:28) ref elgagab- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.3.9 Übersetzung[Bearbeiten]
Sections können Sub-Sections mit Übersetzungen des narrativen Textes in andere Sprachen beinhalten. Der Language-Code muss aus dem Value Set ELGA_LanguageCode gewählt werden.
Beispiel mit deutscher Übersektion:
<section>
<templateId root="1.2.40.0.34.11.2.2.13" assigningAuthorityName="ELGA"/>
<id root="..." extension="..."/>
<code code="48765-2" displayName="Allergies, adverse reactions, alerts" codeSystem="2.16.840.1.113883.6.1" codeSystemName="LOINC"/>
<title>Allergien, Unverträglichkeiten und Risiken</title>
<text>keine Allergien bekannt</text>
<component>
<!-- Übersetzung -->
<section>
<templateId root="1.2.40.0.34.6.0.11.2.8"/>
<title>Allergie ed Intolleranze</title>
<text>Nessuna Allergia Nota</text>
<languageCode code="it-IT"/>
</section>
</component>
</section>
11.3.9.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.2.8 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 11:28:05 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_section_Uebersetzung | Bezeichnung | Übersetzung |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.2.8 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Section level template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.2.8 Übersetzung (2021‑02‑19 11:58:13) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.2.8 Übersetzung (2019‑05‑14 15:24:50) ref at-cda-bbr- Adaptation: Template 2.16.840.1.113883.10.12.201 CDA Section (2005‑09‑07) ref ad1bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.3.10 Risiken[Bearbeiten]
11.3.10.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.2.76 | Gültigkeit | 2021‑02‑19 11:57:59 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabrr_section_Risiken | Bezeichnung | Risiken | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Wird ausschließlich als Untersektion zu einer fachlichen Sektion angewandt. Enthält die Risiken zum Thema der übergeordneten Sektion als narrative Beschreibung oder Auflistung. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.2.76 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Section level template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.2.76 Risiken (2020‑01‑27 13:14:21) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.1.2.8 Risiken (2011‑12‑19) ref elgabbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.3.11 Hilfsmittel und Ressourcen[Bearbeiten]
11.3.11.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.2.77 | Gültigkeit | 2021‑02‑19 11:46:25 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabrr_section_HilfsmittelRessourcen | Bezeichnung | Hilfsmittel und Ressourcen | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Wird ausschließlich als Untersektion zu einer fachlichen Sektion angewandt. Enthält die Hilfsmittel und Ressourcen zum Thema der übergeordneten Sektion als narrative Beschreibung oder Auflistung. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.2.77 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Section level template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.2.77 Hilfsmittel und Ressourcen (2020‑01‑27 13:24:04) ref at-cda-bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4 Maschinenlesbare Elemente[Bearbeiten]
Dieses Kapitel beschreibt ELGA Entry-Templates, die von mehr als einem speziellen Implementierungsleitfaden verwendet werden.
11.4.1 Eingebettetes Objekt Entry[Bearbeiten]
11.4.1.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.19 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 11:13:27 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_entry_EingebettetesObjektEntry | Bezeichnung | Eingebettetes Objekt Entry |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.19 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.19 Eingebettetes Objekt Entry (2021‑02‑19 12:43:14) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.3.19 Eingebettetes Objekt Entry (2020‑12‑17 12:24:45) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4.2 Logo Entry[Bearbeiten]
11.4.2.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.53 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 11:08:49 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_entry_Logo | Bezeichnung | Logo Entry | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.53 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.53 Logo Entry (2021‑02‑19 12:51:55) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.3.53 Logo Entry (2020‑01‑09 12:00:13) ref at-cda-bbr- Version: Template 1.2.40.0.34.11.1.3.2 Logo Entry (2011‑12‑19) ref elgabbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4.3 Vitalparameter Gruppe Entry[Bearbeiten]
11.4.3.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.23 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 13:01:06 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.1.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_entry_VitalparameterGruppeEntry | Bezeichnung | Vitalparameter Gruppe Entry |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.23 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.23 Vitalparameter Gruppe Entry (2020‑10‑07 07:45:39) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.3.23 Vitalparameter Gruppe Entry (2019‑07‑19 14:21:41) ref at-cda-bbr- Spezialisierung: Template 2.16.840.1.113883.10.20.22.4.26 Vital Signs Organizer (V3) (DYNAMIC) ref ccda- Spezialisierung: Template 2.16.840.1.113883.10.20.36.2 (DYNAMIC) ref ? Version: Template 1.2.40.0.34.11.1.3.3 Vitalparameter Gruppe Entry (DYNAMIC) ref elgabbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4.3.2 Vitalparameter (component)[Bearbeiten]
Jeder Vitalparameter ist als Komponente der Vitalparametergruppe angeführt. Es MUSS mindestens ein Vitalparameter angegeben werden.
Jeder Vitalparameter des Vitalparameter Gruppe Entry ist in Form eines ELGA Vitalparameter Entry (1.2.40.0.34.6.0.11.3.24) anzugeben.
11.4.4 Vitalparameter Entry[Bearbeiten]
11.4.4.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.24 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 13:00:55 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.1.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_entry_VitalparameterEntry | Bezeichnung | Vitalparameter Entry |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.24 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.24 Vitalparameter Entry (2020‑10‑07 07:50:09) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.3.24 Vitalparameter Entry (2019‑07‑19 14:38:56) ref at-cda-bbr- Spezialisierung: Template 2.16.840.1.113883.10.20.1.31 Result observation (DYNAMIC) ref ccd1- Spezialisierung: Template 1.3.6.1.4.1.19376.1.5.3.1.4.13 eHDSI Simple Observation (DYNAMIC) ref epsos- Spezialisierung: Template 1.3.6.1.4.1.19376.1.5.3.1.4.13.2 eHDSI Vital Signs Observation (DYNAMIC) ref epsos- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4.5 Serienmessung Vitalparameter Entry[Bearbeiten]
11.4.5.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.100 ref at-cda-bbr- | Gültigkeit | 2021‑01‑28 14:50:03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.1.1+20210303 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_entry_SerienmessungVitalparameterEntry | Bezeichnung | Serienmessung Vitalparameter Entry |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.100 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.100 Serienmessung Vitalparameter Entry (2020‑10‑07 07:51:58) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.3.100 Serienmessung Vitalparameter Entry (2020‑06‑02 10:24:26) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.3.54 (2020‑06‑02 07:03:02) ref ? | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4.6 Serienmessung Entry[Bearbeiten]
11.4.6.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.101 ref at-cda-bbr- | Gültigkeit | 2021‑01‑21 08:12:21 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.2.0+20210303 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_entry_SerienmessungEntry | Bezeichnung | Serienmessung Entry |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.101 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.101 Serienmessung Entry (2020‑10‑07 08:03:31) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.3.101 Serienmessung Entry (2020‑06‑02 07:03:02) ref at-cda-bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4.7 Serienmessungs-Gruppe Entry[Bearbeiten]
11.4.7.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.102 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 12:59:10 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_entry_SerienmessungsGruppeEntry | Bezeichnung | Serienmessungs-Gruppe Entry |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.102 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.102 Serienmessungs-Gruppe Entry (2020‑06‑02 07:48:02) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4.8 Serienmessungs-Werte Entry[Bearbeiten]
11.4.8.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.103 ref at-cda-bbr- | Gültigkeit | 2021‑01‑28 14:58:41 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210303 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | SerienmessungsWerteEntry | Bezeichnung | Serienmessungs-Werte Entry |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.103 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.103 Serienmessungs-Werte Entry (2020‑06‑02 08:05:24) ref at-cda-bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4.9 Serienmessungs-Periode Entry[Bearbeiten]
11.4.9.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.104 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 12:59:19 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | SerienmessungsPeriodeEntry | Bezeichnung | Serienmessungs-Periode Entry |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.104 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.104 Serienmessungs-Periode Entry (2020‑06‑02 09:22:17) ref at-cda-bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4.10 Problem Concern Entry[Bearbeiten]
11.4.10.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.7 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 12:55:33 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.1.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_entry_ProblemConcern | Bezeichnung | Problem Concern Entry |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.7 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Label | IHE PCC TF2 Rev.11, 6.3.4.12 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.7 Problem Concern Entry (2020‑11‑17 14:30:36) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.3.7 Problem Concern Entry (2019‑01‑18 10:05:27) ref at-cda-bbr- Adaptation: Template 1.3.6.1.4.1.19376.1.5.3.1.4.5.2 eHDSI Problem Concern (DYNAMIC) ref epsos- Adaptation: Template 1.3.6.1.4.1.19376.1.5.3.1.4.5.1 IHE Concern Entry (DYNAMIC) ref IHE-PCC- Adaptation: Template 2.16.840.1.113883.10.20.1.27 Problem act (DYNAMIC) ref ccd1- Adaptation: Template 2.16.840.1.113883.10.12.301 CDA Act (2005‑09‑07) ref ad1bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4.11 Problem Entry[Bearbeiten]
Das Problem Entry erlaubt die Dokumentation eines Gesundheitsproblems, das verschiedene Ausprägungen haben kann:
- Diagnose (Diagnosis)
- Problem (Problem)
- Zustand (Condition)
- Symptom (Symptom)
- Befund (Finding)
- Beschwerde (Complaint)
- Funktionelle Einschränkung (Functional limitation)
Da es sich bei einem Problem technisch um eine observation, also eine dokumentierte Beobachtung handelt, erhält sie den fixen StatusCode "completed". Der Status des Gesundheitsproblems selbst kann über das darin liegende Entry "Problem Status Observation" angegeben werden. Um welches Problem es sich handelt, wird im value-Element angegeben.
11.4.11.1 effectiveTime[Bearbeiten]
Die effectiveTime (die "medizinisch relevante Zeit") ist der Zeitraum, zu dem die Beobachtung für den Patienten gilt. Für z.B. einen Arzt, der heute einen Patienten in der Klinik behandelt und einen Herzinfarkt dokumentiert, der vor fünf Jahren aufgetreten ist, liegt die effectiveTime fünf Jahre zurück.
- low ("Beginn des Problems")
- Entspricht dem Zeitpunkt, zu dem das Problem erstmals aufgetreten ist (z.B. der Start der Erkrankung oder Beginn der Symptome). Kann auch unbekannt sein (nullFlavor "UNK")
- high ("Ende des Problems")
- Gibt den Zeitpunkt an, seit dem die zugrunde liegende Erkrankung nicht mehr besteht ("Zustand nach" oder "status post"). Wenn es nicht angegeben ist, gilt das Problem als weiterhin bestehend. Wenn bekannt ist, dass das Problem nicht mehr auftritt, dann MUSS ein effectiveTime.high angegeben werden. Wenn das Datum der Lösung nicht bekannt ist, dann wird der nullFlavor "UNK" angegeben.
11.4.11.2 Weitere Informationen[Bearbeiten]
Das Problem Entry erlaubt die Angabe weiterer Informationen zum Problem:
- qualifier: Typ der Diagnose (Haupt-, Nebendiagnose, Dauerdiagnose)
- targetSiteCode / Laterality Qualifier: Seitenlokalisation und anatomische Lage (links, rechts)
- Problem Status Observation: Medizinischer Status des Gesundheitsproblems (bestehend, nicht mehr bestehend)
- Certainty Observation: Diagnosesicherheit (bestätigt, unbestätigt, Verdacht, ...)
- Severity Observation: Schweregrad der Erkrankung (schwer, mittel, leicht)
- Comment Entry: Kommentar
Ob das Problem codiert angegeben werden muss und welche Codesysteme zur Anwendung kommen müssen bzw. sollen, ergibt sich aus dem jeweiligen speziellen Implementierungsleitfaden.
11.4.11.3 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.6 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 12:55:41 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.1.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_entry_Problem | Bezeichnung | Problem Entry |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.6 Problem Entry (2020‑11‑06 10:08:41) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.3.6 Problem Entry (2019‑01‑18 09:59:00) ref at-cda-bbr- Adaptation: Template 1.3.6.1.4.1.19376.1.5.3.1.4.5 IHE Problem Entry (DYNAMIC) ref ch-pcc- Spezialisierung: Template 2.16.840.1.113883.10.12.303 CDA Observation (2005‑09‑07) ref ad1bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4.12 Severity Observation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.38 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 13:00:38 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_entry_SeverityObservation | Bezeichnung | Severity Observation | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Dokumentation des Schweregrades des Gesundheitsproblems | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.38 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.38 Severity Observation (2019‑11‑21 09:31:57) ref at-cda-bbr- Adaptation: Template 1.3.6.1.4.1.19376.1.5.3.1.4.1 eHDSI Severity (DYNAMIC) ref epsos- Adaptation: Template 2.16.840.1.113883.10.22.4.25 IPS Severity Observation (DYNAMIC) ref hl7ips- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4.13 Certainty Observation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.36 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 12:42:49 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_entry_CertaintyObservation | Bezeichnung | Certainty Observation | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Dokumentiert die Gewissheit, mit der das Gesundheitsproblem besteht | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.36 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.36 Certainty Observation (2019‑11‑21 09:11:18) ref at-cda-bbr- Adaptation: Template 2.16.840.1.113883.10.22.4.19 IPS Certainty Observation (DYNAMIC) ref hl7ips- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4.14 Problem Status Observation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.49 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 12:55:53 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_entry_ProblemStatusObservation | Bezeichnung | Problem Status Observation | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Klinischer Status des Gesundheitsproblems | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.49 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.49 Problem Status Observation (2019‑12‑03 09:46:18) ref at-cda-bbr- Adaptation: Template 1.3.6.1.4.1.19376.1.5.3.1.4.1.1 Entry Problem Status Observation (2013‑12‑20) ref epsos- Adaptation: Template 2.16.840.1.113883.10.22.4.20 IPS Problem Status Observation (DYNAMIC) ref hl7ips- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4.15 Comment Entry[Bearbeiten]
11.4.15.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.11 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 12:42:56 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabrr_entry_Comment | Bezeichnung | Comment Entry |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.11 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.11 Comment Entry (2019‑02‑07 13:10:44) ref at-cda-bbr- Spezialisierung: Template 1.3.6.1.4.1.19376.1.5.3.1.4.2 Comment (2013‑12‑20) ref epsos- Spezialisierung: Template 2.16.840.1.113883.10.20.1.40 Befundtext (Anmerkungen und Kommentare)-deprecated (DYNAMIC) ref elga- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.4.16 External Document Entry[Bearbeiten]
11.4.16.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.3.14 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 12:43:40 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_entry_externalDocument | Bezeichnung | External Document Entry | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Dokumentenverweis. Mehrere Quell-Dokumente können angegeben werden. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Elternknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.3.14 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.3.14 External Document Entry (2019‑05‑06 14:00:33) ref at-cda-bbr- Spezialisierung: Template 2.16.840.1.113883.10.12.328 CDA ExternalDocument (2005‑09‑07) ref ad1bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5 Sonstige Templates (Fragmente)[Bearbeiten]
Bei den nachfolgenden Templates handelt es sich um Compilations oder auch Template-Fragmente, die mehrfach wiederkehrende Teilabschnitte von Templates abbilden. Innerhalb einer Compilation werden keine Template-Id's angegeben, der Typ des Templates ist "nicht spezifiziert".
11.5.1 Address Compilation[Bearbeiten]
11.5.1.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.25 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 13:05:47 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_AddressCompilation | Bezeichnung | Address Compilation |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.25 Address Compilation (2019‑02‑28 14:24:14) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.2 Address Compilation Minimal[Bearbeiten]
11.5.2.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.10 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 13:44:14 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_AddressCompilationMinimal | Bezeichnung | Address Compilation Minimal | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Adressangabe in Granularitätsstufe 2 oder 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.10 Address Compilation Minimal (2021‑02‑19 13:05:57) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.9.10 Address Compilation Minimal (2019‑03‑27 11:26:08) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.9.25 Address Compilation (DYNAMIC) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.9.4 Address Information Compilation (2019‑02‑11 13:19:54) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.3 Assigned Entity[Bearbeiten]
11.5.3.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.22 ref at-cda-bbr- | Gültigkeit | 2021‑05‑26 13:50:41 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210526 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_AssignedEntity | Bezeichnung | Assigned Entity |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.22 Assigned Entity (2021‑02‑19 13:09:09) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.9.22 Assigned Entity (2019‑03‑04 12:03:36) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.4 Assigned Entity with id, name, addr and telecom[Bearbeiten]
11.5.4.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.41 ref at-cda-bbr- | Gültigkeit | 2021‑05‑11 10:40:27 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_AssignedEntityWithIdNameAddrAndTelecom | Bezeichnung | Assigned Entity with id, name, addr and telecom |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.41 Assigned Entity with id, name, addr and telecom (2021‑02‑19 13:12:12) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.9.41 Assigned Entity with id, name, addr and telecom (2020‑04‑17 10:54:57) ref at-cda-bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.5 Assigned Entity Body[Bearbeiten]
11.5.5.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.16 ref at-cda-bbr- | Gültigkeit | 2021‑05‑26 14:04:21 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210526 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_AssignedEntityBody | Bezeichnung | Assigned Entity Body |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.16 Assigned Entity Body (2021‑02‑19 13:09:15) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.9.16 Assigned Entity Body (2019‑04‑17 13:08:49) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.9.22 Assigned Entity (2019‑03‑04 12:03:36) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.6 Assigned Entity Body with name, addr and telecom[Bearbeiten]
11.5.6.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.29 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 13:44:23 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.2+20210628 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_AssignedEntityBodyWithNameAddrAndTelecom | Bezeichnung | Assigned Entity Body with name, addr and telecom |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.29 Assigned Entity Body with name, addr and telecom (2021‑02‑19 13:12:05) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.9.29 Assigned Entity Body with name, addr and telecom (2019‑05‑15 16:50:22) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.7 Author Body[Bearbeiten]
11.5.7.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.36 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 13:12:19 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_AuthorBody | Bezeichnung | Author Body |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.36 Author Body (2019‑11‑20 12:13:04) ref at-cda-bbr- Spezialisierung: Template 2.16.840.1.113883.10.12.318 CDA Author (Body) (2005‑09‑07) ref ad1bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.8 Device Compilation[Bearbeiten]
11.5.8.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.18 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 13:57:36 | ||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | |||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_DeviceCompilation | Bezeichnung | Device Compilation | ||||||||||||||||||||||||||||||||||
| Beschreibung | Datenerstellende Geräte/Software | ||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | ||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.18 Device Compilation (2021‑02‑19 13:12:38) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.9.18 Device Compilation (2019‑02‑13 10:11:00) ref at-cda-bbr- Spezialisierung: Template 2.16.840.1.113883.10.12.315 CDA Device (2005‑09‑07) ref ad1bbr- | ||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
11.5.9 Informant Body[Bearbeiten]
11.5.9.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.3 ref at-cda-bbr- | Gültigkeit | 2021‑10‑04 08:03:25 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 2.0.0+202109 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_InformantBody | Bezeichnung | Informant Body |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.3 Informant Body (2021‑02‑19 13:12:43) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.9.3 Informant Body (2019‑02‑07 13:29:32) ref at-cda-bbr- Adaptation: Template 2.16.840.1.113883.10.12.319 CDA Informant (Body) (2005‑09‑07) ref ad1bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.10 Laterality Qualifier[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.42 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 12:51:12 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_entry_LateralityQualifier | Bezeichnung | Laterality Qualifier | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Entry Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.42 Laterality Qualifier (2020‑02‑20 09:00:36) ref at-cda-bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.11 Narrative Text Reference[Bearbeiten]
11.5.11.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.1 ref at-cda-bbr- | Gültigkeit | 2021‑05‑06 09:38:20 | ||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210512 | |||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabrr_other_NarrativeTextReference | Bezeichnung | Narrative Text Reference |
| |||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | ||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.1 Narrative Text Reference (2021‑02‑19 13:12:50) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.9.1 Narrative Text Reference (2019‑01‑17 15:27:17) ref at-cda-bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
11.5.12 Organization Compilation with name[Bearbeiten]
11.5.12.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.9 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 13:31:25 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_OrganizationCompilationWithName | Bezeichnung | Organization Compilation with name | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.9 Organization Compilation with name (2019‑02‑13 10:30:51) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.9.12 (2019‑02‑12 15:50:47) ref ? Spezialisierung: Template 2.16.840.1.113883.10.12.151 CDA Organization (2005‑09‑07) ref ad1bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.13 Organization Compilation with id, name[Bearbeiten]
11.5.13.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.5 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 13:57:53 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_OrganizationCompilationWithIdName | Bezeichnung | Organization Compilation with id, name | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Wiederverwendbare Compilation mit verpflichtender Angabe von name und id. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.5 Organization Compilation with id, name (2021‑02‑19 13:31:10) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.9.5 Organization Compilation with id, name (2019‑03‑25 13:43:57) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.9.12 (2019‑02‑12 15:50:47) ref ? Spezialisierung: Template 2.16.840.1.113883.10.12.151 CDA Organization (2005‑09‑07) ref ad1bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.14 Organization Compilation with id, name, tel, addr[Bearbeiten]
11.5.14.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.7 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 13:31:19 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_OrganizationCompilationWithIdNameTelAddr | Bezeichnung | Organization Compilation with id, name, tel, addr | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Wiederverwendbare Compilation mit verpflichtender Angabe von id, name, telecom und addr-Elementen. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.7 Organization Compilation with id, name, tel, addr (2019‑02‑12 15:42:02) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.9.12 (2019‑02‑12 15:50:47) ref ? Spezialisierung: Template 2.16.840.1.113883.10.12.151 CDA Organization (2005‑09‑07) ref ad1bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.15 Organization Compilation with name, addr minimal[Bearbeiten]
11.5.15.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.20 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 13:58:02 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_OrganizationCompilationWithNameAddrMinimal | Bezeichnung | Organization Compilation with name, addr minimal | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Wiederverwendbare Compilation mit verpflichtender Angabe des name-Elements. Minimale Adressangabe möglich. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.20 Organization Compilation with name, addr minimal (2021‑02‑19 13:31:31) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.9.20 Organization Compilation with name, addr minimal (2019‑04‑18 11:28:59) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.9.9 Organization Compilation with name (2019‑02‑13 10:30:51) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.9.12 (2019‑02‑12 15:50:47) ref ? Spezialisierung: Template 2.16.840.1.113883.10.12.151 CDA Organization (2005‑09‑07) ref ad1bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.16 Organization Compilation with name, addr minimal and telecom[Bearbeiten]
11.5.16.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.30 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 14:00:05 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_OrganizationCompilationWithNameAddrMinimalTelecom | Bezeichnung | Organization Compilation with name, addr minimal and telecom | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Wiederverwendbare Compilation mit verpflichtender Angabe des name-Elements. Minimale Adressangabe möglich. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.30 Organization Compilation with name, addr minimal and telecom (2021‑02‑19 13:31:37) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.9.30 Organization Compilation with name, addr minimal and telecom (2019‑05‑16 08:42:59) ref at-cda-bbr- Spezialisierung: Template 1.2.40.0.34.6.0.11.9.20 Organization Compilation with name, addr minimal (2019‑04‑18 11:28:59) ref at-cda-bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.17 Organization Name Compilation[Bearbeiten]
11.5.17.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.27 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 14:00:14 | |||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | ||||||||||||||||||||||||||||
| Name | atcdabbr_other_OrganizationNameCompilation | Bezeichnung | Organization Name Compilation | |||||||||||||||||||||||||||
| Beschreibung | Organisations-Namen werden über das Element name abgebildet. Dieser Implementierungsleitfaden lässt nur die unstrukturierte Angabe des Organisations-namens zu. | |||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | |||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.27 Organization Name Compilation (2021‑02‑19 13:31:42) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.9.27 Organization Name Compilation (2019‑03‑11 12:06:20) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.9.26 Person Name Compilation G1 (2019‑03‑11 11:40:35) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.9.6 Person Name Compilation G2 (2019‑02‑12 14:00:33) ref at-cda-bbr- | |||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
11.5.18 Original Text Reference[Bearbeiten]
11.5.18.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.2 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 13:31:48 | ||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_OriginalTextReference | Bezeichnung | Original Text Reference | ||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Verweist auf die Stelle im narrativen Text-Bereich (section.text), an der der gegebene codierte Inhalt (originalText von code oder value) beschrieben ist. | ||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | ||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.2 Original Text Reference (2019‑01‑18 10:49:11) ref at-cda-bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
11.5.19 Participant Body[Bearbeiten]
11.5.19.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.13 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 14:00:23 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_ParticipantBody | Bezeichnung | Participant Body | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.13 Participant Body (2021‑02‑19 13:35:21) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.9.13 Participant Body (2019‑04‑03 12:08:16) ref at-cda-bbr- Spezialisierung: Template 2.16.840.1.113883.10.12.821 CDA Participant (Body) SDTC (2005‑09‑07) ref ad1bbr- Adaptation: Template 2.16.840.1.113883.10.12.321 CDA Participant (Body) (2005‑09‑07) ref ad1bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.20 Performer Body[Bearbeiten]
11.5.20.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.17 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 13:36:15 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_PerformerBody | Bezeichnung | Performer Body | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Durchführende Entität der Gesundheitsdienstleistung | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kontext | Geschwisterknoten des Template-Element mit Id 1.2.40.0.34.6.0.11.9.17 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.17 Performer Body (2019‑01‑17 12:44:16) ref at-cda-bbr- Adaptation: Template 2.16.840.1.113883.10.12.323 CDA Performer (Body) (2005‑09‑07) ref ad1bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.21 Person Name Compilation G1[Bearbeiten]
11.5.21.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.26 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 13:36:38 | |||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_PersonNameCompilationG1 | Bezeichnung | Person Name Compilation G1 | |||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | In Granularitätsstufe 1 wird der Personen-Name unstrukturiert angegeben. Die einzelnen Elemente des Namens (Vorname, Nachname) werden nicht getrennt. nullflavors für Name zugelassen. | |||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | |||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.26 Person Name Compilation G1 (2019‑03‑11 11:40:35) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.9.6 Person Name Compilation G2 (2019‑02‑12 14:00:33) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||
11.5.22 Person Name Compilation G1 M[Bearbeiten]
11.5.22.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.12 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 13:36:43 | |||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_PersonNameCompilationG1M | Bezeichnung | Person Name Compilation G1 M | |||||||||||||||||||||||||||||||||||
| Beschreibung | In Granularitätsstufe 1 wird der Personen-Name unstrukturiert angegeben. Die einzelnen Elemente des Namens (Vorname, Nachname) werden nicht getrennt. Name ist Mandatory. | |||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | |||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.12 Person Name Compilation G1 M (2019‑04‑02 12:34:04) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.9.26 Person Name Compilation G1 (2019‑03‑11 11:40:35) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.9.6 Person Name Compilation G2 (2019‑02‑12 14:00:33) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||
11.5.23 Person Name Compilation G2[Bearbeiten]
11.5.23.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.6 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 13:36:49 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_PersonNameCompilationG2 | Bezeichnung | Person Name Compilation G2 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.6 Person Name Compilation G2 (2019‑02‑12 14:00:33) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.24 Person Name Compilation G2 M[Bearbeiten]
11.5.24.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.11 ref at-cda-bbr- | Gültigkeit | 2021‑02‑19 13:36:55 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.0+20210219 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_PersonNameCompilationG2M | Bezeichnung | Person Name Compilation G2 M |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | Template-Typ nicht spezifiziert | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.11 Person Name Compilation G2 M (2019‑04‑02 10:09:43) ref at-cda-bbr- Adaptation: Template 1.2.40.0.34.6.0.11.9.6 Person Name Compilation G2 (2019‑02‑12 14:00:33) ref at-cda-bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.5.25 Time Interval Information minimal[Bearbeiten]
11.5.25.1 Spezifikation[Bearbeiten]
| Id | 1.2.40.0.34.6.0.11.9.15 ref at-cda-bbr- | Gültigkeit | 2021‑06‑28 14:02:29 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | 1.0.1+20210628 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | atcdabbr_other_TimeIntervalInformationMinimal | Bezeichnung | Time Interval Information minimal | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Geschlossen (nur definierte Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Version: Template 1.2.40.0.34.6.0.11.9.15 Time Interval Information minimal (2021‑02‑19 13:37:11) ref at-cda-bbr- Version: Template 1.2.40.0.34.6.0.11.9.15 Time Interval Information minimal (2019‑04‑08 08:15:46) ref at-cda-bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
12 Liste der verwendeten Terminologien[Bearbeiten]
- ELGA_NullFlavor
- ELGA_Dokumentenklasse
- ELGA_URLScheme
- ELGA_TelecomAddressUse
- ELGA_EntityNameUse
- ELGA_EntityNamePartQualifier
- ELGA_AddressUse
- ELGA_RealmCode
- ELGA_Confidentiality
- ELGA_LanguageCode
- ELGA_AdministrativeGender
- ELGA_MaritalStatus
- ELGA_ReligiousAffiliation
- ELGA_HumanLanguage
- ELGA_LanguageAbilityMode
- ELGA_ProficiencyLevelCode
- ELGA_AuthorSpeciality
- ELGA_InformationRecipientType
- ELGA_PersonalRelationship
- ELGA_InsuredAssocEntity
- ELGA_ServiceEventPerformer
- ELGA_ActEncounterCode
- ELGA_Medientyp
- ELGA_Sections_VS
- ELGA_ConditionStatusCode
- ELGA_Vitalparameterarten
- atcdabbr_ConditionVerificationStatus_VS
- atcdabbr_LateralityQualifierCode_VS
- atcdabbr_TopographicalModifierQualifier_VS
- atcdabbr_ProblemSeverity_VS
- atcdabbr_PracticeSetting_VS
- HL7-at_XDS-Dokumentenklassen
13 Anhang[Bearbeiten]
13.1 Anwendungsfälle für CDA-Dokumente in ELGA[Bearbeiten]
Folgende Kapitel stellen eine Zusammenfassung der Inhalte der ELGA Gesamtarchitektur<ref name="ELGA-Gesamtarchitektur" />, des Leitfadends XDS Metadaten und Usability Styleguides zum Thema e-Befunde dar. Detailinformationen sind in den entsprechenden Dokumenten nachzulesen (verfügbar auf der Homepage der ELGA GmbH). Die wesentlichen Anwendungsfälle sind
- Schreiben und Einbringen von Dokumenten
- Versionierung von Dokumenten
- Stornierung von Dokumenten
- Filtern und Suchen von Dokumenten
- Lesen von Dokumenten
13.1.1 Voraussetzungen für den Zugriff auf e-Befunde in ELGA[Bearbeiten]
Der ELGA GDA ist in ELGA angemeldet, berechtigt und besitzt eine gültige Kontaktbestätigung für den Patienten. Der Patient ist ELGA-Teilnehmer und hat keinen generellen, partiellen oder situativen Widerspruch hinsichtlich ELGA eingelegt.
13.1.2 Schreiben und Einbringen von Dokumenten[Bearbeiten]
Im Zuge der Veröffentlichung eines CDA-Dokuments in ELGA übermittelt das lokale System des ELGA-GDA als XDS Document Source ein Dokument an das, seitens des ELGA-GDA bereitzustellende, XDS Document Repository. Anschließend übernimmt das XDS Repository die Aufgabe der Übermittlung entsprechender Dokument-Metadaten an eine (ELGA) XDS Registry.
Das Dokumentdatum (clinicalDocument.effectiveTime) wird abhängig von der Dokumentenklasse gesetzt.
Die Registrierung von Dokumenten in ELGA muss je nach Trigger (u.a. abhängig von Dokumententyp, Informationssystem, Versandzeitpunkt) automatisch vom jeweiligen Informationssystem erfolgen.
13.1.2.1 Mehrsprachigkeit und grenzüberschreitender Austausch[Bearbeiten]
Ein ELGA Dokument wird grundsätzlich in deutscher Sprache erstellt. Es ist möglich, den Inhalt zusätzlich in weiteren Sprachen im Dokument anzugeben. Dokumente mit durchgängig maschinenlesbaren Inhalten können prinzipiell auch automatisiert übersetzt werden. Bestimmte Dokumente (wie z.B. Patient Summary) sollen auch für den grenzüberschreitenden Austausch von Gesundheitsdaten eingesetzt werden können.
13.1.2.2 Vorgaben zu Dokument-Metadaten (XDS-Metadaten)[Bearbeiten]
Die Metadaten für die Registrierung eines Dokuments in ELGA sind teilweise im Dokument vorhanden und teilweise explizit durch die Document Source anzugeben. Zur schnellen Übersicht ist eine tabellarische Übersicht informativ angegeben, die normative Referenz ist der Leitfaden XDS Metadaten.
Informationen, welche CDA Elemente in die welche XDS-Metadaten übernommen werden müssen ("XDS-Mapping"), wurden an den entsprechenden Stellen der Templates eingefügt.
| XDS DocumentEntry Attribut | Optio- nalität in XDS | CDA Header-Element clinicalDocument. |
Beispiel | Erklärung |
|---|---|---|---|---|
| uniqueId | M | .id | Dokumenten-Id des CDA-Dokuments
Es MUSS eine gültige und innerhalb des ID-Pools eindeutige Dokumenten-ID angegeben werden. | |
| typeCode | M | .code |
|
Dokumententyp in feiner Granularität |
| classCode | M | .code.translation |
|
Dokumentenklasse in grober Granularität |
| formatCode | M | .hl7at:formatCode |
|
Das Format des Dokuments bezüglich seiner semantischen Interoperabilität. Werte aus Value Set 1.2.40.0.34.10.61 ELGA_Formatcode |
| practiceSettingCode | M | .hl7at:practiceSettingCode |
|
Die fachliche Zuordnung des Dokumentes |
| confidentialityCode | F | .confidentialityCode |
|
Vertraulichkeitscode des Dokuments aus ValueSet "ELGA_Confidentiality" |
| languageCode | F | .languageCode |
|
Sprachcode des Dokuments |
| referenceIdList | M | .setId |
|
Eindeutige Id des Dokumentensets. Diese bleibt über alle Versionen der Dokumente gleich (initialer Wert bleibt erhalten).
Die setId SOLL unterschiedlich zur clinicalDocument.id sein. Dieses Element wird ins XDS-Attribut referenceIdList ("urn:elga:iti:xds:2014:ownDocument_setId") gemappt. |
| sourcePatientId | M [1..1] | .recordTarget.patientRole.id[1] |
|
Identifikation des Patienten im lokalen System |
| author | M [1..1] | .author |
|
Ausschließlich das erste Author-Element MUSS übernommen werden. Wenn eine Person als Autor vorhanden ist, MUSS diese vorangestellt werden. Sind mehrere Personen vorhanden, MUSS der "Hauptautor" vorgereiht werden. |
| intendedRecipient | O | .intendedRecipient |
Elemente in der Auswahl:
|
Identifikation des beabsichtigten Empfängers (Person)
Empfohlene Information für einen Empfänger ist die ID aus dem GDA-Index. Dieses Element kann ins XDS-Attribut intendedRecipient gemappt werden (derzeit von ELGA nicht unterstützt). |
| legalAuthenticator | R | .legalAuthenticator |
|
Hauptunterzeichner, Rechtlicher Unterzeichner
ACHTUNG: Nach DocumentEntry.legalAuthenticator kann jeweils nur das erste ELement (ClinicalDocument/LegalAuthenticator[1]) übernommen werden. |
| eventCodeList | R [1..*] | .serviceEvent/@classCode |
|
Hauptunterzeichner, Rechtlicher Unterzeichner
Code der Gesundheitsdienstleistung |
| serviceStartTime | R [1..1] | .documentationOf.serviceEvent
.effectiveTime.low |
Zeitpunkt des ältesten effectiveTime aus:
|
Beginn des ersten documentationOf/serviceEvent-Elements |
| serviceStopTime | R [1..1] | documentationOf.serviceEvent
.effectiveTime.high |
Zeitpunkt des jüngsten effectiveTime aus:
|
Ende des ersten documentationOf/serviceEvent-Elements |
| healthcareFacility TypeCode | M | componentOf.
encompassingEncounter. location.healthCareFacility.code |
|
Code zur Klassifizierung des GDA |
13.1.3 Versionierung von Dokumenten[Bearbeiten]
Änderungen an einem Dokument, das bereits in ELGA registriert wurde, sollen über die Registrierung einer neuen Dokumentenversion in ELGA Eingang finden. Mittels ITI-41/42 Provide and Register DocumentSet wird eine neue Version des Dokumentes geschrieben und die Metadaten der Vorversion auf den Status "deprecated" gesetzt. In den XDS-Metadaten und in den CDA-Metadaten der neuen Version werden Verweise auf das ersetzte Dokument eingetragen (Beziehungstyp "replace" (RPLC)).
Es dürfen ausschließlich Dokumente derselben Dokumentenklasse ersetzt werden. Dementsprechend muss das Metadaten-Attribut XDSDocumentEntry.classCode von ersetztem und ersetzenden Dokument ident sein (der typeCode darf sich unterscheiden). Ein Dokument darf auch durch ein älteres Dokument ersetzt werden.
Folgeversionen zu Originaldokumenten dürfen aus Gründen der rechtlichen Autorenschaft ausschließlich von jenem GDA (Organisation) registriert werden, der auch das entsprechende Originaldokument in ELGA veröffentlicht hat.
Ein bestehendes Dokument, das auf Basis eines bestimmten Leitfadens erstellt wurde, KANN auch später mit einer höheren Leitfadenversion ersetzt werden. Die Metadaten müssen entsprechend angegeben werden (formatCode).
Eventuell der Dokumentenvorversion zugeordnete individuelle Zugriffsberechtigungen werden durch das ELGA Berechtigungssystem auch auf die Nachfolgeversionen angewendet.
Neue Versionen eines Dokuments im jeweiligen Informationssystem sollen automatisch für ELGA registriert werden. In der neuen Dokumentversion sollen die Änderungen im Text erkennbar gemacht werden. Zur Kennzeichnung der Änderungen stehen spezielle Funktionen für CDA zur Verfügung die vom Referenzstylesheet entsprechend angezeigt werden können (siehe Kapitel Verwendung von Revisionsmarken).
13.1.4 Stornierung von Dokumenten[Bearbeiten]
Falls eine Korrektur des Dokumentes nicht möglich ist, kann ein Dokument auch komplett storniert werden. Dazu wird der Status des Dokumentes via ITI-57 (Metadata Update availability Status) in der Registry auf "deprecated" gesetzt, aber keine neue Dokumentenversion registriert. Ein storniertes Dokument wird daher nicht in der Dokumentliste enthalten sein, sofern nicht spezifische Anfragen gestellt werden, um deprecated-Versionen zu bekommen.
Diese Aktion ist nur in bestimmten Ausnahmefällen zulässig, z.B. wenn ein Dokument für einen falschen Patienten angelegt wurde.
Das Löschen von Dokumenten in ELGA erfolgt ausschließlich in folgenden Fällen:
- Löschen durch ELGA-Teilnehmer
- Opt-Out des ELGA-Teilnehmers
- Ablauf der gesetzlichen Aufbewahrungsfrist (GTelG2012).
13.1.5 Filtern und Suchen von Dokumenten[Bearbeiten]
ELGA ermöglicht den Zugriff auf die vollständige Liste von registrierten e-Befunden eines Patienten (entsprechend der jeweiligen Berechtigungen). Um die relevanten e-Befunde selektieren zu können, kann die Dokumentenliste nach verschiedenen Kriterien ("XDS-Metadaten") gefiltert werden. Zu den Filterkriterien zählen in XDS Metadaten wie
- classCode (Dokumentenklasse)
- typeCode (Dokumententyp)
- title (Titel des Dokuments)
- creationTime (Datum des Dokuments)
- authorPerson (Autor des Dokuments)
- availabilityStatus (Gültigkeit des Dokuments)
- serviceStartTime und serviceStopTime (Beginn und Ende der Gesundheitsleistung)
- serviceEventList ("Stichwortliste")
- …
Ein Mapping der Metadaten im CDA Header zu den entsprechenden XDS-Metadaten ist in diesem Leitfaden bei den jeweiligen Elementen beschrieben. Eine vollständige Dokumentation findet sich im Leitfaden XDS-Metadaten.<ref>http://www.elga.gv.at/cda</ref>
13.1.6 Lesen von ELGA Dokumenten[Bearbeiten]
Die ELGA-Anwendung "e-Befunde" stellt für jeden ELGA-Teilnehmer über Dokumentenverweise den Zugriff auf dezentral gespeicherte Dokumente bereit. Der ELGA-Teilnehmer kann über das ELGA-Portal Dokumente ansehen, lokal abspeichern oder ausdrucken (als PDF z.B. mittels CDA2PDF, mit eingefügter persönlicher Kennung).
Der ELGA-GDA kann auf ELGA Dokumente direkt aus seiner Software-Umgebung, entsprechend seiner Rolle und Berechtigung, über standardisierte Schnittstellen zugreifen. Grundsätzlich lassen sich die gesamte Dokumentenliste, bestehend aus deren Dokumentmetadaten (Registry Stored Query [ITI-18]) oder einzelne Dokumente eines Patienten abrufen (Retrieve Document Set [ITI-43]) und in das lokale System übernehmen.
Das ELGA-Berechtigungssystem liefert in erster Linie immer nur jene CDA-Dokumente, die im Status "approved" sind. Um Dokumente, die in den Status "deprecated" gesetzt worden sind zu lesen, müssen spezifische Anfragen (z.B. zeige alle Versionen eines bestimmten Dokumentes) gestellt werden.
13.1.6.1 Vorherige Version eines bestimmten ELGA Dokuments abrufen[Bearbeiten]
Gemäß dem XDS Document-Lifecycle sind neu veröffentlichte Dokument-Metadaten mit dem Status "approved" zu versehen. Diese ersetzen die entsprechenden Vorversionen. Technisch wird dabei ein neues Dokument, das in Beziehung vom Typ "replace" (RPLC) zur Vorversion steht, erstellt. Auch Ergänzungen zu einem bestehenden Dokument müssen direkt im betroffenen Dokument durchgeführt und anschließend als Folgeversion über die Dokumentenbeziehung "replace" (RPLC) abgebildet werden.
Das Updatedatum eines Dokuments ist in submissionTime in den XDS submissionSet Metadaten zu finden.
13.1.6.2 Darstellung von CDA Dokumenten mittels ELGA Referenzstylesheet und CDA2PDF[Bearbeiten]
Zur Darstellung der ELGA-Befunde steht das CDA-Visualization-Paket auf der ELGA-Website zur Verfügung. Dieses Paket enthält zwei unterschiedliche Tools zur Darstellung von CDA-Dokumenten: Ein Stylesheet zur Erzeugung einer HTML-Bildschirmansicht (Referenzstylesheet) und einen Generator zur Erzeugung eines druckfähigen PDF-Dokuments (CDA2PDF). Diese Tools sind speziell für die Anzeige von CDA-Dokumenten optimiert, die den Regeln des Allgemeinen CDA Implementierungsleitfadens entsprechen. Bei den Referenzstylesheets sowie dem CDA2PDF Tool wird großer Wert auf die Benutzerfreundlichkeit gelegt. Zuletzt wurde unter Beteiligung von ELGA-Benutzern und einem Usability-Experten eine kompakte, platzsparende Darstellung geschaffen.
13.1.6.2.1 Referenzstylesheet[Bearbeiten]
Das "ELGA Referenz-Stylesheet" ermöglicht eine allgemeine, einheitliche und benutzerfreundliche Darstellung von medizinischen CDA-Dokumenten (HL7 CDA Release 2.0), die gemäß der Vorgaben der ELGA CDA Implementierungsleitfäden erstellt wurden. Dabei werden die XML-Dateien mit einer XSLT-Transformation in HTML umgewandelt, die in einem Webbrowser angezeigt werden kann. Informationen zur Hinterlegung eines Stylesheets im CDA-Dokument siehe Kapitel Hinterlegung eines Stylesheets. Für bestimmte CDA Dokumente, die vollständig maschinenlesbar vorliegen (z.B. e-Medikation, e-Impfpass), können alternativ speziell auf diese Dokumentenklasse optimierte Stylesheets zur Anwendung kommen, die ebenfalls im Paket enthalten sind. Diese greifen dann auch auf die maschinenlesbaren Daten zu. Für Details zur Anwendung des Referenzstylesheets, etwa zu den umfangreichen einstellbaren Optionen oder der Darstellung von lokal gespeicherten CDA-Dateien beachten Sie bitte die im CDA-Visualization-Paket mitgelieferte readme-Datei.
13.1.6.2.1.1 Versionierung[Bearbeiten]
Sowohl das Referenzstylesheet für e-Befunde als auch das CDA2PDF Tool zieht ausschließlich den menschenlesbaren (Level 2) Teil des CDA-Dokuments für die Anzeige heran und ist damit in der Lage beliebige CDA Dokumente anzuzeigen. Das Referenzstylesheet wird aus Gründen der Abwärtskompatibilität bis dato immer in der Version 1.0 zur Verfügung gestellt. Damit ist sichergestellt, dass alle e-Befunde weiterhin dargestellt werden können (die Stylesheet-Version ist im CDA-Dokument enthalten). Sollte es wider Erwarten größere Änderungen geben, die einen Versionswechsel nötig machen (breaking changes) wird die Stylesheet-Version geändert.
13.1.6.2.1.2 Verbindlichkeit und eigene Änderungen[Bearbeiten]
Die Referenzstylesheets für e-Befunde und die e-Medikation werden von der ELGA GmbH bis auf Widerruf unentgeltlich und nicht-exklusiv sowie zeitlich und örtlich unbegrenzt, jedoch beschränkt auf Verwendungen für die Zwecke der "Clinical Document Architecture" (CDA) zur Verfügung gestellt. Veränderungen für die lokale Verwendung sind zulässig. Derartige Veränderungen (sogenannte bearbeitete Fassungen) dürfen Ihrerseits publiziert und Dritten zur Weiterverwendung und Bearbeitung zur Verfügung gestellt werden. Bei der Veröffentlichung von bearbeiteten Fassungen ist darauf hinzuweisen, dass diese auf Grundlage des von der ELGA GmbH publizierten "ELGA Referenzstylesheet" erstellt wurden. Die Anwendung sowie die allfällige Bearbeitung des "ELGA Referenzstylesheet" erfolgt in ausschließlicher Verantwortung der Anwender. Aus der Veröffentlichung, Verwendung und/oder Bearbeitung können keinerlei Rechtsansprüche gegen die ELGA GmbH erhoben oder abgeleitet werden.
13.1.6.2.2 CDA2PDF[Bearbeiten]
Mit der CDA2PDF-Suite können ELGA-konforme CDA-Dokumente zu PDF-Dokumenten transformiert werden. Das WAR-File kann auf einem Web Application Server eingespielt und verwendet werden. Das CDA2PDFOffline Paket steht auch zur offline-Nutzung zur Verfügung. Im CDA-Visualization Paket finden Sie eine umfangreiche Dokumentation zur Nutzung der CDA2PDF-Suite. Die ELGA GmbH stellt den ELGA CDA2PDF Konverter unentgeltlich zur Verfügung. Die ELGA GmbH übernimmt keine Haftung für die korrekte Funktion, etwaige Mängel, Schäden oder Folgefehler. Aus der Verwendung des vorliegenden Programmes kann keinerlei Rechtsanspruch gegen die ELGA GmbH erhoben und/oder abgeleitet werden.
Informationen zur Anpassung des Stylesheets mittels Parametern sind unter ELGA Referenz-Stylesheet zu finden.
Ein Downloadpaket zum Thema CDA-Darstellung (inkl. Referenzstylesheets, Changelog und CDA2PDF) ist unter Technische ELGA-Leitfäden abrufbar.
13.1.6.3 Drucken von CDA Dokumenten[Bearbeiten]
Mit der CDA2PDF-Suite können ELGA-konforme CDA-Dokumente zu PDF-Dokumenten transformiert werden. Diese inkl. Benutzer- und Entwickler-Dokumentation ist ebenfalls im Downloadpaket zum Thema CDA-Darstellung unter ELGA-Leitfäden abrufbar.
13.2 Abbildungsverzeichnis[Bearbeiten]
<references group="Abbildung"/>
13.3 Tabellenverzeichnis[Bearbeiten]
<references group="Tabelle"/>
13.4 Einzelnachweise[Bearbeiten]
<references />
13.5 Literatur und Weblinks[Bearbeiten]
- Clinical Document Architcture (CDA®) Release 2.0 https://www.hl7.org/implement/standards/product_brief.cfm?product_id=7
- Boone, Keith W. "The CDA-Book", Springer, 2011 https://www.springer.com/gp/book/9780857293350
- Anleitungsartikel "Art-Decor-Tabellen verstehen (auf wiki.hl7.at)".
13.6 Revisionsliste[Bearbeiten]
13.6.1 Hauptversion 2020 (3.0.0+20200821)[Bearbeiten]
Die Hauptversion 2020 (3.0.0+20200821 nach neuem Versionsschema) wurde grundlegend überarbeitet und umstrukturiert. Auf eine Revisionsliste mit direktem Vergleich zur Vorversion wurde daher verzichtet. Eine Liste der relevanten Änderungen findet sich in Allgemeiner Implementierungsleitfaden 2020 Änderungen.
13.6.2 Nebenversion 2020.1 (3.1.0+20201120)[Bearbeiten]
Folgende Änderungen wurden in der Nebenversion 2020.1 (3.1.0+20201120 nach neuem Versionsschema) gegenüber der Hauptversion durchgeführt (weitere Details siehe Diskussionsseite):
13.6.2.1 recordTarget 1.2.40.0.34.6.0.11.1.3[Bearbeiten]
Hinzufügen von @assigningAuthorityName bei patientRole[1]/id[@root="1.2.40.0.34.4.21"] mit dem Wert "Nationaler Krankenversicherungsträger"
13.6.2.2 Document code.translation 1.2.40.0.34.6.0.11.1.16[Bearbeiten]
Das translation-Element wurde auf Unterelement von code korrigiert, war in dem Template zuvor auf derselben Ebene modelliert.
13.6.2.3 Problem Entry 1.2.40.0.34.6.0.11.3.6[Bearbeiten]
Auswahl value mit 3. Variante ergänzt; ValueSet 1.2.40.0.34.10.201 ELGA_Problems ergänzt, EntryRelationship 1.2.40.0.34.6.0.11.3.35 Criticality Observation ergänzt, Änderung von id 1..1 M auf 1..* M, Beschreibungen optimiert
13.6.2.4 Problem Concern Entry 1.2.40.0.34.6.0.11.3.7[Bearbeiten]
statusCode-Beschreibung ergänzt: Weitere statusCodes sind möglich (finden aber keine Anwendung in eHealth Austria)
13.6.2.5 Willenserklärungen und andere juridische Dokumente 1.2.40.0.34.6.0.11.2.61[Bearbeiten]
Fehlende Kardinalitäten bei 1.2.40.0.34.6.0.11.2.62 Willenserklärungen und andere juridische Dokumente - Subsektion und 1.2.40.0.34.6.0.11.2.8 Übersetzung mit 0..* ergänzt
13.6.2.6 Erweiterungen des Datentyps für effectiveTime[Bearbeiten]
Die Templates
- Messergebnis Gruppe Entry 1.2.40.0.34.6.0.11.3.70
- Messergebnis Entry 1.2.40.0.34.6.0.11.3.71
- Serienmessung Entry 1.2.40.0.34.6.0.11.3.101
- Vitalparameter Gruppe Entry 1.2.40.0.34.6.0.11.3.23
- Vitalparameter Entry 1.2.40.0.34.6.0.11.3.24
- Serienmessung Vitalparameter Entry 1.2.40.0.34.6.0.11.3.100
wurde jeweils mit einer Auswahl für drei verschiedenen effectiveTime ausgestattet, hatten vorher nur eine Variante mit low & high.
13.6.2.7 Vitalparameter - kodiert 1.2.40.0.34.6.0.11.2.46[Bearbeiten]
Die Vitaparameter Section wurde durch ein Entry für Grafiken erweitert (wie Messergebnisse)
13.6.2.8 Vitalparameter 1.2.40.0.34.6.0.11.2.46[Bearbeiten]
In der Vorversion war der Titel für die Sektion Vitalparameter fest vorgegeben. Im TmE ist diese Sektion als Untersektion von "Erhobenen Daten" angedacht, wo die einzelnen Typen, wie "Blutdruck und Puls" oder "Gewicht", als Titel gewählt werden sollen.
13.6.2.9 Korrektur der Textreference[Bearbeiten]
Bei folgenden Entrys wurde jeweils die Modellierung der Textreference korrigiert:
- Problem Entry 1.2.40.0.34.6.0.11.3.6
- Problem Status Observation 1.2.40.0.34.6.0.11.3.49
13.6.2.10 Schematron Assert in allen "Organization Compilation" Templates[Bearbeiten]
Das Schematron Assert in allen "Organization Compilation" Templates und dem "Author" Template ist strenger als sein narrativer Constraint ihn beschreibt. Deswegen wurden das Assert dort jeweils entfernt. Betrifft: Organization Compilation: representedOrganization/telecom
13.6.3 Nebenversion 3.2.0+20210304[Bearbeiten]
Folgende Änderungen wurden in der Nebenversion 3.2.0+20210304 gegenüber der Nebenversion 2020.1 (3.1.0+20201120 nach neuem Versionsschema) durchgeführt (weitere Details siehe Diskussionsseite):
13.6.3.1 Document FormatCode 1.2.40.0.34.6.0.11.1.47 & Document PracticeSettingCode 1.2.40.0.34.6.0.11.1.44[Bearbeiten]
Fehler in hl7at:practiceSettingCode und hl7at:formatCode mit fehlenden Elementen verhinderte die direkte Daten-Übernahme in XDS
13.6.3.2 DocumentLevelTemplate 1.2.40.0.34.6.0.11.0.3[Bearbeiten]
ClassCode und MoodCode-Attribute in <clinicalDocument> ergänzt
13.6.3.3 8.4.1.2.1 telecom – Format Konventionen für Telekom-Daten[Bearbeiten]
Die Einschränkung für erlaubte Zeichen betrifft nur Telefonnummern, die Beschreibung wurde verbessert.
13.6.3.4 8.1.1 id-Element II[Bearbeiten]
Fußnote zur Beschreibung der UUID hinzugefügt
13.6.3.5 recordTarget 1.2.40.0.34.6.0.11.1.3[Bearbeiten]
Hinzufügen von @assigningAuthorityName bei /ClinicalDocument[1]/recordTarget[1]/patientRole[1]/id[@root="1.2.40.0.34.4.21"] mit dem Wert "Nationaler Krankenversicherungsträger". Fehlerhafte Übernahme bei 2020.1 behoben.
13.7 Erratum[Bearbeiten]
Weitere Probleme und allfällige Korrekturen werden auf der Diskussionsseite im Wiki gesammelt.